Clear Sky Science · sv
Att förebygga trogocytos genom hämning av katepsin B ökar CAR-T-cellers funktion
Varför denna forskning är viktig för framtida cancerterapier
CAR-T-cellterapi har förvandlat behandlingen av vissa blodcancerformer och lett många patienter i djup remission. Ändå relapsar en stor andel av patienterna så småningom, ofta därför att cancerceller finner sätt att gömma sig för dessa designade immunceller. Denna studie avslöjar en tidigare dunkel flyktväg — ”trogocytos”, en process där cancerceller avger viktiga ytantigen till CAR-T-celler — och visar hur blockering av ett enda enzym kan göra CAR-T-celler mer uthålliga och effektiva.
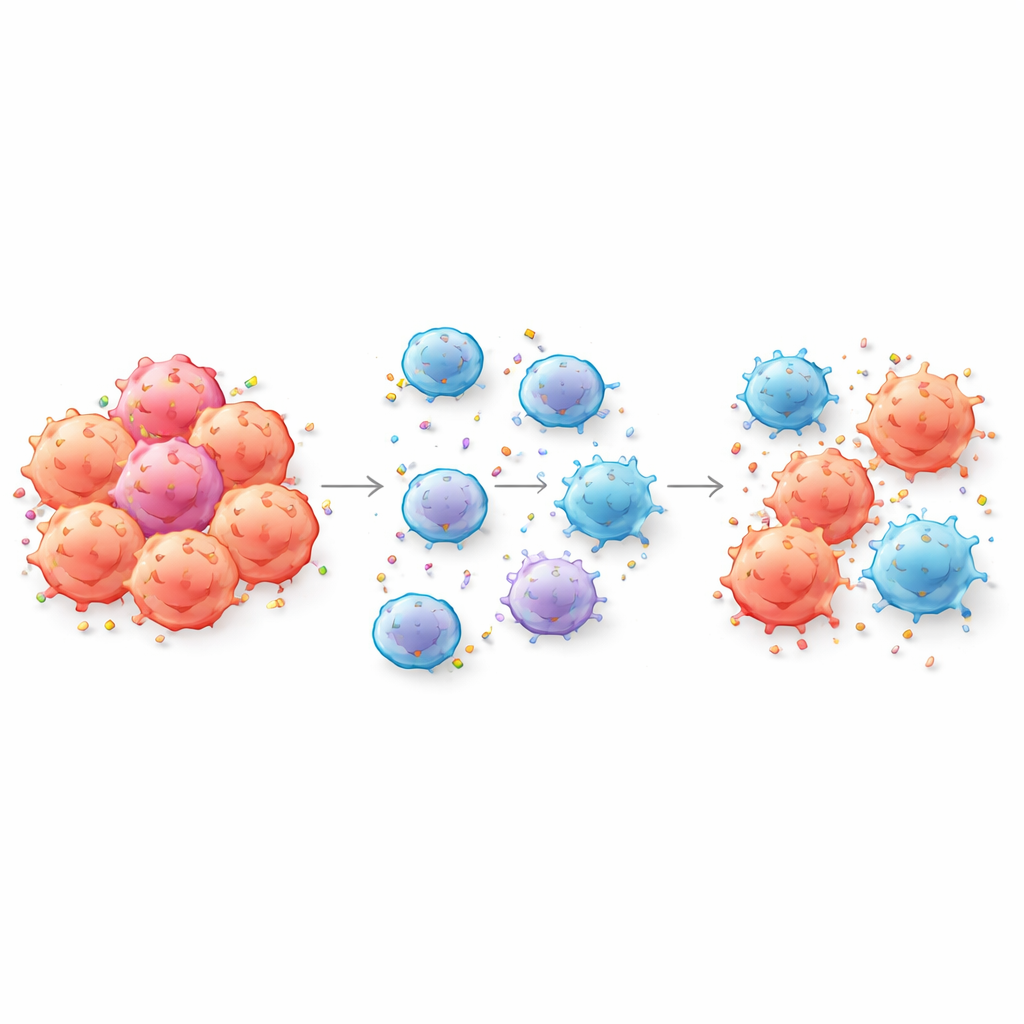
När cancerceller lämnar ifrån sig sina ID-brickor
CAR-T-celler är konstruerade för att känna igen cancer genom att binda specifika markörer, eller antigener, på tumörcellens yta. Författarna visar att i nära kontakt kan CAR-T-celler bokstavligen riva av delar av tumörens membran och införliva dessa antigener i sin egen yta — en process som kallas trogocytos. När detta sker förlorar tumörcellerna de markörer som CAR-T-cellerna behöver för att upptäcka dem, samtidigt som CAR-T-cellerna själva blir täckta av tumörantigener. Forskargruppen bekräftade denna överföring för flera kliniskt viktiga mål, inklusive CD19 och BCMA, i både blodcancer- och solida tumörmodeller, och upptäckte den till och med i patienters blod efter CAR-T-behandling.
Vänskapligt eld: hur trogocytos försvagar CAR-T-celler
När CAR-T-celler bär tumörantigener på sin egen yta börjar de känna igen varandra som mål. Det leder till ”fratricide”, där CAR-T-celler dödar andra CAR-T-celler, och till kronisk självstimulering som driver dem in i ett utmattat, mindre funktionellt tillstånd. För att bevisa att trogocytos var den direkta orsaken konstruerade forskarna ett system för att degradera trogocytiska antigener som selektivt förstör de överförda antigenerna på CAR-T-celler utan att påverka deras normala mål. Att avlägsna dessa förvärvade antigener minskade kraftigt fratricide och uppbyggnaden av utmattningsmarkörer, och gjorde att CAR-T-celler bättre kunde kontrollera leukemiceller vid upprepade utmaningar i laboratoriet.
Att spåra och dissekera processer för antigenstöld
För att studera trogocytos i realtid byggde teamet ett split-luciferas-test där ljus endast produceras när antigenfragment rör sig från tumörceller in i CAR-T-celler. Denna känsliga avläsning möjliggjorde snabb screening av cellulära processer som kan driva antigenöverföring. Med hjälp av småmolekylära hämmare upptäckte de att enzymet katepsin B, en proteas normalt involverad i nedbrytning av proteiner, är en nyckelspelare. Katepsin B rör sig snabbt till kontaktzonen där CAR-T-celler engagerar tumörceller, och dess aktivitet utanför cellen är tillräcklig för att främja avskalning och upptag av antigensrika membranfragment. Anmärkningsvärt nog minskade blockering av katepsin B starkt trogocytos utan att nämnvärt försämra CAR-T-cellernas förmåga att döda tumörceller.
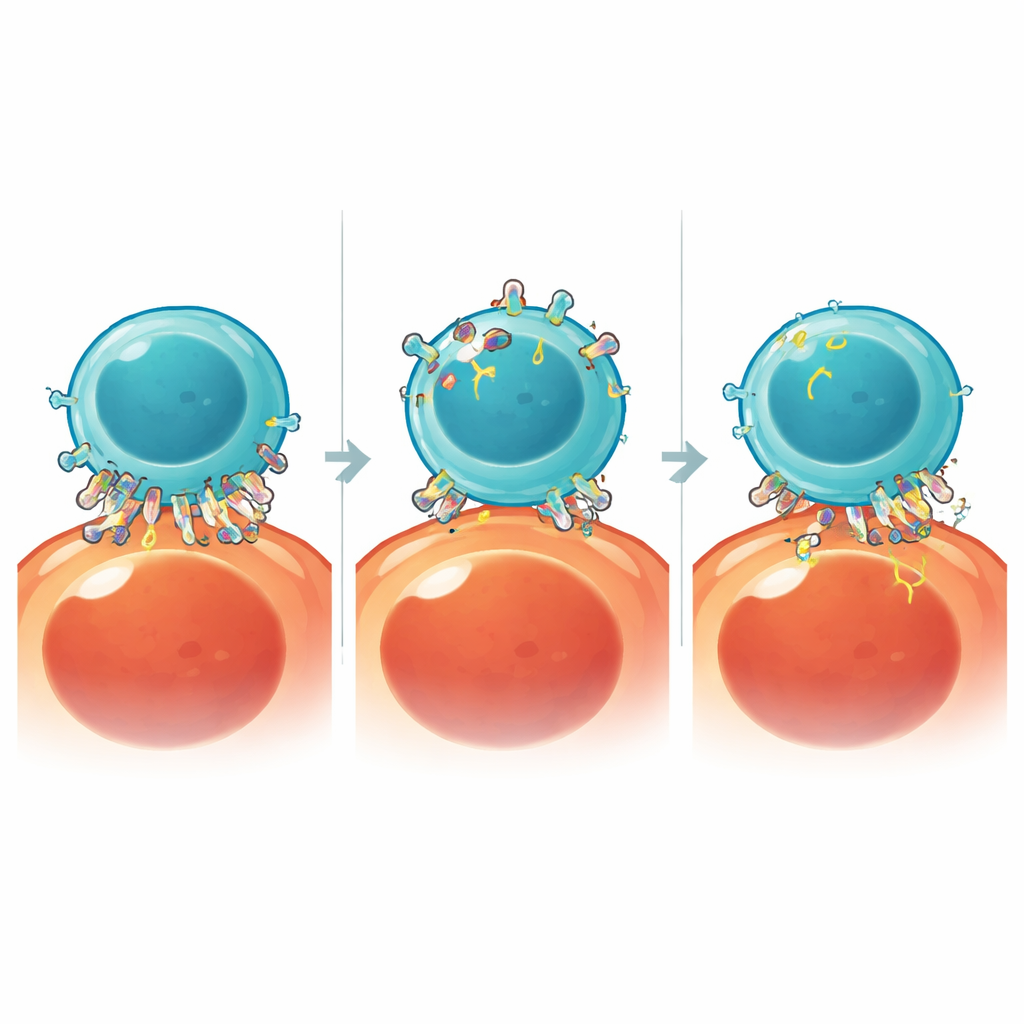
Att använda kroppens egna bromsar för att skydda CAR-T-celler
Kroppen innehåller redan inbyggda inhibitorer av katepsin B, kända som cystatiner. Forskarna ökade nivån av en av dessa, cystatin A, i CAR-T-celler och visade att detta tryggt sänkte katepsin B-aktiviteten och kraftigt reducerade trogocytos i flera tumörmodeller, inklusive primära leukemiceller från en patient. Med mindre antigenstöld överlevde CAR-T-celler bättre, ackumulerades i högre antal och upprätthöll starkare långtidskontroll över tumörer i både odlingsrätter och musmodeller. Däremot utlöste kronisk cystatin A-expression oväntat en separat intern broms — uppreglering av det regulatoriska proteinet CISH — vilket främjade tecken på T-cellsutmattning. Genom att slå ut CISH samtidigt som man överuttryckte cystatin A kunde teamet behålla fördelarna med minskad trogocytos och fratricide samtidigt som utmattningen minimerades, vilket ytterligare förlängde CAR-T-cellernas persistens.
Vad detta kan innebära för patienter
Dessa resultat ger tydliga bevis för att antigenstöld av CAR-T-celler inte bara är en nyfiken bieffekt utan en direkt orsak till behandlingssvikt, som orsakar både tumöryttring och terapeutiska cellers självförstörelse. Studien visar också att trogocytos är beroende av katepsin B och kan selektivt lösas från cancerdödande aktivitet med hjälp av antingen läkemedel eller genetiska knep som cystatin-överuttryck. I framtiden kan CAR-T-produkter som förkonstruerats för att begränsa trogocytos — eller som kombineras med smarta katepsin B-hämmare — förbli aktiva längre, hålla bättre tryck på cancerceller och minska risken för återfall.
Citering: Dietze, K.A., Nguyen, K., Pathni, A. et al. Preventing trogocytosis by cathepsin B inhibition augments CAR T-cell function. Sig Transduct Target Ther 11, 149 (2026). https://doi.org/10.1038/s41392-026-02654-z
Nyckelord: CAR T-cellterapi, trogocytos, katepsin B, cystatin A, cancerimmunterapi