Clear Sky Science · zh
用于癌症精准医学的主动矩阵数字微流控芯片上的肿瘤类器官功能性药物筛选
把癌症治疗带入芯片实验室
即便肿瘤在显微镜下看起来相似,抗癌药在不同患者身上的疗效也各不相同。这项研究描述了一种小型“实验室芯片”,可以用极少量的组织快速测试患者来源的小型肿瘤对药物的反应。目标是帮助医生为每位患者选择合适的药物和剂量,减少依靠试错的方法。
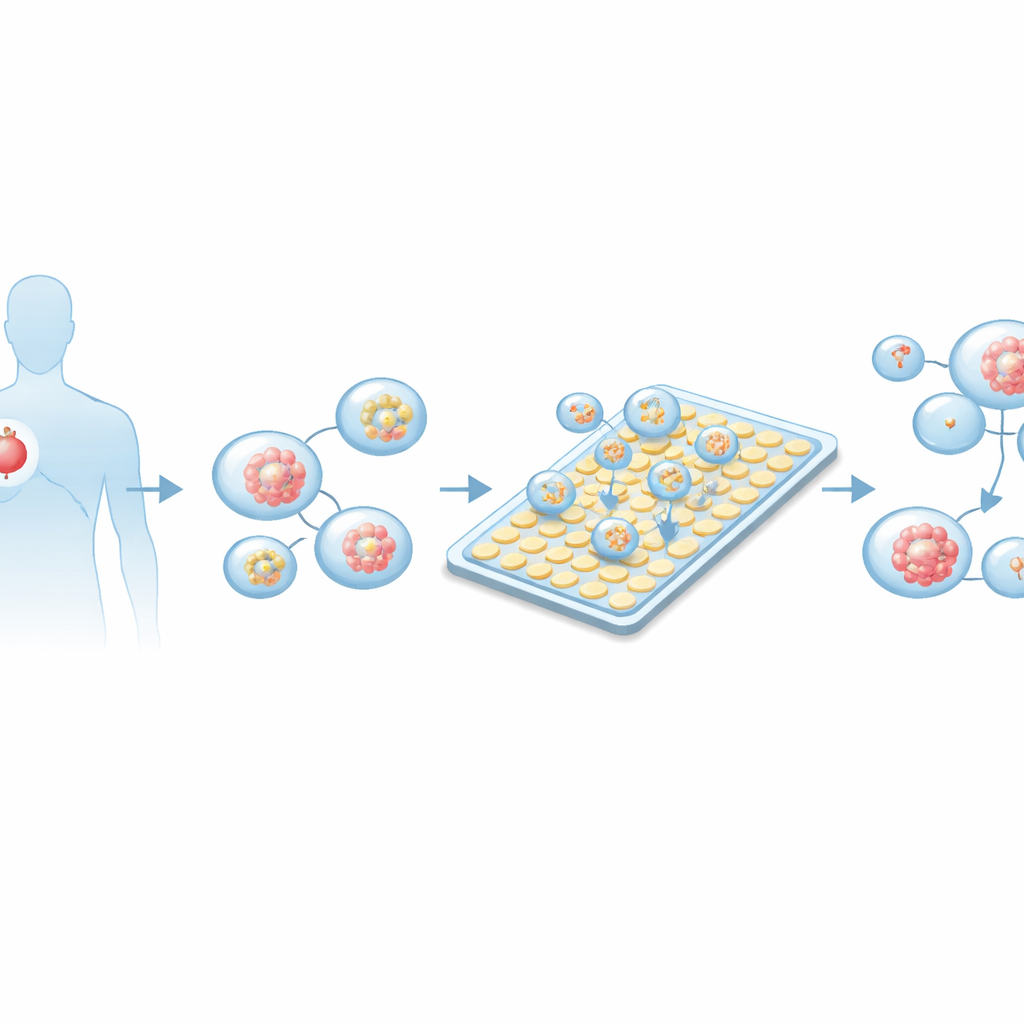
为什么微小肿瘤能指导重大决策
传统的癌症药物实验通常依赖于在塑料培养板上培养的单层细胞或动物模型。这些方法速度慢、需用大量细胞,且常常无法模拟真实人类肿瘤的行为。近年来,三维“类器官”——由患者肿瘤培养而成的微小球状细胞团——成为更可靠的替代物。它们保留了原始肿瘤的许多特征,包括遗传多样性和结构,并且常常能反映患者的真实治疗反应。然而,类器官样本十分珍贵:活检获得的细胞有限,这使得使用传统大体积方法难以进行大量药物测试。
将液滴像像素一样移动的智能芯片
研究人员基于一种称为主动矩阵数字微流控的技术进行构建。该系统不是通过窄通道推动液体,而是在平面电极网格上移动微小液滴,有点类似在屏幕上移动像素。通过开关电极,芯片可以产生、分裂、移动和混合体积小至数纳升的液滴——比典型实验体积小数千倍。主动矩阵设计在每个电极下方使用薄膜晶体管,因此大量“像素”可以用相对较少的导线进行控制。整个平台还集成了精确的温控、计时电子学和成像,使芯片成为一个自动化、自给自足的实验站。
培养患者肿瘤并装载芯片
为测试该平台,团队从多位患者的肺腺癌样本中培养了类器官。将肿瘤组织温和解离成单细胞,嵌入支持三维生长的凝胶中培养,直到形成并成熟为小型球状结构。显微镜和荧光染色确认这些类器官表达与肺肿瘤一致的标志物,并不表达其他癌种的标志物。与此同时,研究人员优化了用于装载芯片的肿瘤球体悬浮液中球体数量,以便设备上产生的大多数液滴包含一个到几个适当大小的类器官——足够成熟但不会因过大而中心坏死。
高速、高精度的药物测试
一旦含类器官的液滴被置于芯片上,系统会自动分裂并将它们排列成规则阵列。随后按步骤产生并合并含有培养基和常用化疗药顺铂的额外液滴,以形成一系列精确可控的浓度。然后将类器官液滴与这些药物液滴合并,并在类人体温下在芯片上维持长达三天。集成显微镜随时间捕捉相同的类器官,显示在较高药物剂量下12小时即可见早期收缩,72小时后结构破坏更明显。活/死荧光染色表明顺铂暴露越强,损伤细胞越多,表现为相对于绿色信号的红色信号增加。
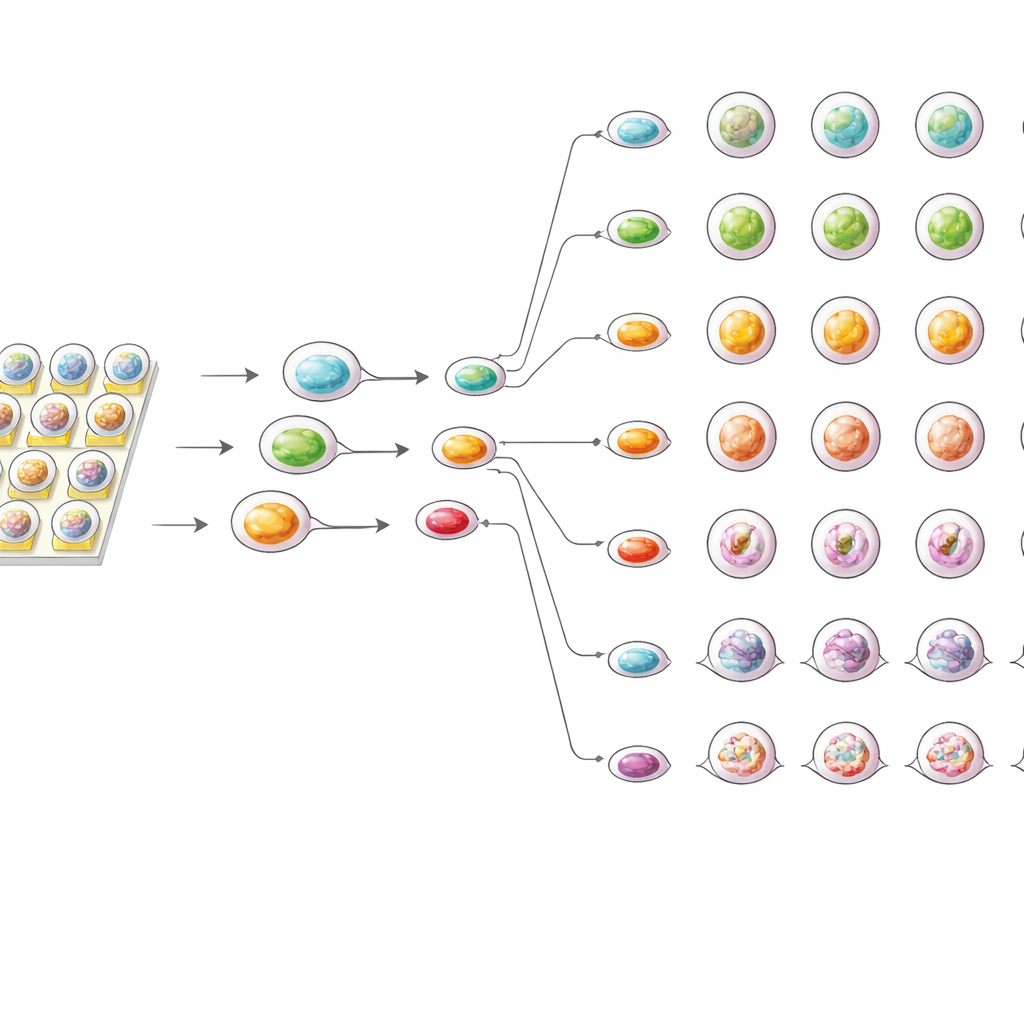
更敏锐的检测,所需样本更少
为了比较芯片与标准方法的差异,团队还在传统96孔板中测试了相同的类器官。在两种设置中,药物效应均随剂量增加而增强,并且每位患者的类器官呈现出独特的反应模式。然而,芯片上的测试一致显示对类器官生长的抑制略强、有效剂量值低于板式检测。作者认为,微小液滴环境使药物分子能更均匀、更快速地到达类器官,并防止在大孔中可能出现的有利于存活的信号积累。与此同时,芯片所需的细胞和试剂远少于常规方法,并在重复实验中产生高度可重复的结果。
从原型走向个体化癌症护理
通俗地说,这项工作表明一台掌上设备可以培养出患者肿瘤的微型版本,并在只需极少组织的情况下对其进行多剂量药物暴露。通过观察这些微型肿瘤随时间的形态变化以及存活或死亡情况,该平台能提供一种详尽的功能性药物敏感性读数,作为基因检测的补充。尽管还需要更多药物、更长培养时间的进一步验证,这种主动矩阵微流控芯片为更快速、更精准、更面向患者个体差异的癌症治疗决策提供了有前景的路径。
引用: Sun, R., Feng, Z., Wu, T. et al. Functional drug screening of tumor organoids on an active-matrix digital microfluidic chip for cancer precision medicine. Microsyst Nanoeng 12, 135 (2026). https://doi.org/10.1038/s41378-026-01215-2
关键词: 癌症精准医学, 肿瘤类器官, 微流控芯片, 药物敏感性检测, 肺腺癌