Clear Sky Science · sv
Funktionell läkemedelscreening av tumörorganoider på en aktiv-matris digital mikrofluidisk chip för precisionsmedicin vid cancer
Att föra cancerbehandling till labbet på en chip
Cancerläkemedel fungerar inte likadant hos alla patienter, även när tumörer ser liknande ut i mikroskopet. Den här studien beskriver en liten ”lab-on-a-chip” som snabbt kan testa hur en persons egna mini-tumörer reagerar på läkemedel, med hjälp av mycket små mängder vävnad. Målet är att hjälpa läkare välja rätt läkemedel, i rätt dos, för varje individ i stället för att förlita sig på försöks- och felmetoder.
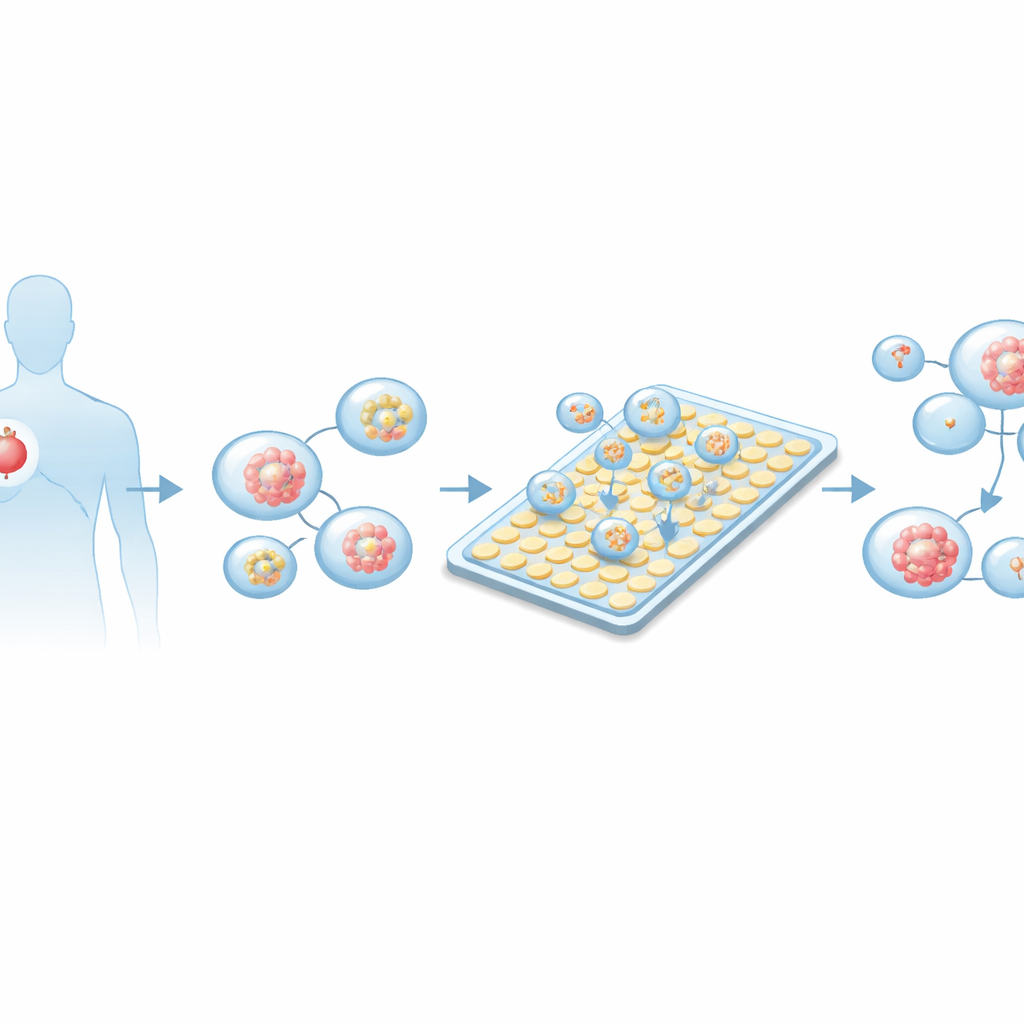
Varför små tumörer kan vägleda stora beslut
Traditionella laboratorietester för cancerläkemedel bygger vanligtvis på platta cellskikt odlade i plastplattor eller på djurmodeller. Dessa metoder är långsamma, kräver många celler och efterliknar ofta inte hur en verklig mänsklig tumör beter sig. Under de senaste åren har tredimensionella ”organoider” – små, sfäriska cellkluster odlade från en patients tumör – framträtt som mer trogna motsvarigheter. De bevarar många egenskaper hos den ursprungliga cancern, inklusive genetisk mångfald och struktur, och speglar ofta hur patienten faktiskt svarar på behandling. Organoider är dock knappa: biopsier ger få celler, vilket gör det svårt att genomföra många läkemedelstester med konventionella metoder som kräver stora volymer.
En smart chip som flyttar droppar som pixlar
Forskarna byggde vidare på en teknik kallad aktiv-matris digital mikrofluidik. I stället för att trycka vätskor genom smala kanaler rör det här systemet små droppar över ett plant rutnät av elektroder, ungefär som att förflytta pixlar på en skärm. Genom att slå på och av elektroder kan chippet skapa, dela, flytta och blanda droppar med volymer ner till några nanoliter – tusentals gånger mindre än ett typiskt labbtest. Aktiv-matrisdesignen använder tunnfilmstransistorer under varje elektrod, så ett stort antal ”pixlar” kan styras med relativt få ledningar. Den kompletta plattformen lägger till precis temperaturkontroll, tidsstyrningselektronik och integrerad bildtagning, vilket låter chippet fungera som en automatiserad, fristående experimentstation.
Att odla patienttumörer och lasta chippet
För att testa plattformen odlade teamet organoider från lungadenokarcinomprover tagna från flera patienter. Tumörvävnaden sönderdelades varsamt till enskilda celler, inbäddades i ett gelé som stödjer tredimensionell tillväxt och kulturerades tills små sfäriska strukturer bildades och mognade. Mikroskopi och fluorescerande färgning bekräftade att dessa organoider uttryckte markörer som stämde överens med lungtumörer och saknade markörer för andra cancertyper. Parallellt optimerade forskarna hur många tumorsfärer som skulle suspenderas i vätska för chip-inladdning, så att de flesta droppar genererade på enheten skulle innehålla en till några organoider av lämplig storlek – tillräckligt stora för att vara mogna, men inte så stora att kärnorna blev ohälsosamma.
Högfarts- och högprecisions läkemedelstestning
När organoidinnehållande droppar väl var på chippet delade och omarrangerade systemet dem automatiskt till regelbundna arrayer. Ytterligare droppar med odlingsmedium och ett vanligt cytostatikum, cisplatin, genererades och kombinerades stegvis för att bilda en serie noggrant kontrollerade koncentrationer. Organoiddropparna slogs sedan samman med dessa läkemedelsdroppar och hölls på chippet i upp till tre dagar vid kroppslik temperatur. Ett integrerat mikroskop fångade samma organoider över tid och avslöjade tidig krympning vid högre läkemedelsdoser redan efter 12 timmar, och mer uttalad nedbrytning av strukturen efter 72 timmar. Live/död-fluorescensfärgningar visade att starkare cisplatinexponering ledde till fler skadade celler, vilket syntes som en ökning i röd signal relativt grön.
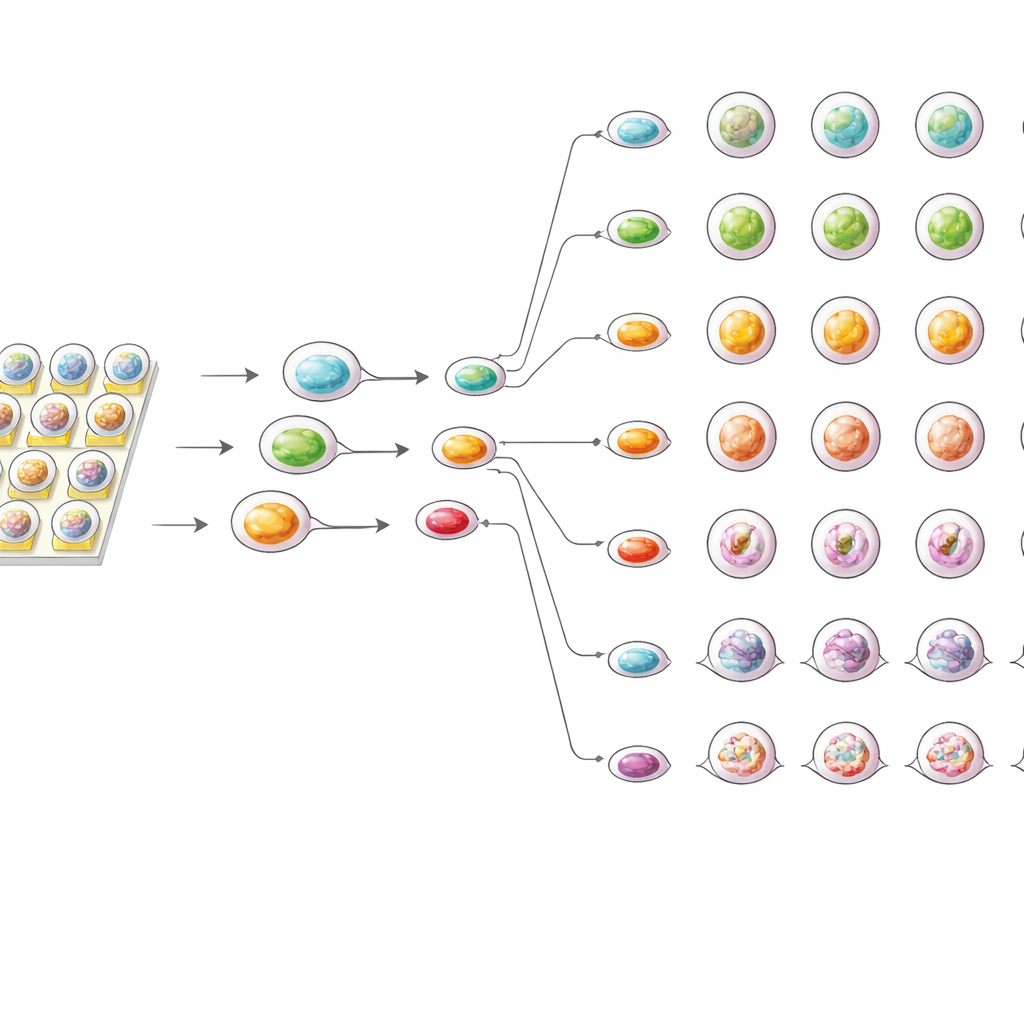
Skarpare känslighet med mindre prov
För att se hur chippet stod sig mot standardmetoder testade teamet samma organoider i konventionella 96-brunnsplattor. I båda systemen ökade läkemedelseffekterna med dosen, och varje patients organoider följde ett särskiljande responsmönster. On-chip-testerna visade dock konsekvent något starkare hämning av organoidtillväxt och lägre effektiva dosvärden än plattbaserade tester. Författarna föreslår att den lilla droppmiljön gör att läkemedelsmolekyler når organoiderna jämnare och snabbare, och förhindrar uppbyggnad av överlevnadssignaler som kan uppstå i större brunnar. Samtidigt krävde chippet långt färre celler och reagenser och gav mycket reproducerbara resultat över upprepade experiment.
Från prototyp till personlig cancervård
I praktiska termer visar detta arbete att en handflatesstor enhet kan odla miniatyrversioner av en patients tumör och utsätta dem för många doser av ett cancerläkemedel, allt med bara en bråkdel av vävnaden. Genom att iaktta hur dessa mini-tumörer förändrar form och lever eller dör över tid kan plattformen ge en detaljerad, funktionell avläsning av läkemedelskänslighet som kompletterar genetiska tester. Även om vidare validering med fler läkemedel och längre odlingstider krävs, erbjuder denna aktiv-matris mikrofluidiska chip en lovande väg mot snabbare, mer precisa och mer patientanpassade beslut i cancerbehandling.
Citering: Sun, R., Feng, Z., Wu, T. et al. Functional drug screening of tumor organoids on an active-matrix digital microfluidic chip for cancer precision medicine. Microsyst Nanoeng 12, 135 (2026). https://doi.org/10.1038/s41378-026-01215-2
Nyckelord: precisionsmedicin vid cancer, tumörorganoider, mikrofluidisk chip, läkemedelskänslighetstestning, lungadenokarcinom