Clear Sky Science · ar
فحص وظيفي للأدوية على أعضاء ورمية صغيرة باستخدام رقاقة ميكروفلويديك رقمية بمصفوفة نشطة لطب السرطان الدقيق
نقل علاج السرطان إلى مختبر على رقاقة
الأدوية المضادة للسرطان لا تعمل بنفس الطريقة مع كل مريض، حتى عندما تبدو الأورام متشابهة تحت المجهر. تصف هذه الدراسة «مختبراً على رقاقة» صغيراً يمكنه بسرعة اختبار كيفية استجابة أورام صغيرة مأخوذة من المريض للأدوية، مستخدماً كميات ضئيلة جداً من النسيج. الهدف هو مساعدة الأطباء على اختيار الدواء المناسب، بالجرعة المناسبة، لكل فرد بدلاً من الاعتماد على التجربة والخطأ.
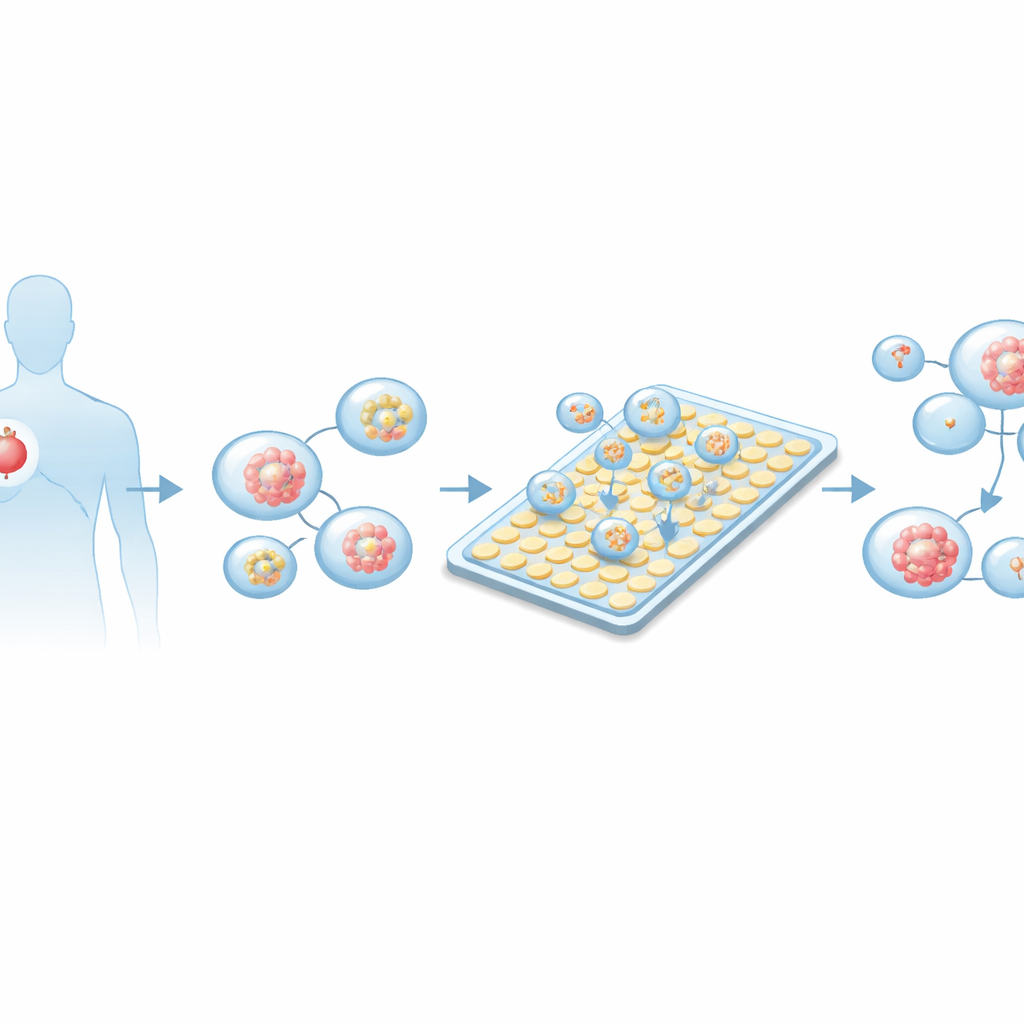
لماذا يمكن للأورام الصغيرة أن توجه قرارات كبيرة
تعتمد الاختبارات المخبرية التقليدية للأدوية عادة على طبقات مسطحة من الخلايا تنمو في أطباق بلاستيكية أو على نماذج حيوانية. هذه الطرق بطيئة، تتطلب عدداً كبيراً من الخلايا، وغالباً ما تفشل في تقليد سلوك الورم البشري الحقيقي. في السنوات الأخيرة، ظهرت «الأورغانويدات» ثلاثية الأبعاد — تجمعات خلوية كروية صغيرة تنمو من ورم المريض — كبدائل أكثر تمثيلاً. إنها تحافظ على العديد من خصائص السرطان الأصلي، بما في ذلك التنوع الجيني والبنية، وغالباً ما تعكس استجابة المريض الحقيقية للعلاج. ومع ذلك، الأورغانويدات ثمينة: عينات الخزعة توفر خلايا قليلة، مما يصعب إجراء العديد من اختبارات الأدوية بطرق الحجم الكبير التقليدية.
رقاقة ذكية تحرك القطرات مثل البكسلات
بنى الباحثون على تقنية تسمى الميكروفلويديك الرقمية ذات المصفوفة النشطة. بدلاً من دفع السوائل عبر قنوات ضيقة، يحرك هذا النظام قطرات صغيرة عبر شبكة مسطحة من الأقطاب الكهربائية، شبيهة بتحريك البكسلات على شاشة. عن طريق تشغيل وإطفاء الأقطاب الكهربائية، يمكن للرقاقة توليد، تقسيم، تحريك ومزج القطرات بحجوم تصل إلى نانولترات قليلة — أصغر بعدة آلاف من الاختبار المخبر التقليدي. يستخدم تصميم المصفوفة النشطة ترانزستورات رقيقة تحت كل قطب كهربائي، بحيث يمكن التحكم في عدد كبير من «البكسلات» بعدد نسبي قليل من الأسلاك. تضيف المنصة الكاملة تحكماً دقيقاً في الحرارة، إلكترونيات للزمن، وتصويراً مدمجاً، مما يسمح للرقاقة بأن تعمل كمحطة تجريبية مؤتمتة ومعزولة ذاتياً.
نمو أورام المرضى وتحميل الرقاقة
لاختبار المنصة، قام الفريق بزراعة أورغانويدات من عينات سرطان غدة رئوية غدية مأخوذة من عدة مرضى. تم تفكيك نسيج الورم بلطف إلى خلايا مفردة، وزرعها في هلام يدعم النمو ثلاثي الأبعاد، وحُضّنت حتى تشكلت هياكل كروية صغيرة ونمت. أكدت الميكروسكوبيات والصبغات الفلورية أن هذه الأورغانويدات تعبر عن علامات متوافقة مع أورام الرئة وتفتقر إلى علامات أنواع سرطانية أخرى. بالتوازي، حدد الباحثون العدد الأمثل للتجمعات الورمية التي يجب تعليقها في السائل لتحميل الرقاقة، بحيث تحتوي معظم القطرات المولدة على الجهاز على واحد إلى بضعة أورغانويدات بحجم مناسب — كبير بما يكفي للنضج، ولكن ليس كبيراً بحيث تصبح مراكزها غير صحية.
اختبار أدوية عالي السرعة والدقة
بمجرد وضع قطرات تحتوي الأورغانويدات على الرقاقة، قام النظام تلقائياً بتقسيمها وترتيبها في مصفوفات منتظمة. تم توليد قطرات إضافية تحتوي وسط زرعي ودواء كيماوي شائع، سيسبلاتين، ودمجها تدريجياً لتشكيل سلسلة من التراكيز المضبوطة بدقة. ثم دمجت قطرات الأورغانويدات مع قطرات الدواء واحتُفظ بها على الرقاقة لمدة تصل إلى ثلاثة أيام في درجة حرارة شبيهة بدرجة حرارة الجسم. التقطت ميكروسكوب مدمج نفس الأورغانويدات عبر الزمن، كاشفة عن تقلص مبكر عند جرعات دوائية أعلى خلال 12 ساعة تقريباً، وتفكك أكثر حدة في البنية بعد 72 ساعة. أظهرت صبغات الحي/الميت الفلورية أن التعرض الأقوى للسيسبلاتين أدى إلى مزيد من الخلايا المتضررة، مبيناً بزيادة الإشارة الحمراء مقارنة بالخضراء.
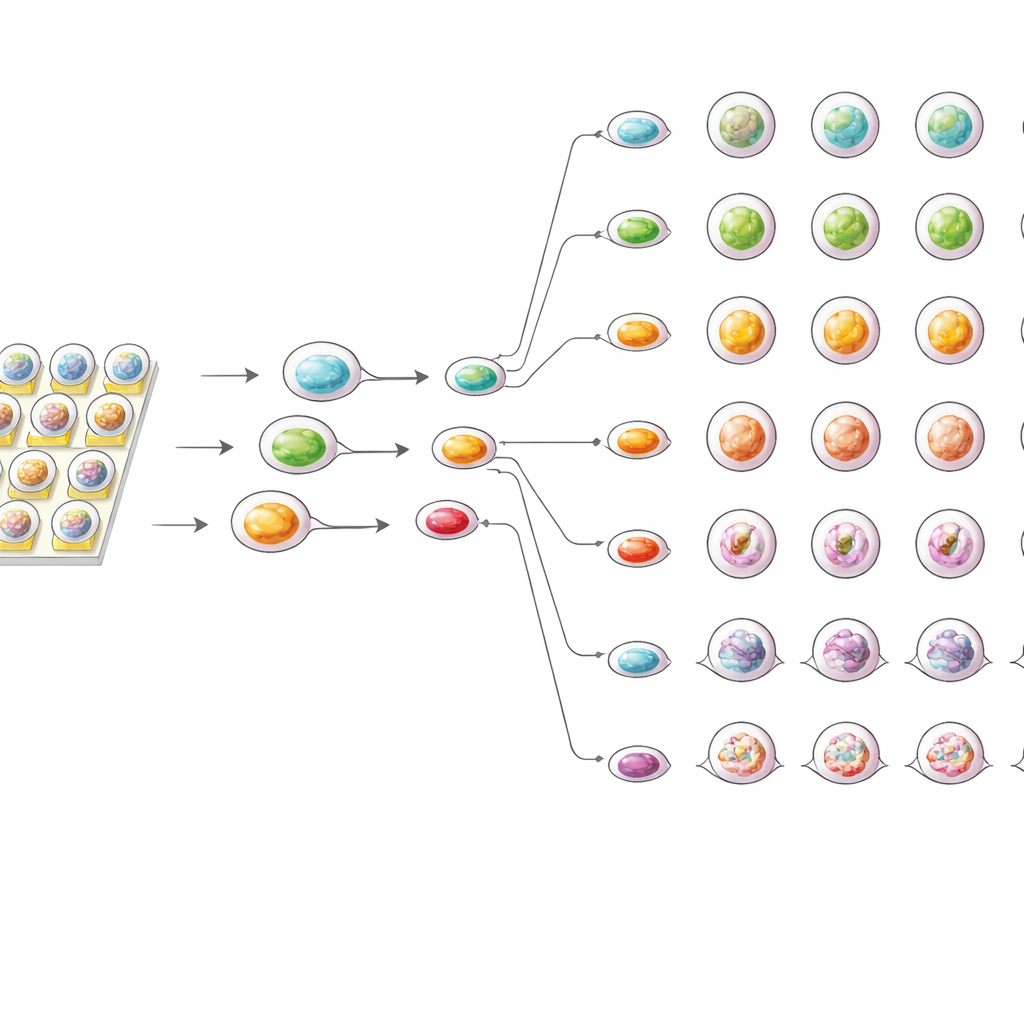
حساسية أعلى بعينة أقل
لمقارنة الرقاقة بالطرق القياسية، اختبر الفريق نفس الأورغانويدات أيضاً في أطباق 96 بئراً التقليدية. في كلا الإعدادين، زادت تأثيرات الدواء مع الجرعة، وتبعت أورغانويدات كل مريض نمط استجابة مميزاً. مع ذلك، أظهرت الاختبارات على الرقاقة باستمرار تثبيطاً أقوى لنمو الأورغانويدات وقيم جرعة فعالة أقل مقارنة بالاختبارات القائمة على الأطباق. يقترح المؤلفون أن بيئة القطرات الصغيرة تسمح لجزيئات الدواء بالوصول إلى الأورغانويدات بشكل أكثر توازناً وسرعة، وتمنع تراكم إشارات البقاء التي قد تحدث في الآبار الأكبر حجماً. وفي الوقت نفسه، احتاجت الرقاقة إلى عدد أقل بكثير من الخلايا والمواد الكاشفة ووفرت نتائج قابلة للتكرار بدرجة عالية عبر التجارب المتكررة.
من النموذج الأولي إلى رعاية سرطان مخصصة
بعبارات بسيطة، تُظهر هذه العمل أن جهازاً بحجم الكف يمكنه زراعة نسخ مصغرة من ورم المريض وتعريضها لجرعات متعددة من دواء السرطان، مع استخدام جزء صغير فقط من النسيج. من خلال مراقبة كيفية تغير شكل هذه الأورام الصغيرة وابقائها على قيد الحياة أو موتها مع مرور الوقت، يمكن للمنصة أن تقدّم قراءة وظيفية مفصّلة لحساسية الدواء تُكمّل الاختبارات الجينية. وعلى الرغم من الحاجة إلى مزيد من التحقق باستخدام أدوية أكثر وأوقات زراعة أطول، فإن رقاقة الميكروفلويديك ذات المصفوفة النشطة تقدم طريقاً واعداً نحو قرارات أسرع وأكثر دقة وتفصيلاً حسب المريض في علاج السرطان.
الاستشهاد: Sun, R., Feng, Z., Wu, T. et al. Functional drug screening of tumor organoids on an active-matrix digital microfluidic chip for cancer precision medicine. Microsyst Nanoeng 12, 135 (2026). https://doi.org/10.1038/s41378-026-01215-2
الكلمات المفتاحية: الطب الدقيق لمرض السرطان, الأورغانويدات الورمية, رقاقة ميكروفلويديك, اختبار حساسية الدواء, سرطان غدة رئوية غدية