Clear Sky Science · de
Funktionelle Wirkstoff-Screenings an Tumor-Organoiden auf einem Active-Matrix-Digital-Microfluidic-Chip für die präzisionsmedizinische Onkologie
Krebsbehandlung ins Labor-auf-einer-Platine bringen
Krebsmedikamente wirken nicht bei jeder Patientin und jedem Patienten gleich, selbst wenn Tumoren unter dem Mikroskop ähnlich aussehen. Diese Studie beschreibt ein winziges „Labor-auf-einer-Platine“, das schnell testen kann, wie die eigenen Mini-Tumoren einer Person auf Medikamente reagieren, und dafür nur sehr kleine Gewebemengen benötigt. Ziel ist es, Ärztinnen und Ärzten zu helfen, für jede Person das richtige Medikament in der richtigen Dosis zu wählen, statt sich auf Ausprobieren zu verlassen.
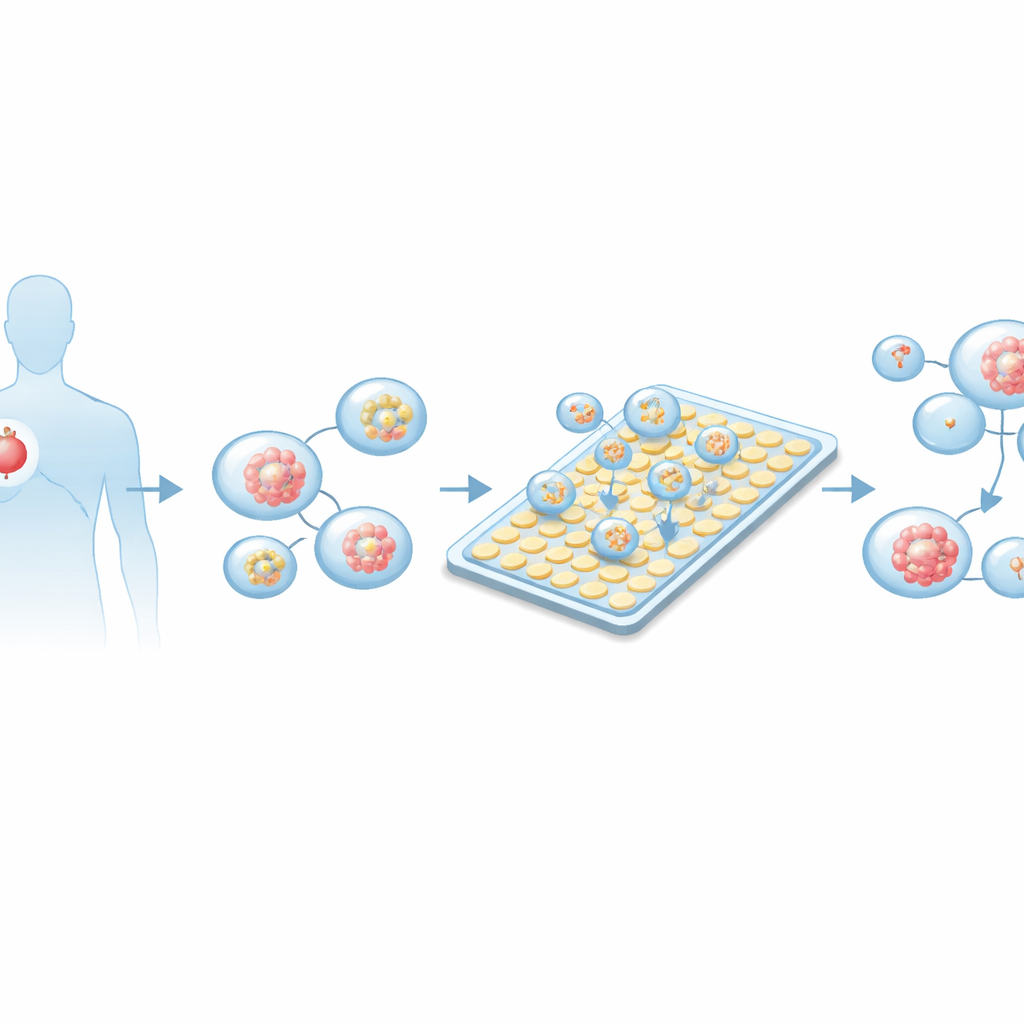
Warum winzige Tumoren große Entscheidungen leiten können
Traditionelle Labortests für Krebsmedikamente beruhen meist auf flachen Zellschichten in Plastiktellern oder auf Tiermodellen. Diese Ansätze sind langsam, benötigen viele Zellen und ahmen oft nicht nach, wie ein menschlicher Tumor wirklich funktioniert. In den letzten Jahren haben sich dreidimensionale „Organoide“ – winzige, kugelige Zellverbände aus Patiententumoren – als treuere Stellvertreter etabliert. Sie bewahren viele Eigenschaften des ursprünglichen Krebses, inklusive genetischer Vielfalt und Struktur, und spiegeln häufig wider, wie die Patientin oder der Patient tatsächlich auf eine Behandlung reagiert. Organoide sind jedoch kostbar: Biopsien liefern nur wenige Zellen, sodass mit herkömmlichen, großvolumigen Methoden nur schwer viele Wirkstofftests durchführbar sind.
Ein intelligenter Chip, der Tropfen wie Pixel bewegt
Die Forschenden bauten auf einer Technologie namens Active-Matrix-Digital-Microfluidics auf. Anstatt Flüssigkeiten durch enge Kanäle zu drücken, bewegt dieses System winzige Tröpfchen über ein flaches Gitter aus Elektroden – ähnlich dem Verschieben von Pixeln auf einem Bildschirm. Durch Ein- und Ausschalten einzelner Elektroden kann der Chip Tröpfchen erzeugen, teilen, bewegen und mischen, mit Volumina bis in den Nanoliterbereich – tausendfach kleiner als ein typischer Labortest. Das Active-Matrix-Design nutzt Dünnfilmtransistoren unter jeder Elektrode, sodass eine große Zahl von „Pixeln“ mit vergleichsweise wenigen Leitungen angesteuert werden kann. Die komplette Plattform ergänzt präzise Temperatursteuerung, Zeitsteuerungs‑Elektronik und integrierte Bildgebung, sodass der Chip als automatisierte, in sich geschlossene Versuchsstation fungiert.
Tumoren von Patientinnen und Patienten züchten und auf den Chip laden
Um die Plattform zu testen, züchtete das Team Organoide aus Lungenadenokarzinomproben mehrerer Patientinnen und Patienten. Tumorgewebe wurde schonend in Einzelzellen aufgelöst, in ein Gel eingebettet, das dreidimensionales Wachstum unterstützt, und kultiviert, bis sich kleine kugelige Strukturen bildeten und reiften. Mikroskopie und fluoreszierende Färbungen bestätigten, dass diese Organoide Marker zeigten, die mit Lungentumoren übereinstimmen, und keine Marker anderer Krebsarten exprimierten. Parallel optimierten die Forschenden die Anzahl von Tumorsphäroiden, die in Flüssigkeit suspendiert sein sollten, damit die meisten auf dem Gerät erzeugten Tröpfchen ein bis wenige Organoide passender Größe enthielten – groß genug, um ausgereift zu sein, aber nicht so groß, dass die Zentren ungesund wurden.
Hochgeschwindigkeits- und hochpräzise Wirkstofftests
Sobald Organoid-haltige Tröpfchen auf dem Chip waren, teilte und ordnete das System sie automatisch in regelmäßige Anordnungen. Zusätzliche Tröpfchen mit Kulturmedium und dem häufig verwendeten Chemotherapeutikum Cisplatin wurden erzeugt und schrittweise kombiniert, um eine Reihe präzise kontrollierter Konzentrationen zu bilden. Die Organoid-Tröpfchen wurden dann mit diesen Wirkstofftröpfchen verschmolzen und bis zu drei Tage bei körperähnlicher Temperatur auf dem Chip belassen. Ein integriertes Mikroskop erfasste dieselben Organoide über die Zeit und zeigte frühe Schrumpfungen bei höheren Wirkstoffdosen bereits nach 12 Stunden sowie stärkere Strukturzerfälle nach 72 Stunden. Live-/Dead‑fluoreszente Färbungen zeigten, dass stärkere Cisplatin-Exposition zu mehr geschädigten Zellen führte, sichtbar als Zunahme des roten Signals gegenüber dem grünen.
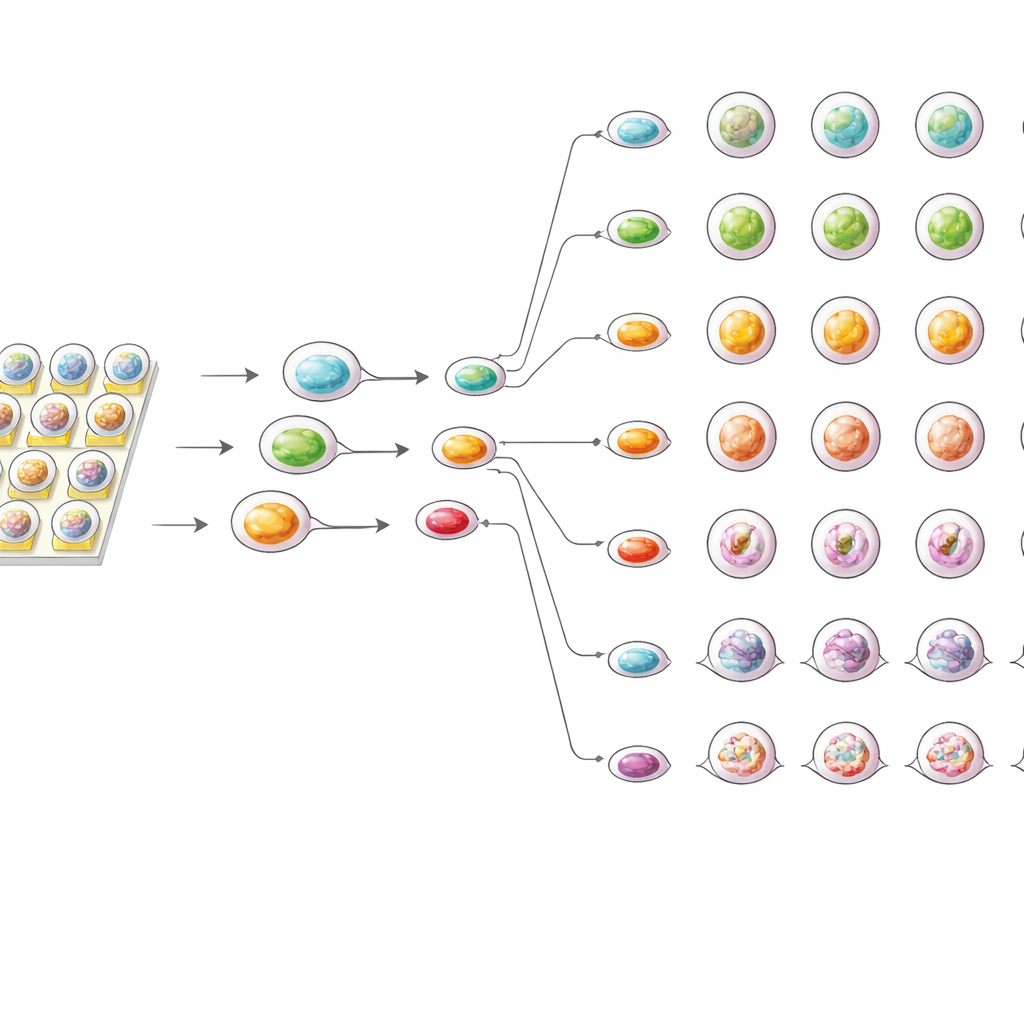
Feinere Sensitivität bei geringerem Probenverbrauch
Um den Chip mit Standardmethoden zu vergleichen, testete das Team dieselben Organoide auch in herkömmlichen 96-Well-Platten. In beiden Aufbauten nahmen die Wirkungseffekte mit der Dosis zu, und die Organoide jeder Patientin bzw. jedes Patienten folgten einem charakteristischen Reaktionsmuster. Die On‑Chip‑Tests zeigten jedoch durchgängig eine etwas stärkere Hemmung des Organoidwachstums und niedrigere effektive Dosiswerte als die Plattenassays. Die Autorinnen und Autoren vermuten, dass die winzige Tropfenumgebung Wirkstoffmolekügen erlaubt, Organoide gleichmäßiger und schneller zu erreichen, und die Ansammlung von Überlebenssignalen verhindert, die in größeren Wells auftreten kann. Gleichzeitig benötigte der Chip deutlich weniger Zellen und Reagenzien und lieferte über wiederholte Experimente hinweg hochreproduzierbare Ergebnisse.
Vom Prototyp zur personalisierten Krebsversorgung
Anschaulich zeigt diese Arbeit, dass ein handtellergroßes Gerät Miniaturausgaben des Tumors einer Patientin oder eines Patienten züchten und mit vielen Dosen eines Krebsmedikaments exponieren kann – und das mit nur einem Bruchteil des Gewebes. Indem beobachtet wird, wie sich diese Mini-Tumoren über die Zeit formen und überleben oder absterben, kann die Plattform ein detailliertes, funktionelles Messergebnis zur Wirkstoffsensitivität liefern, das genetische Tests ergänzt. Obwohl weitere Validierungen mit mehr Wirkstoffen und längeren Kulturzeiten nötig sind, bietet dieser Active‑Matrix‑Microfluidic‑Chip einen vielversprechenden Weg zu schnelleren, genaueren und individuelleren Entscheidungen in der Krebsbehandlung.
Zitation: Sun, R., Feng, Z., Wu, T. et al. Functional drug screening of tumor organoids on an active-matrix digital microfluidic chip for cancer precision medicine. Microsyst Nanoeng 12, 135 (2026). https://doi.org/10.1038/s41378-026-01215-2
Schlüsselwörter: präzisionsmedizin bei Krebs, Tumor-Organoide, mikrofluidischer Chip, Wirkstoff-Empfindlichkeitstest, Lungenadenokarzinom