Clear Sky Science · tr
Tümör organoidlerinin aktif-matris dijital mikroakışkan çip üzerinde işlevsel ilaç taraması: kanser hassas tıbbı için
Kanser Tedavisini Lab-on-a-Chip'e Taşımak
Kanser ilaçları, tümörler mikroskop altında benzer görünse bile her hastada aynı etkiyi göstermez. Bu çalışma, çok az doku kullanarak bir kişinin mini-tümörlerinin ilaçlara nasıl yanıt verdiğini hızla test edebilen küçük bir “lab-on-a-chip”i tanımlıyor. Amaç, doktorların deneme-yanılma yerine her birey için doğru ilacı ve doğru dozu seçmesine yardımcı olmak.
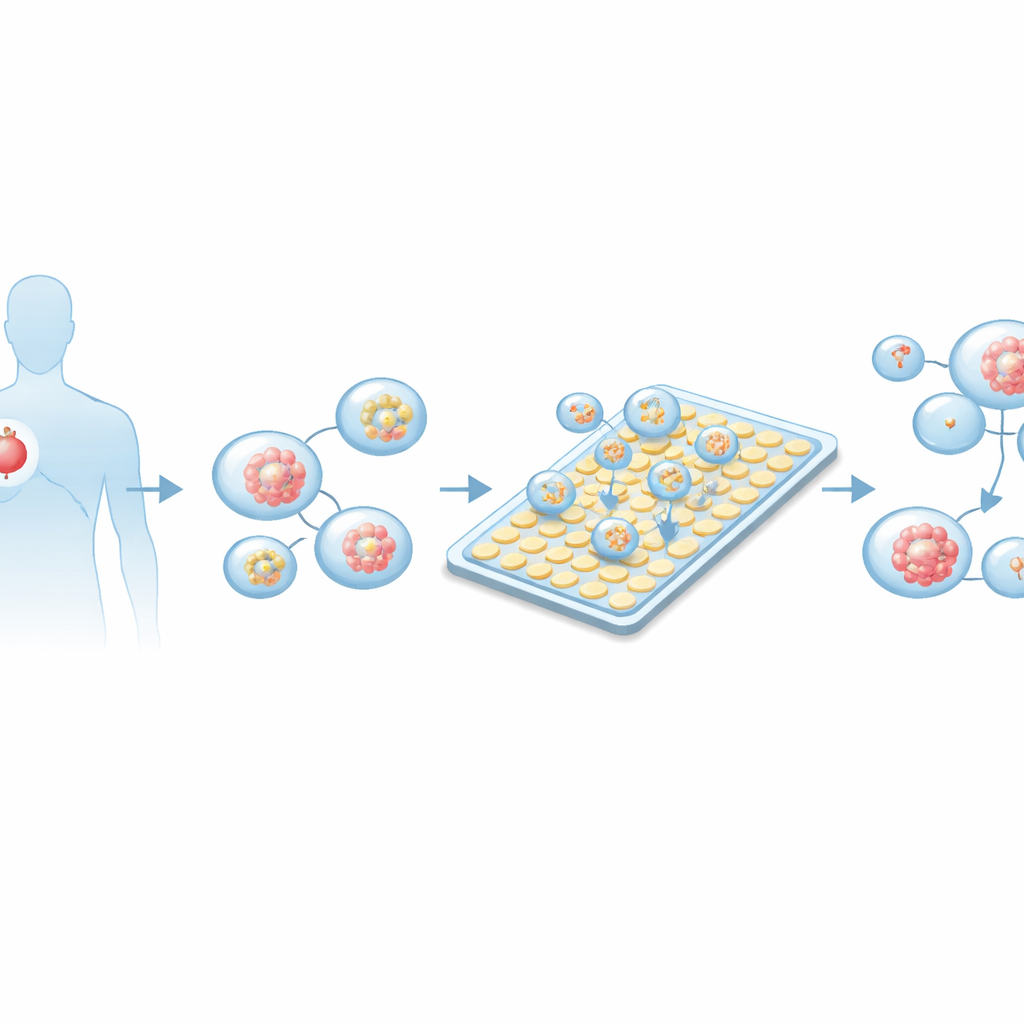
Neden Küçük Tümörler Büyük Kararlar İçin Yol Gösterir
Geleneksel kanser ilaç testleri genellikle plastik plaklarda yetiştirilen tek katmanlı hücre kültürlerine veya hayvan modellerine dayanır. Bu yaklaşımlar yavaştır, çok sayıda hücre gerektirir ve genellikle gerçek bir insan tümörünün davranışını taklit etmekte yetersiz kalır. Son yıllarda üç boyutlu “organoidler” – hastanın tümöründen türetilmiş, küçük küresel hücre kümeleri – orijinal kanserin genetik çeşitliliği ve yapısı da dahil olmak üzere birçok özelliğini koruyarak daha güvenilir modeller olarak öne çıktı. Bu organoidler sıklıkla hastanın tedaviye gerçek yanıtını da yansıtır. Ancak organoidler değerlidir: biyopsi örnekleri az sayıda hücre sağlar, bu da geleneksel büyük hacimli yöntemlerle çok sayıda ilaç testi yapmayı zorlaştırır.
Pikseller Gibi Damlacıkları Hareket Ettiren Akıllı Çip
Araştırmacılar, aktif-matris dijital mikroakışkanlık adı verilen bir teknolojinin üzerine inşa ettiler. Sıvıları dar kanallar boyunca itmek yerine, bu sistem küçük damlacıkları elektrotlardan oluşan düz bir ızgara üzerinde hareket ettirir; ekran üzerindeki pikselleri kaydırmaya benzer. Elektrotları açıp kapatarak çip, birkaç nanolitreye kadar hacimlerde damlacık oluşturabilir, bölebilir, taşıyabilir ve karıştırabilir — tipik bir laboratuvar testinden binlerce kat daha küçük. Aktif-matris tasarım, her elektrotun altında ince film transistörler kullanır, böylece çok sayıda “piksel” nispeten az tel ile kontrol edilebilir. Tam platform hassas sıcaklık kontrolü, zamanlama elektroniği ve entegre görüntüleme ekleyerek çipin otomatik, kendi içinde deney istasyonu gibi çalışmasını sağlar.
Hastadan Alınan Tümörlerin Büyütülmesi ve Çipe Yüklenmesi
Platformu test etmek için ekip, birden fazla hastadan alınan akciğer adenokarsinomu örneklerinden organoidler yetiştirdi. Tümör dokusu nazikçe tek hücrelere ayrıldı, üç boyutlu büyümeyi destekleyen bir jelde gömüldü ve küçük küresel yapılar oluşup olgunlaşana kadar kültüre edildi. Mikroskopi ve florasan boyama, bu organoidlerin akciğer tümörleri ile uyumlu belirteçler ifade ettiğini ve diğer kanser türlerinin belirteçlerini taşımadığını doğruladı. Paralel olarak, araştırmacılar çipe yükleme için kaç tane tümör sferoidinin sıvıda süspanse edilmesi gerektiğini optimize ettiler, böylece cihazda oluşturulan çoğu damlacık uygun boyutta bir veya birkaç organoid içerecek — olgun olmaya yetecek kadar büyük, fakat merkezleri sağlıksız hale gelmeyecek kadar büyük olmayan.
Yüksek Hızda, Yüksek Hassasiyetli İlaç Testleri
Organoid içeren damlacıklar çip üzerinde olduğunda, sistem bunları otomatik olarak böldü ve düzenli diziler haline getirdi. Kültür ortamı ve yaygın kullanılan bir kemoterapi ilacı olan sisplatin içeren ek damlacıklar adım adım oluşturularak hassas şekilde kontrol edilen bir dizi konsantrasyon elde edildi. Organoid damlacıkları bu ilaç damlacıklarıyla birleştirildi ve vücut benzeri sıcaklıkta çip üzerinde üç güne kadar tutuldu. Entegre bir mikroskop, aynı organoidleri zaman içinde görüntüleyerek daha yüksek ilaç dozlarında 12 saat içinde erken küçülme ve 72 saat sonra yapısal bozulmanın daha belirgin hale geldiğini gösterdi. Canlı/ölü floresan boyalar, daha güçlü sisplatin maruziyetinin daha fazla hasarlı hücreye yol açtığını; bunun yeşile kıyasla kırmızı sinyalde artış olarak görüldüğünü gösterdi.
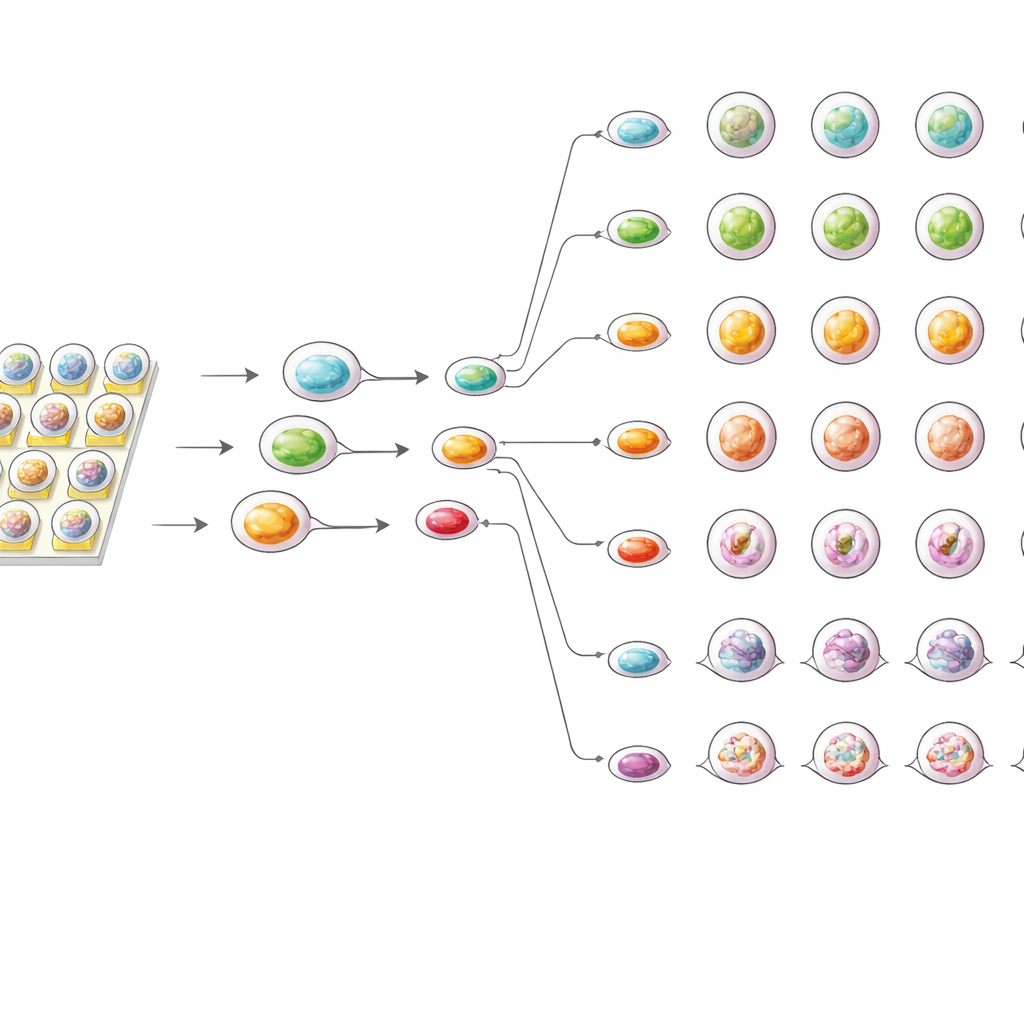
Daha Az Örnekle Daha Keskin Hassasiyet
Çipin standart yöntemlerle nasıl karşılaştırıldığını görmek için ekip aynı organoidleri geleneksel 96 kuyucuklu plaklarda da test etti. Her iki düzende de ilaç etkileri doza bağlı olarak arttı ve her hastanın organoidleri ayırt edici bir yanıt deseni izledi. Bununla birlikte, çip üzerindeki testler tutarlı şekilde organoid büyümesinin biraz daha güçlü bir şekilde inhibe edildiğini ve plaka tabanlı testlere göre daha düşük etkili doz değerleri gösterdi. Yazarlar, küçük damlacık ortamının ilaç moleküllerinin organoidlere daha eşit ve hızlı ulaşmasını sağladığını ve daha büyük kuyularda oluşabilecek hayatta kalma sinyallerinin birikimini önlediğini öne sürüyor. Aynı zamanda çip, çok daha az hücre ve reaktif gerektirdi ve tekrarlanan deneyler arasında yüksek düzeyde tekrarlanabilir sonuçlar üretti.
Prototipten Kişiselleştirilmiş Kanser Bakımına
Günlük terimlerle, bu çalışma avuç içi büyüklüğünde bir cihazın bir hastanın tümörünün minyatür versiyonlarını büyütebileceğini ve yalnızca küçük bir doku parçası kullanarak bunları birçok kanser ilacı dozuna maruz bırakabileceğini gösteriyor. Bu mini-tümörlerin zaman içinde şekil değiştirmesini ve hayatta kalma ya da ölüm durumlarını izleyerek platform, genetik testleri tamamlayıcı, ilaç duyarlılığına dair ayrıntılı işlevsel bir çıktı sağlayabilir. Daha fazla ilaç ve daha uzun kültür süreleri ile ek doğrulamaya ihtiyaç olmasına rağmen, bu aktif-matris mikroakışkan çip daha hızlı, daha doğru ve hastaya özgü kararlara doğru umut verici bir yol sunuyor.
Atıf: Sun, R., Feng, Z., Wu, T. et al. Functional drug screening of tumor organoids on an active-matrix digital microfluidic chip for cancer precision medicine. Microsyst Nanoeng 12, 135 (2026). https://doi.org/10.1038/s41378-026-01215-2
Anahtar kelimeler: kanser hassas tıbbı, tümör organoidleri, mikroakışkan çip, ilaç duyarlılık testi, akciğer adenokarsinomu