Clear Sky Science · ja
がん精密医療のためのアクティブマトリクス型デジタルマイクロフルイディクスチップ上での腫瘍オルガノイドの機能的薬剤スクリーニング
がん治療をラボオンチップへ
顕微鏡で似たように見える腫瘍であっても、がん薬が各患者で同じように作用するとは限りません。本研究は、患者自身のミニ腫瘍(オルガノイド)をごく少量の組織から迅速に薬剤反応を調べられる小型の「ラボオンチップ」を示します。目的は、試行錯誤に頼るのではなく、各個人にとって適切な薬と用量を医師が選べるようにすることです。
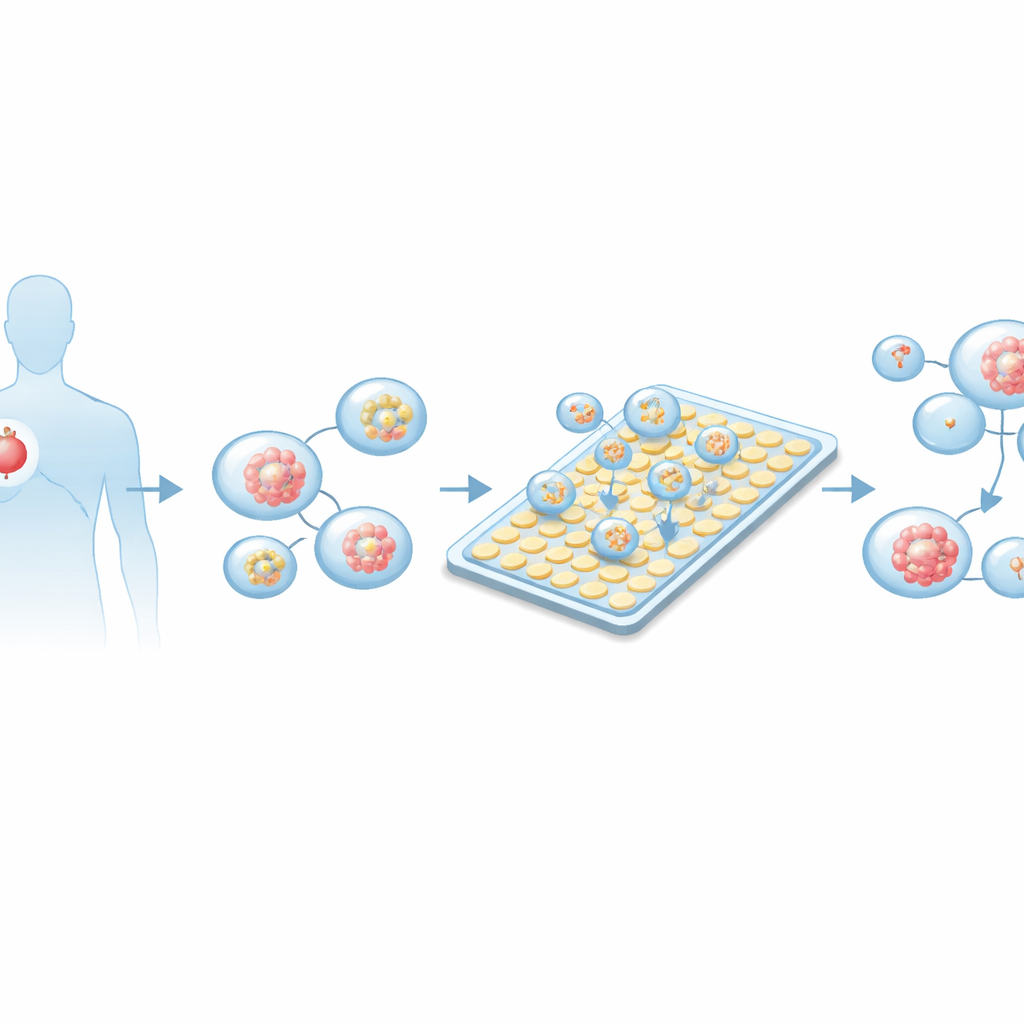
小さな腫瘍が大きな判断を導く理由
従来のがん薬の実験は、プラスチックプレート上の平面的な細胞層や動物モデルに依存することが多く、これらは時間がかかり、多くの細胞を必要とし、実際のヒト腫瘍の挙動を十分に再現できないことがあります。近年、患者の腫瘍から育てた三次元の「オルガノイド」— 小さな球状の細胞塊 — が、より忠実な代替として登場しました。これらは元のがんの遺伝的多様性や構造など多くの特徴を保持し、患者の治療反応を反映することが多いです。しかしオルガノイドは貴重で、組織生検から得られる細胞は少量であり、従来の大容量法では多くの薬剤試験を行うのが困難です。
ドロップレットをピクセルのように動かすスマートチップ
研究者たちはアクティブマトリクス型デジタルマイクロフルイディクスという技術を応用しました。細いチャンネルを通して液体を押し出す代わりに、このシステムは電極の平面グリッド上を微小な液滴として移動させます。電極をオン・オフすることで、チップは数ナノリットルまでの体積の液滴を生成、分割、移動、混合できます — 典型的な実験より何千倍も小さいスケールです。アクティブマトリクス設計では各電極の下に薄膜トランジスタを配置するため、多数の“ピクセル”を比較的少ない配線で制御できます。プラットフォームには精密な温度制御、タイミング用電子回路、統合イメージングが加わり、チップは自動化された自己完結型の実験ステーションとして機能します。
患者の腫瘍を育ててチップに搭載する
プラットフォームを検証するため、チームは複数の患者から採取した肺腺癌サンプルからオルガノイドを培養しました。腫瘍組織はやさしく解離して単一細胞にし、三次元成長を支えるゲルに埋め込んで培養し、小さな球状構造が形成・成熟するまで育てました。顕微鏡観察と蛍光標識により、これらのオルガノイドが肺腫瘍に一致するマーカーを発現し、他のがん種のマーカーを欠くことが確認されました。同時に、チップに搭載するための懸濁液中にどれくらいの腫瘍球状体を含めるべきかを最適化し、生成されるほとんどの液滴に成熟に十分だが中心が不健康になりすぎない適切なサイズのオルガノイドが1〜数個含まれるようにしました。
高速で高精度な薬剤試験
オルガノイドを含む液滴がチップ上に配置されると、システムはそれらを自動で分割・再配置して規則的な配列を作りました。培地や一般的な化学療法薬であるシスプラチンを含む追加の液滴を段階的に生成・混合して、精密に制御された濃度系列を作成しました。オルガノイド液滴はこれらの薬液滴と合体させ、体温に近い条件で最大3日間チップ上に保持されました。統合顕微鏡は同一オルガノイドを時間経過で撮影し、高用量では12時間ですでに収縮が見られ、72時間後には構造のより深刻な崩壊が明らかになりました。生死を示す蛍光染色では、シスプラチンの曝露が強いほど壊れた細胞が増え、緑に対する赤の信号が増加しました。
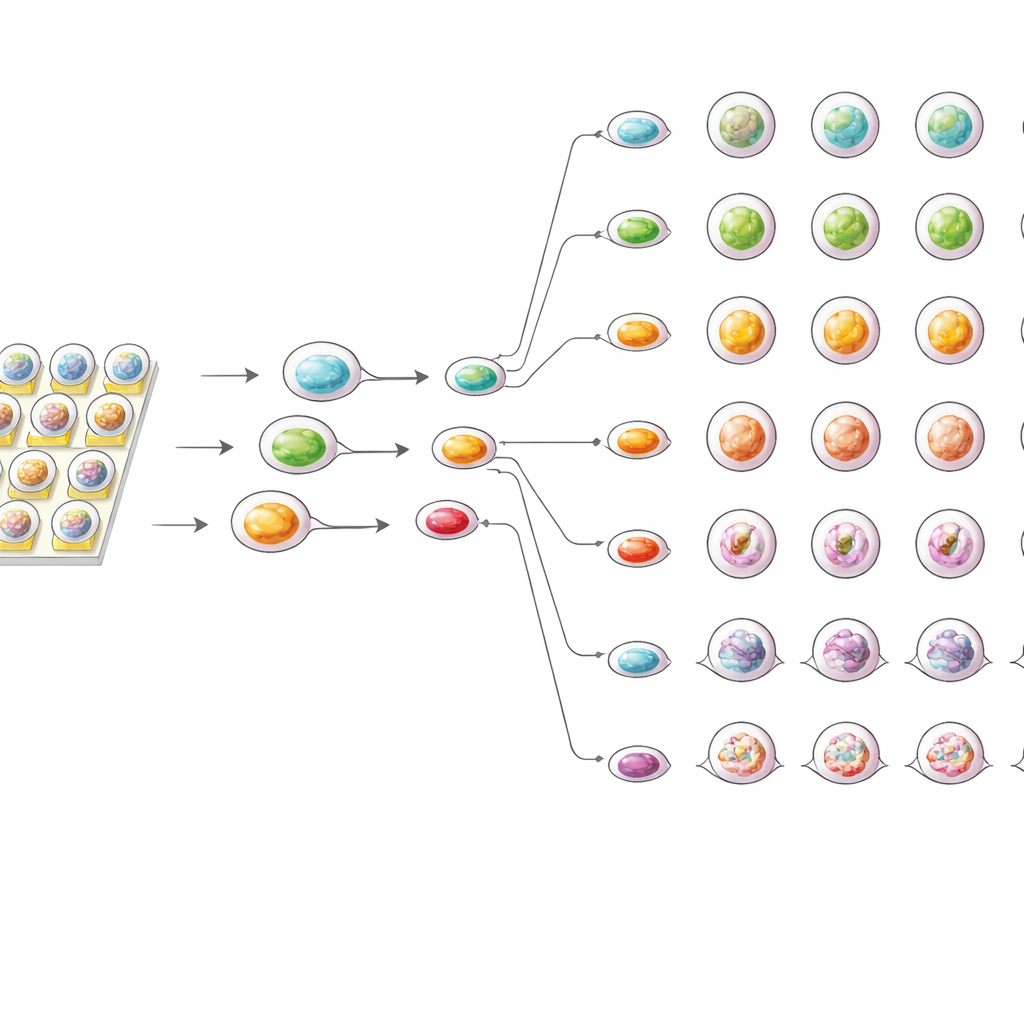
少ないサンプルでより鋭い感度
チップの結果を標準法と比較するため、同じオルガノイドを従来の96ウェルプレートでも試験しました。どちらのセットアップでも薬効は用量に伴って増加し、各患者のオルガノイドは特徴的な反応パターンを示しました。しかし、オンチップ試験は一貫してオルガノイドの成長阻害がわずかに強く、プレートベースのアッセイよりも有効濃度値が低く出ることが多かったと報告されます。著者らは、微小な液滴環境が薬剤分子をオルガノイドにより均一かつ迅速に到達させ、大きなウェルで起こり得る生存シグナルの蓄積を防ぐためだと示唆しています。同時に、チップははるかに少ない細胞と試薬で済み、繰り返しの実験間で高い再現性を示しました。
試作から個別化がんケアへ
日常的な言い方をすれば、この研究は手のひらサイズの装置が患者の腫瘍のミニ版を育て、多数の薬剤用量に曝露させることができることを示しています。それもごく少量の組織で済みます。これらのミニ腫瘍が形を変え、生存あるいは死に至る様子を時間経過で観察することで、プラットフォームは遺伝子検査を補完する詳細な機能的薬剤感受性の読み出しを提供できます。さらなる薬剤での検証や長期培養の検討は必要ですが、このアクティブマトリクス型マイクロフルイディクスチップは、より迅速で正確、かつ患者個別化されたがん治療の決定に向けた有望な道を示しています。
引用: Sun, R., Feng, Z., Wu, T. et al. Functional drug screening of tumor organoids on an active-matrix digital microfluidic chip for cancer precision medicine. Microsyst Nanoeng 12, 135 (2026). https://doi.org/10.1038/s41378-026-01215-2
キーワード: がん精密医療, 腫瘍オルガノイド, マイクロフルイディクスチップ, 薬剤感受性試験, 肺腺癌