Clear Sky Science · ru
Функциональный скрининг лекарств на опухолевых органоидах с помощью цифрового микрофлюидного чипа с активной матрицей для прецизионной онкологии
Перенос лечения рака на лабораторный чип
Противораковые препараты действуют по‑разному у разных пациентов, даже если опухоли выглядят похоже под микроскопом. В этом исследовании описан крошечный «лабораторно-на-чипе», который может быстро проверять, как мини‑опухоли пациента реагируют на лекарства, используя лишь небольшие образцы ткани. Цель — помочь врачам подобрать правильный препарат и дозу для каждого человека, вместо эмпирических попыток.
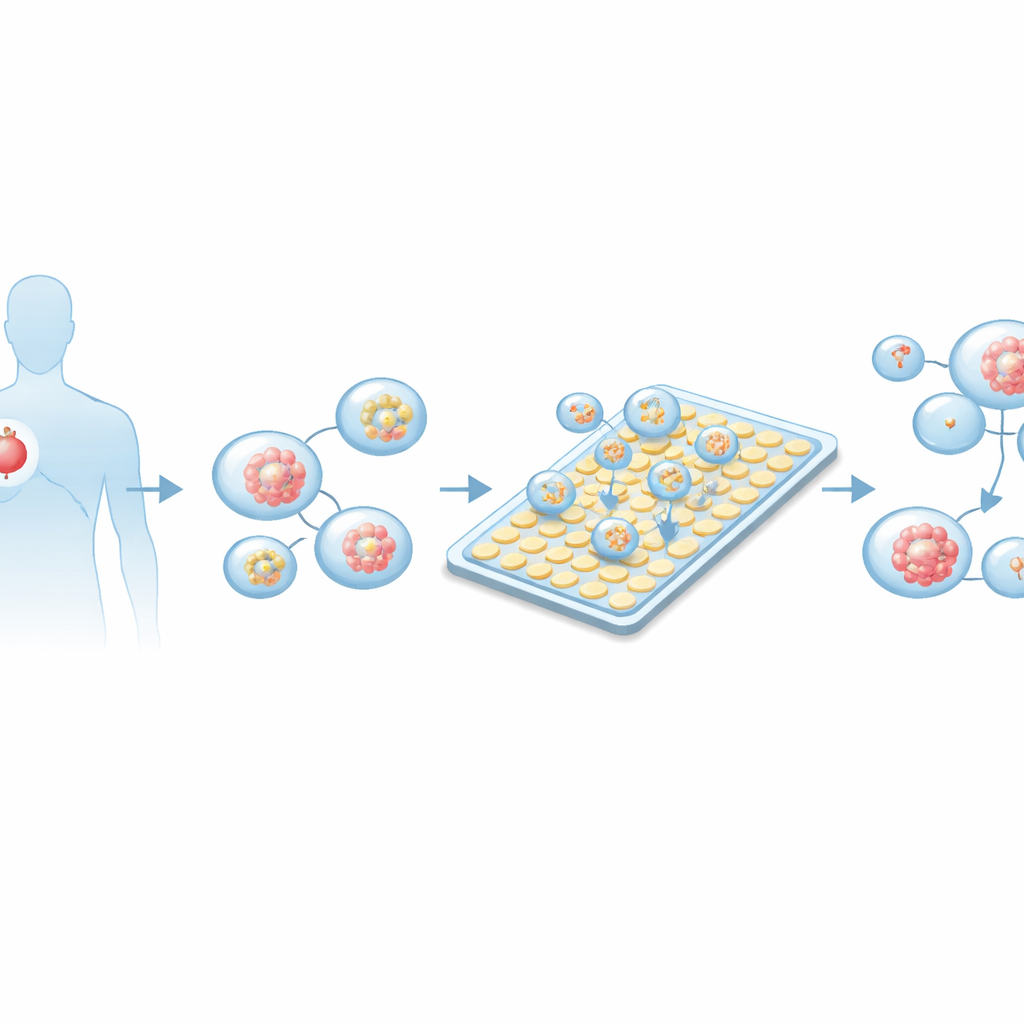
Почему крошечные опухоли помогают принимать важные решения
Традиционные лабораторные тесты противораковых препаратов обычно используют плоские слои клеток в пластмассовых планшетах или на животных моделях. Эти подходы медленные, требуют большого числа клеток и часто не воспроизводят поведение настоящей человеческой опухоли. В последние годы трехмерные «органы в чашке» — органоиды, небольшие сферические скопления клеток, выращенные из опухоли пациента, — стали более достоверной моделью. Они сохраняют многие признаки исходного рака, включая генетическое разнообразие и структуру, и часто соответствуют реальной реакции пациента на лечение. Однако органоиды — ценное сырье: из биопсии получается мало клеток, что затрудняет проведение множества тестов с использованием традиционных методов большого объема.
Умный чип, который перемещает капли как пиксели
Исследователи опирались на технологию цифровой микрофлюдики с активной матрицей. Вместо того чтобы проталкивать жидкости по узким каналам, эта система перемещает крошечные капли по плоскому массиву электродов, подобно смещению пикселей на экране. Включая и выключая электроды, чип может генерировать, делить, перемещать и смешивать капли объёмом до нескольких нанолитров — в тысячи раз меньше обычного лабораторного теста. Дизайн с активной матрицей использует тонкоплёночные транзисторы под каждым электродом, что позволяет управлять большим числом «пикселей» при сравнительно небольшом количестве проводов. Полная платформа включает точный контроль температуры, электронику для синхронизации и встроенную визуализацию, что превращает чип в автоматизированную, самодостаточную экспериментальную станцию.
Выращивание опухолей пациента и загрузка чипа
Чтобы протестировать платформу, команда вырастила органоиды из образцов аденокарциномы легкого, полученных от нескольких пациентов. Опухолевую ткань аккуратно диссоциировали до отдельных клеток, внедряли в гель, поддерживающий трехмерный рост, и культивировали до формирования и созревания небольших сферических структур. Микроскопия и флуоресцентное окрашивание подтвердили, что эти органоиды экспрессировали маркеры, характерные для легочной опухоли, и не имели маркеров других типов рака. Параллельно исследователи оптимизировали концентрацию опухолевых сфероидов в суспензии для загрузки в чип, чтобы большинство генерируемых на устройстве капель содержали одну‑две органоиды подходящего размера — достаточно большие для зрелости, но не настолько, чтобы в центре возникали нежелательные процессы гибели.
Высокоскоростное и высокоточное тестирование препаратов
После размещения капель с органоидами на чипе система автоматически делила и упорядочивала их в регулярные массивы. Дополнительные капли с питательной средой и распространенным химиотерапевтическим препаратом цисплатином генерировались и объединялись пошагово для получения ряда точно контролируемых концентраций. Затем капли с органоидами сливались с каплями с лекарством и выдерживались на чипе до трех дней при температуре, близкой к телесной. Встроенный микроскоп снимал одни и те же органоиды во времени, показывая раннее сокращение при более высоких дозах уже через 12 часов и более выраженное разрушение структуры через 72 часа. Флуоресцентные краски «живые/мертвые» продемонстрировали, что более сильное воздействие цисплатина приводило к большему числу поврежденных клеток, что проявлялось увеличением красного сигнала по отношению к зелёному.
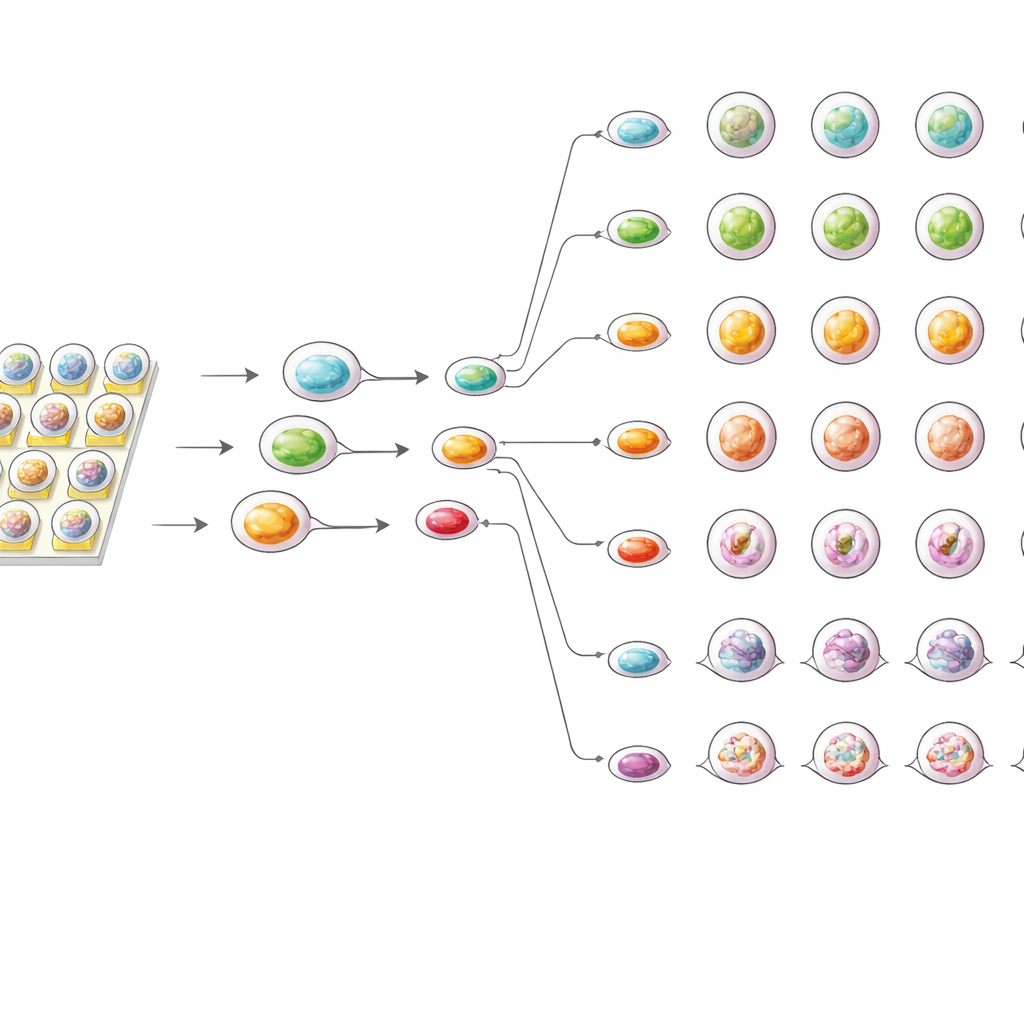
Более высокая чувствительность при меньшем объеме материала
Чтобы сравнить чип со стандартными методами, команда также протестировала те же органоиды в традиционных 96‑луночных планшетах. В обеих системах эффект препарата увеличивался с ростом дозы, и органоиды каждого пациента демонстрировали характерный профиль ответа. Однако тесты на чипе последовательно показывали чуть более сильное угнетение роста органоидов и более низкие эффективные дозы по сравнению с тестами в планшетах. Авторы предполагают, что среда с крошечными каплями обеспечивает более равномерное и быстрое достижение органоидов молекулами препарата и препятствует накоплению сигналов выживания, которые могут возникать в больших лунках. При этом чип требовал значительно меньше клеток и реагентов и давал высоко воспроизводимые результаты при повторных экспериментах.
От прототипа к персонализированной онкологической помощи
Проще говоря, работа показывает, что устройство размером с ладонь может вырастить мини‑версии опухоли пациента и подвергнуть их множественным дозам противоракового препарата, используя при этом лишь небольшой кусочек ткани. Наблюдая, как эти мини‑опухоли меняют форму и выживают или гибнут со временем, платформа предоставляет детализированный функциональный отчёт о чувствительности к лекарству, дополняющий генетические тесты. Хотя необходима дальнейшая валидация с большим числом препаратов и более длительными периодами культивирования, этот микрофлюидный чип с активной матрицей открывает перспективный путь к более быстрым, точным и персонализированным решениям в лечении рака.
Цитирование: Sun, R., Feng, Z., Wu, T. et al. Functional drug screening of tumor organoids on an active-matrix digital microfluidic chip for cancer precision medicine. Microsyst Nanoeng 12, 135 (2026). https://doi.org/10.1038/s41378-026-01215-2
Ключевые слова: прецизионная онкология, опухолевые органоиды, микрофлюидный чип, тестирование чувствительности к лекарствам, аденокарцинома легкого