Clear Sky Science · pl
Funkcjonalne badanie leków na organoidach nowotworowych na aktywnej macierzy cyfrowego mikroprzepływowego chipu dla precyzyjnej medycyny onkologicznej
Przenosząc leczenie raka do laboratorium na chipie
Leki przeciwnowotworowe nie działają jednakowo u każdego pacjenta, nawet gdy guzy wyglądają podobnie pod mikroskopem. W tym badaniu opisano niewielkie „laboratorium na chipie”, które może szybko sprawdzić, jak mini‑guzy pacjenta reagują na leki, wykorzystując bardzo małe ilości tkanki. Celem jest pomoc lekarzom w wyborze właściwego leku i dawki dla konkretnej osoby, zamiast polegania na metodzie prób i błędów.
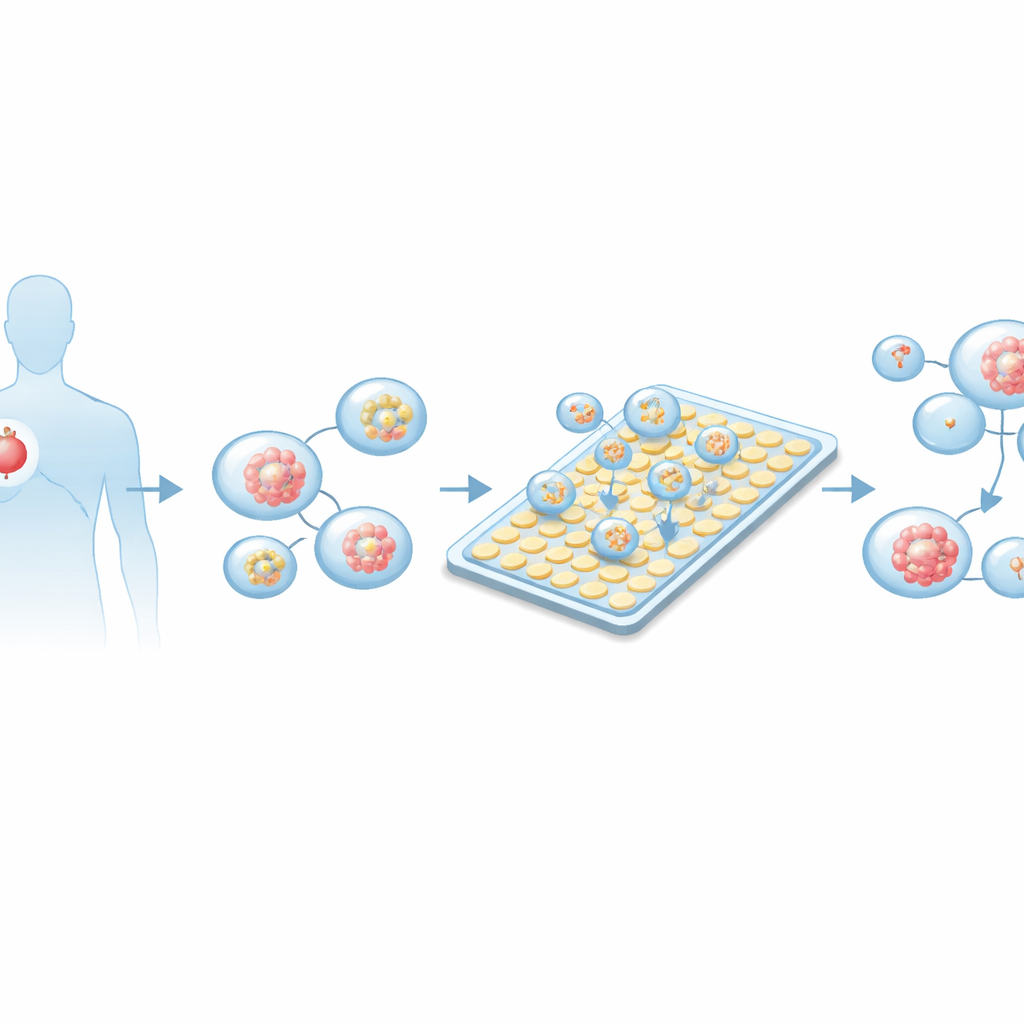
Dlaczego małe guzy mogą kierować dużymi decyzjami
Tradycyjne testy laboratoryjne leków przeciwnowotworowych zwykle opierają się na płaskich warstwach komórek hodowanych na plastikowych płytkach lub na modelach zwierzęcych. Podejścia te są powolne, wymagają wielu komórek i często nie odzwierciedlają zachowania prawdziwego guza ludzkiego. W ostatnich latach trójwymiarowe „organoidy” – drobne, kuliste skupiska komórek hodowane z guza pacjenta – pojawiły się jako wierniejsze zastępniki. Zachowują wiele cech pierwotnego nowotworu, w tym różnorodność genetyczną i strukturę, i często odzwierciedlają rzeczywistą odpowiedź pacjenta na leczenie. Jednak organoidy są cenne: próbki z biopsji dają ich niewiele, co utrudnia przeprowadzenie wielu testów lekowych metodami konwencjonalnymi, o dużych objętościach.
Inteligentny chip, który przesuwa krople jak piksele
Naukowcy rozwinęli technologię zwaną aktywną macierzową cyfrową mikroprzepływkowością. Zamiast przepychać ciecze wąskimi kanałami, system ten przesuwa maleńkie krople po płaskiej siatce elektrod, trochę jak przesuwanie pikseli na ekranie. Włączając i wyłączając elektrody, chip może generować, dzielić, przesuwać i mieszać krople o objętościach sięgających kilku nanolitrów – tysiące razy mniej niż typowy test laboratoryjny. Konstrukcja z aktywną macierzą wykorzystuje cienkowarstwowe tranzystory pod każdą elektrodą, dzięki czemu dużą liczbę „pikseli” można kontrolować przy relatywnie niewielkiej liczbie przewodów. Kompletny system dodaje precyzyjną kontrolę temperatury, elektronikę czasową i zintegrowane obrazowanie, pozwalając chipowi działać jako zautomatyzowana, samodzielna stacja eksperymentalna.
Hodowla guzów pacjentów i załadunek chipu
Aby przetestować platformę, zespół hodował organoidy z próbek gruczolakoraka płuca pobranych od kilku pacjentów. Tkankę guza delikatnie rozdzielono na pojedyncze komórki, osadzono w żelu wspierającym wzrost trójwymiarowy i inkubowano do momentu utworzenia się i dojrzenia małych struktur kulistych. Mikroskopia i barwienia fluorescencyjne potwierdziły, że organoidy te wykazywały markery zgodne z rakiem płuca i nie miały markerów innych typów nowotworów. Równolegle badacze zoptymalizowali, ile sferoidów nowotworowych powinno być zawieszonych w cieczy do załadunku na chip, tak aby większość generowanych kropli zawierała jeden do kilku organoidów o odpowiednim rozmiarze – na tyle duże, by być dojrzałe, ale nie tak duże, by ich centra stawały się niezdrowe.
Szybkie i precyzyjne testy lekowe
Gdy krople zawierające organoidy znalazły się na chipie, system automatycznie dzielił je i układał w regularne tablice. Dodatkowe krople zawierające pożywkę i powszechnie stosowany lek chemioterapeutyczny – cisplatynę – były generowane i łączone stopniowo, tworząc serię precyzyjnie kontrolowanych stężeń. Krople z organoidami następnie łączono z tymi zawierającymi lek i utrzymywano na chipie do trzech dni w temperaturze zbliżonej do ciała. Zintegrowany mikroskop rejestrował te same organoidy w czasie, ukazując wczesne kurczenie się przy wyższych dawkach już po 12 godzinach oraz bardziej nasilony rozpad struktury po 72 godzinach. Barwienia żywy/ martwy fluorescencyjne wykazały, że silniejsza ekspozycja na cisplatynę prowadziła do większego uszkodzenia komórek, widocznego jako wzrost sygnału czerwonego w stosunku do zielonego.
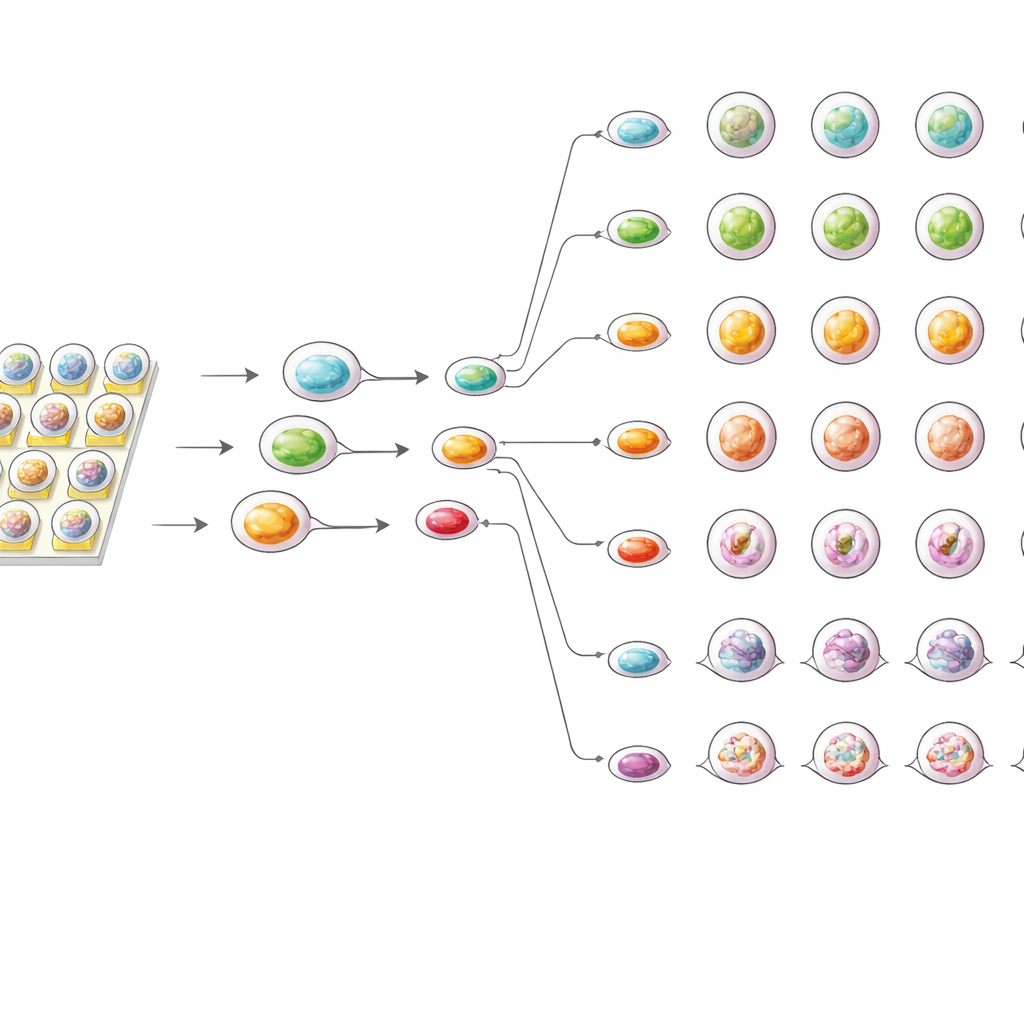
Większa czułość przy mniejszej próbce
Aby porównać chip ze standardowymi metodami, zespół przetestował te same organoidy także w konwencjonalnych płytkach 96-dołkowych. W obu ustawieniach efekty leku rosły wraz z dawką, a organoidy każdego pacjenta wykazywały charakterystyczny wzorzec odpowiedzi. Jednak testy na chipie konsekwentnie wykazywały nieco silniejsze hamowanie wzrostu organoidów i niższe wartości efektywnych dawek niż testy płytkowe. Autorzy sugerują, że środowisko mikrokropli pozwala cząsteczkom leku docierać do organoidów bardziej równomiernie i szybciej oraz zapobiega gromadzeniu się sygnałów przetrwania, które mogą występować w większych dołkach. Jednocześnie chip wymagał znacznie mniejszej liczby komórek i odczynników oraz dawał wysoce powtarzalne wyniki w kolejnych eksperymentach.
Od prototypu do spersonalizowanej opieki onkologicznej
Mówiąc prostymi słowami, praca ta pokazuje, że urządzenie wielkości dłoni może hodować miniaturowe wersje guza pacjenta i eksponować je na wiele dawek leku przeciwnowotworowego, zużywając przy tym jedynie niewielki skrawek tkanki. Obserwując, jak te mini‑guzy zmieniają kształt i czy pozostają żywe lub obumierają w czasie, platforma może dostarczyć szczegółowego, funkcjonalnego odczytu wrażliwości na lek, który uzupełnia badania genetyczne. Choć potrzebna jest dalsza walidacja z większą liczbą leków i dłuższym czasem hodowli, ten mikroprzepływowy chip z aktywną macierzą oferuje obiecującą drogę do szybszych, dokładniejszych i bardziej spersonalizowanych decyzji w leczeniu raka.
Cytowanie: Sun, R., Feng, Z., Wu, T. et al. Functional drug screening of tumor organoids on an active-matrix digital microfluidic chip for cancer precision medicine. Microsyst Nanoeng 12, 135 (2026). https://doi.org/10.1038/s41378-026-01215-2
Słowa kluczowe: precyzyjna medycyna onkologiczna, organoidy nowotworowe, chip mikroprzepływowy, testy wrażliwości na leki, gruczolakorak płuca