Clear Sky Science · zh
划分遗传性乳腺癌基因组不稳定性背后的异质性揭示四种疾病亚型
这项研究对家庭意味着什么
许多发生乳腺癌的女性有明显的家族病史,但在众所周知的BRCA1或BRCA2基因中找不到致病突变。临床上这些肿瘤常常表现不同,并且对治疗有特殊反应,但其原因一直不清晰。本研究采用全基因组分析表明,BRCA1/2阴性的遗传性乳腺癌并非单一实体,而可分为四个明确的遗传学群体,每一类都有各自的DNA损伤模式和潜在的治疗弱点。理解这些隐藏的差异有助于为患者及其家属更精准地制定治疗方案。
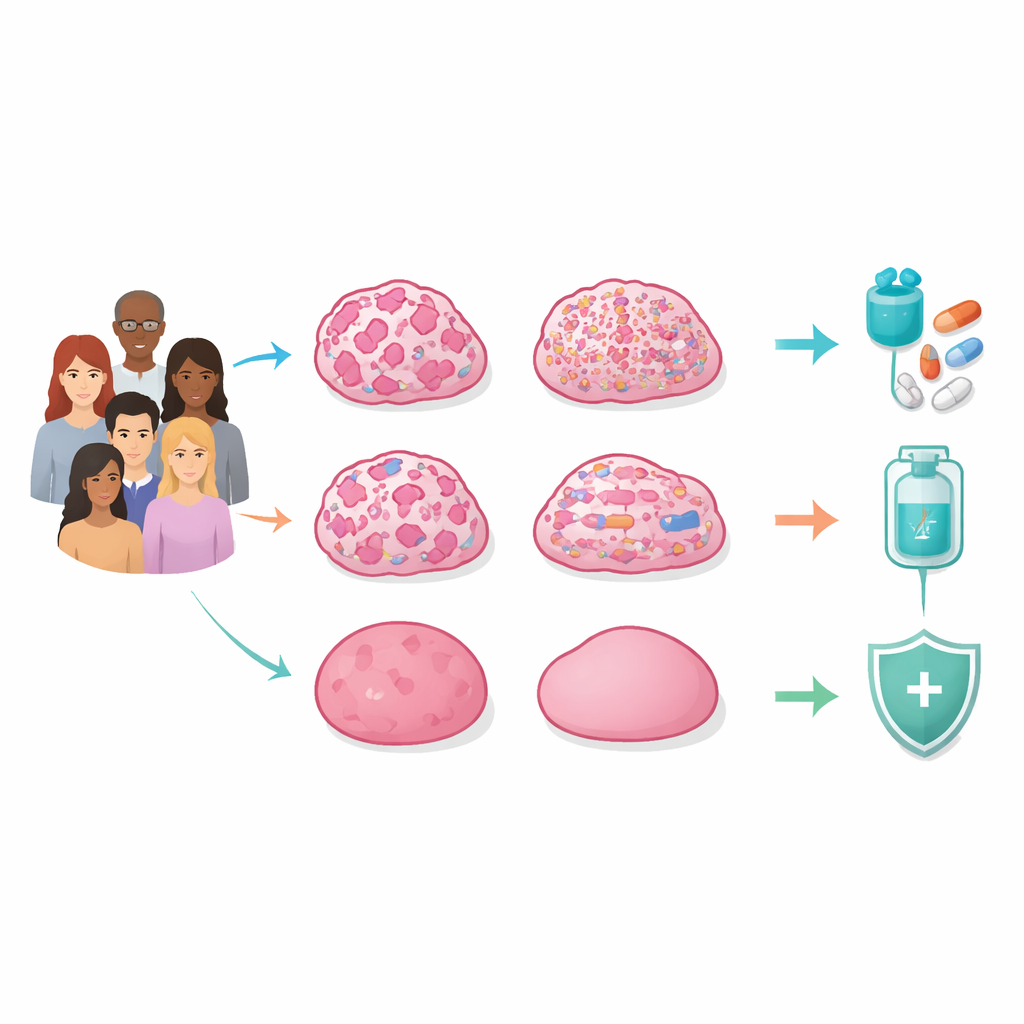
继承性肿瘤中的四种隐秘模式
研究者对129例被疑为遗传性乳腺癌且BRCA1/2无已知有害变异的韩国女性的肿瘤和正常组织进行了全基因组测序。他们不仅关注单个基因突变,还考察了染色体上的大尺度和小尺度断裂、缺失、扩增和重排,以及DNA化学标记和基因表达情况。通过整合这些层次的数据,研究发现区分肿瘤的核心特征并非单一基因,而是整体的基因组不稳定性模式——即DNA受损和紊乱的程度与方式。
DNA修复失败、突变风暴与平静基因组
第一大类被称为同源重组缺陷(HRD)亚型,显示出因关键DNA修复系统失效而产生的广泛“染色体瘢痕”。即便没有遗传性BRCA1/2突变,许多此类肿瘤通过丢失剩余拷贝或通过启动子过度甲基化沉默基因,从而丧失了BRCA功能。它们的染色体高度重排,常见灾难性片段化事件,并且经常伴有TP53突变。这类肿瘤多为三阴性乳腺癌且预后较差,但也对利用DNA修复弱点的药物(如PARP抑制剂)表现出特殊敏感性。
突变占优与拷贝数占优的癌症
第二类称为突变主导(MUT)亚型,其HRD评分相对较低,但点突变数异常增多。许多改变具有APOBEC酶的特征,能触发局部的“突变风暴”,称为kataegis。MUT肿瘤呈现强烈的免疫激活信号,包括杀伤性T细胞相关基因和促炎性巨噬细胞标志,提示它们可能是免疫疗法的良好候选者,尽管按常规检测很多会被归类为激素受体阳性。第三类为拷贝数占优(CN)亚型,表现为大量小片段的DNA缺失和扩增,但总体染色体拷贝数接近正常。这些局灶性改变常常删除经典的抑癌基因,并伴有激活的、富含成纤维细胞的肿瘤间质,提示可能对铂类或紫杉类化疗敏感,且可与靶向肿瘤支持组织的药物联合使用。
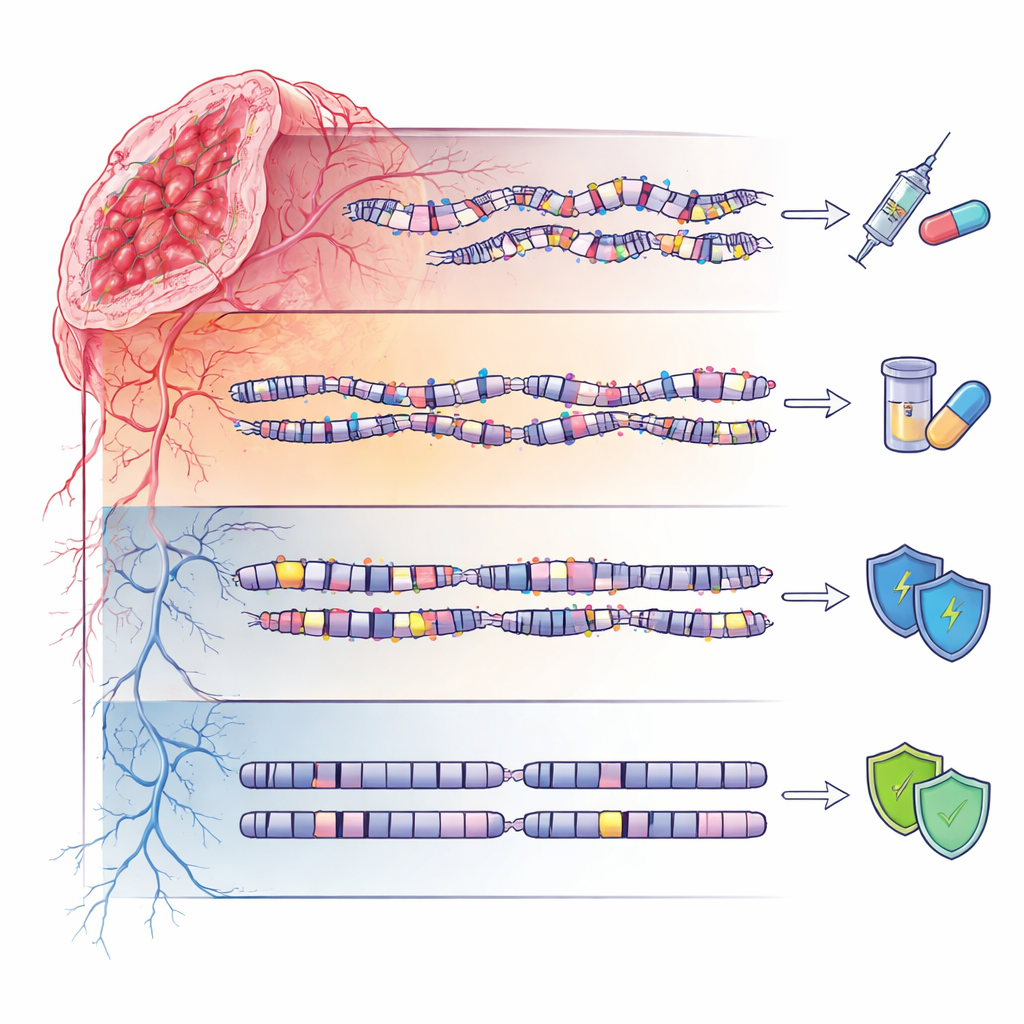
平静的基因组与遗传风险
第四类称为基因组稳定(GS),其DNA图谱相对平静,突变和大规模结构破坏较少。然而,这些患者并非没有遗传影响:他们富集若干与DNA修复相关的罕见胚系变异,许多仍被归类为“意义不确定的变异”。这表明在某些家族中,微妙的遗传变化可能在不引起明显基因组混乱的情况下增加患癌风险,强调了对遗传检测结果进行谨慎且考虑族群差异的解读,尤其是在非欧洲血统人群中。
对未来护理的意义
通过超越单基因检测和传统的表达型亚型,这项工作提出了一个“整合基因组不稳定性指数”,将修复缺陷、突变负荷、拷贝数变化和结构学特征结合起来,将遗传性乳腺癌划分为四种机制性群体。实践中,这支持将HRD肿瘤匹配到PARP抑制剂,将CN驱动的肿瘤匹配到特定化疗及间质靶向策略,将突变密集型肿瘤考虑免疫疗法,同时强调在基因组稳定病例中需要持续重新评估胚系变异。对患者和临床医生而言,该研究预示着一个未来:遗传性乳腺癌的治疗决策不再仅基于BRCA状态,而是基于更丰富的肿瘤DNA病变全貌。
引用: Kim, S., Lee, S., Kim, H. et al. Delineation of the heterogeneity underlying genomic instability in hereditary breast cancers reveals four disease subtypes. Exp Mol Med 58, 1254–1268 (2026). https://doi.org/10.1038/s12276-026-01693-4
关键词: 遗传性乳腺癌, 基因组不稳定性, BRCA阴性, 肿瘤亚型, 个体化治疗