Clear Sky Science · fr
Délimitation de l’hétérogénéité sous-jacente à l’instabilité génomique dans les cancers du sein héréditaires révèle quatre sous‑types de la maladie
Pourquoi cette recherche compte pour les familles
De nombreuses femmes qui développent un cancer du sein ont des antécédents familiaux marqués, sans pour autant porter de mutation dans les gènes bien connus BRCA1 ou BRCA2. Les cliniciens savent que ces tumeurs se comportent souvent différemment et peuvent répondre de façon particulière aux traitements, mais les raisons restaient floues. Cette étude utilise l’analyse du génome complet pour montrer que les cancers du sein héréditaires sans mutation BRCA1/2 ne constituent pas une seule entité : ils se répartissent en quatre groupes génétiques distincts, chacun avec son propre profil de lésions de l’ADN et ses vulnérabilités thérapeutiques potentielles. Comprendre ces différences cachées pourrait permettre d’adapter les traitements de façon beaucoup plus précise pour les patientes et leurs parentes.
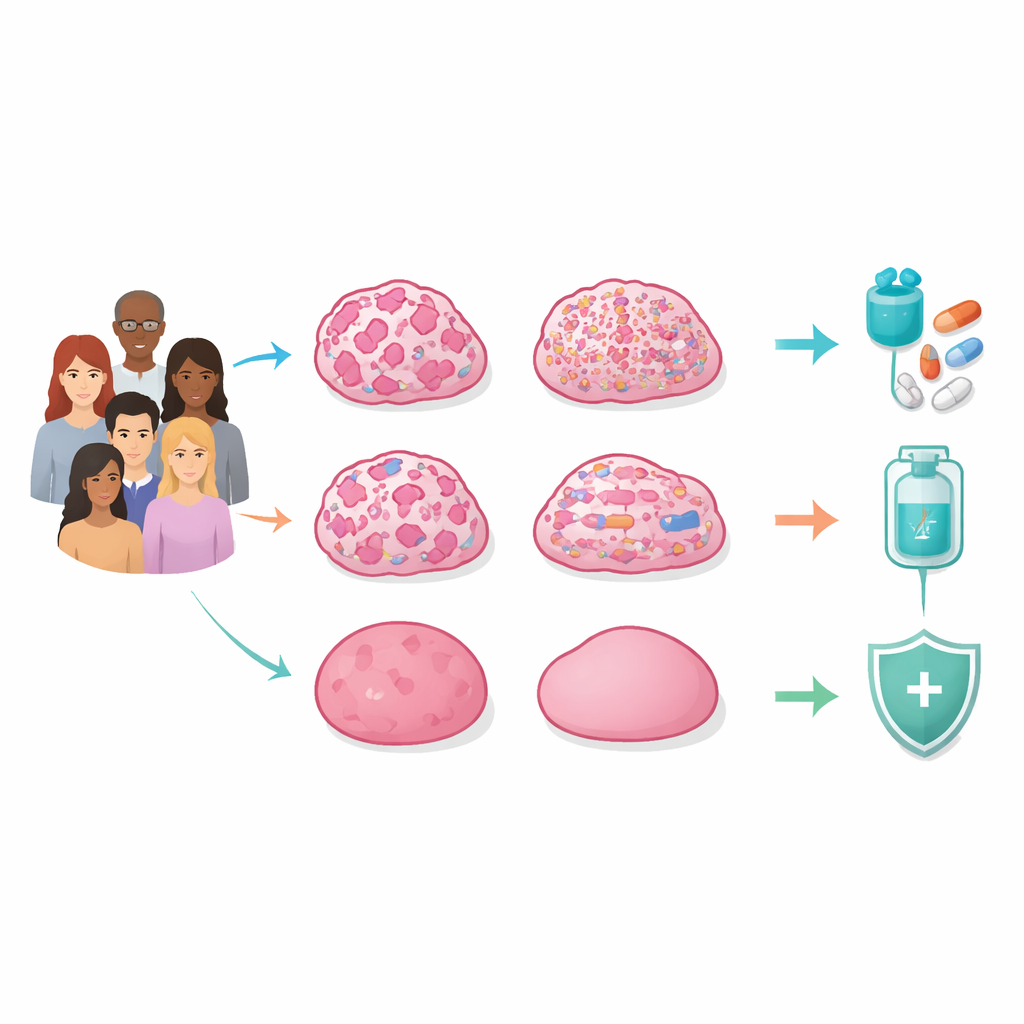
Quatre motifs cachés au sein des tumeurs héritées
Les chercheuses et chercheurs ont séquencé le génome entier des tumeurs et des tissus normaux de 129 femmes coréennes suspectes de cancer du sein héréditaire et testées négatives pour des variantes délétères de BRCA1/2. Ils n’ont pas regardé seulement les mutations d’un gène isolé, mais aussi les ruptures, pertes, gains et réarrangements à différentes échelles chromosomiques, ainsi que les marques chimiques sur l’ADN et l’activité génique. En intégrant tous ces niveaux, ils ont découvert que la caractéristique centrale qui distingue les tumeurs n’est pas un gène unique, mais le patron global d’instabilité génomique — le degré de dommage et de désordre subi par l’ADN.
Défaillance de la réparation de l’ADN, tempêtes de mutations et génomes calmes
Un groupe majeur, qualifié de sous‑type déficient en recombinaison homologue (HRD), présentait de larges « cicatrices chromosomiques » causées par l’échec d’un système clé de réparation de l’ADN. Même en l’absence de mutations héréditaires BRCA1/2, nombre de ces tumeurs avaient perdu la fonction BRCA via la perte de l’allèle restant ou la mise sous silence du promoteur par hyperméthylation. Leurs chromosomes étaient fortement réarrangés, souvent à la suite d’événements catastrophiques de fragmentation, et portaient fréquemment des mutations de TP53. Ces tumeurs avaient tendance à être des cancers triple négatifs et à présenter un pronostic moins favorable, mais elles semblaient aussi particulièrement vulnérables à des médicaments exploitant la faiblesse de la réparation de l’ADN, comme les inhibiteurs de PARP.
Cancers riches en mutations et cancers dominés par le nombre de copies
Un deuxième groupe, le sous‑type à dominance mutationnelle (MUT), présentait des scores HRD relativement faibles mais un nombre exceptionnellement élevé de mutations ponctuelles. Beaucoup de ces altérations portaient la signature des enzymes APOBEC, capables de déclencher des « tempêtes » locales de mutations appelées kataegis. Les tumeurs MUT montraient de forts signaux d’activation immunitaire, y compris des gènes utilisés par les lymphocytes T cytotoxiques et des marqueurs de macrophages pro‑inflammatoires, ce qui suggère qu’elles pourraient être de bons candidats à l’immunothérapie, même si beaucoup seraient classées comme hormono‑réceptrices positives selon les tests standards. Un troisième groupe, le sous‑type à dominance des variations du nombre de copies (CN), accumulait en revanche de nombreuses petites pertes et gains d’ADN tout en conservant un nombre chromosomique global proche de la normale. Ces altérations focales supprimaient souvent des gènes suppresseurs de tumeur classiques et s’accompagnaient d’un stroma tumoral activé, riche en fibroblastes, laissant entrevoir une sensibilité possible aux chimiothérapies à base de platine ou de taxanes, potentiellement en combinaison avec des médicaments ciblant le tissu de soutien.
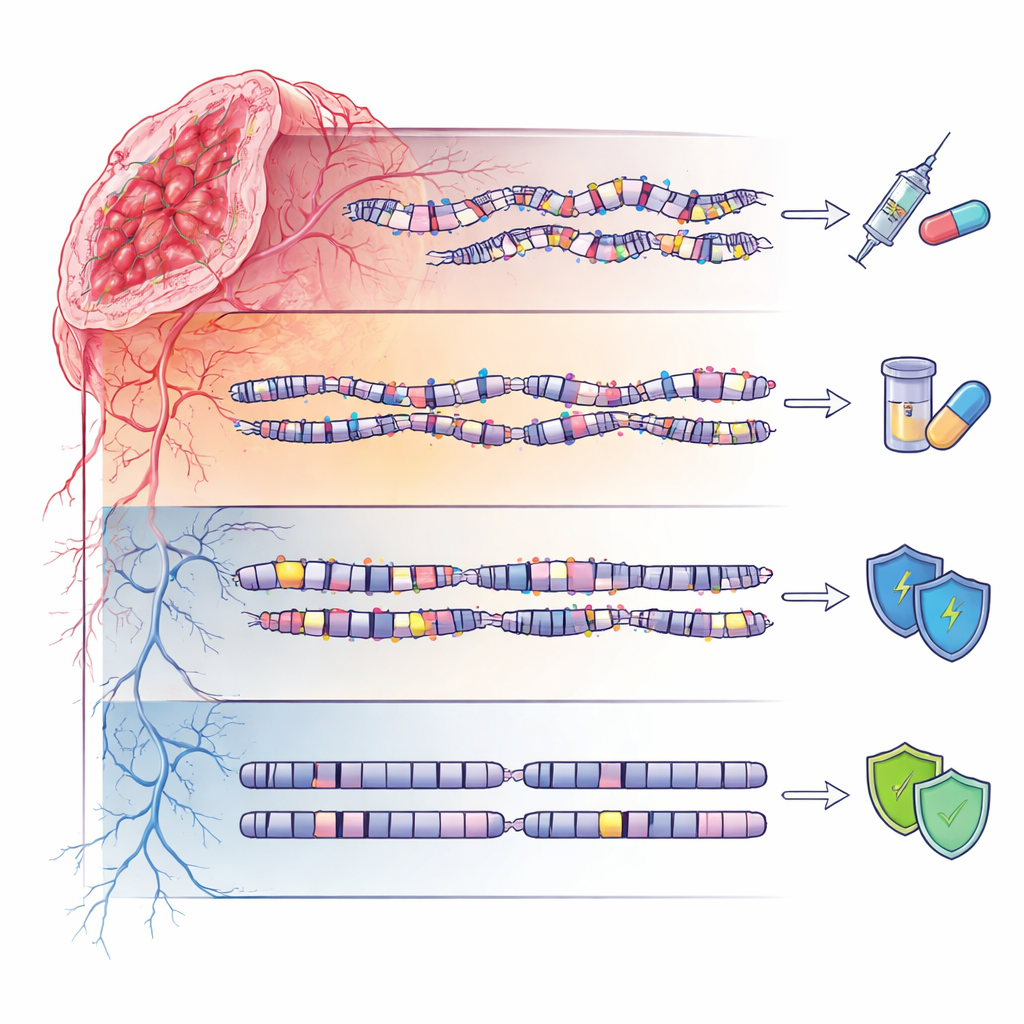
Génomes calmes et risque hérité
Le quatrième groupe, qualifié de stable du génome (GS), présentait des paysages d’ADN relativement calmes, avec peu de mutations ou de perturbations à grande échelle. Pour autant, ces patientes n’étaient pas exemptes d’influences héréditaires : elles étaient enrichies en variantes germinales rares dans plusieurs gènes liés à la réparation de l’ADN, dont beaucoup restent classées comme « variantes de signification incertaine ». Cela suggère que, dans certaines familles, des modifications héritées subtiles peuvent prédisposer au cancer sans provoquer un chaos génomique spectaculaire, soulignant la nécessité d’une interprétation attentive et adaptée à l’origine ancestrale des résultats des tests génétiques, en particulier dans les populations non européennes.
Ce que cela signifie pour la prise en charge future
En dépassant les tests mono‑gène et les sous‑types traditionnels basés sur l’expression, ce travail propose un « indice intégratif d’instabilité génomique » qui combine défauts de réparation, charge mutée, variations du nombre de copies et signatures structurelles pour classer les cancers du sein héréditaires en quatre groupes mécanistiques. Concrètement, cela soutient l’appariement des tumeurs HRD aux inhibiteurs de PARP, des tumeurs CN à des chimiothérapies spécifiques et à des stratégies ciblant le stroma, et des tumeurs riches en mutations à l’immunothérapie, tout en soulignant la nécessité de réévaluations continues des variantes germinales dans les cas genome‑stable. Pour les patientes et les cliniciens, l’étude ouvre la voie à un avenir où la prise en charge du cancer du sein héréditaire serait guidée non seulement par le statut BRCA, mais par une description plus complète de la façon dont l’ADN de chaque tumeur s’est altéré.
Citation: Kim, S., Lee, S., Kim, H. et al. Delineation of the heterogeneity underlying genomic instability in hereditary breast cancers reveals four disease subtypes. Exp Mol Med 58, 1254–1268 (2026). https://doi.org/10.1038/s12276-026-01693-4
Mots-clés: cancer du sein héréditaire, instabilité génomique, BRCA‑négatif, sous‑types tumoraux, thérapie personnalisée