Clear Sky Science · de
Aufschlüsselung der Heterogenität der genomischen Instabilität bei erblichen Brustkrebserkrankungen zeigt vier Erkrankungs‑Subtypen
Warum diese Forschung für Familien wichtig ist
Viele Frauen, bei denen Brustkrebs auftritt, haben eine starke Familienvorgeschichte der Erkrankung, tragen aber keine Mutation in den bekannten BRCA1‑ oder BRCA2‑Genen. Ärztinnen und Ärzte wissen, dass sich diese Tumoren oft anders verhalten und auf gewisse Behandlungen speziell reagieren können, doch die Ursachen waren bislang unklar. Diese Studie verwendet komplette Genomanalysen und zeigt, dass erbliche Brustkrebserkrankungen ohne BRCA1/2‑Mutationen keine einheitliche Entität darstellen, sondern in vier klare genetische Gruppen fallen — jeweils mit eigenem Muster von DNA‑Schäden und möglichen therapeutischen Verwundbarkeiten. Das Verständnis dieser verborgenen Unterschiede könnte helfen, Therapien für Patientinnen und ihre Angehörigen deutlich präziser zuzuschneiden.
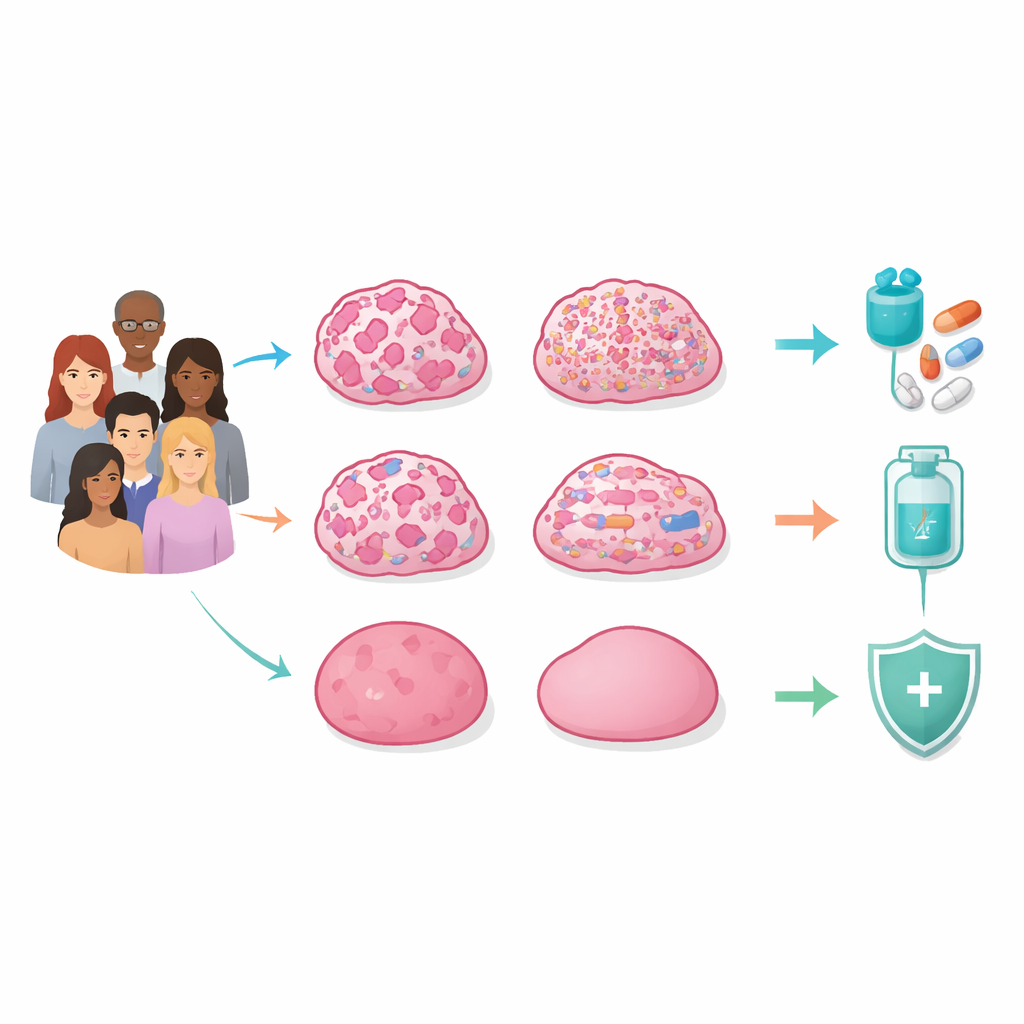
Vier verborgene Muster in ererbten Tumoren
Die Forschenden sequenzierten die kompletten Genome von Tumoren und normalem Gewebe von 129 koreanischen Frauen mit Verdacht auf erblichen Brustkrebs, die auf schädliche BRCA1/2‑Varianten negativ getestet hatten. Sie betrachteten nicht nur einzelne Genmutationen, sondern auch große und kleine Brüche, Verluste, Duplikationen und Umordnungen über die Chromosomen hinweg sowie chemische Markierungen auf der DNA und Genaktivität. Durch die Integration all dieser Ebenen fanden sie heraus, dass das zentrale Unterscheidungsmerkmal der Tumoren nicht ein einzelnes Gen war, sondern das Gesamtmuster der genomischen Instabilität — wie stark die DNA beschädigt und ungeordnet war.
Versagen der DNA‑Reparatur, Mutationsstürme und ruhige Genome
Eine große Gruppe, bezeichnet als homologe Rekombinations‑defizient (HRD) Subtyp, zeigte weitverbreitete „chromosomale Narben“, verursacht durch das Versagen eines zentralen DNA‑Reparatursystems. Selbst ohne vererbte BRCA1/2‑Mutationen hatten viele dieser Tumoren BRCA‑Funktion verloren, etwa durch Verlust der verbleibenden Kopie oder durch Stilllegung des Promotors durch erhöhte Methylierung. Ihre Chromosomen waren stark umgeordnet, oft mit katastrophalen Zerstörungsereignissen, und trugen häufig TP53‑Mutationen. Diese Tumoren neigten dazu, triple‑negative Brustkrebse zu sein und eine schlechtere Überlebensprognose zu haben, zeigten aber zugleich eine besondere Verwundbarkeit gegenüber Arzneimitteln, die Reparaturschwächen ausnutzen, wie PARP‑Inhibitoren.
Mutationsreiche und kopienzahl‑dominante Krebsformen
Eine zweite Gruppe, der mutationsdominante (MUT) Subtyp, wies vergleichsweise niedrige HRD‑Werte auf, trug jedoch ungewöhnlich viele Punktmutationen. Viele dieser Veränderungen trugen die Signatur von APOBEC‑Enzymen, die lokale „Stürme“ von Mutationen auslösen können, bekannt als Kataegis. MUT‑Tumoren zeigten starke Hinweise auf Immunaktivierung, einschließlich Genen, die von Killer‑T‑Zellen verwendet werden, sowie Markern proinflammatorischer Makrophagen, was darauf hindeutet, dass sie besonders gute Kandidaten für Immuntherapien sein könnten — obwohl viele nach Standardtests als Hormonrezeptor‑positiv klassifiziert würden. Ein dritter Typ, der kopienzahl‑dominante (CN) Subtyp, sammelte stattdessen zahlreiche kleine DNA‑Verluste und ‑Gewinne an, während die Gesamtzahl der Chromosomen annähernd normal blieb. Diese fokalen Veränderungen entfernten häufig klassische Tumorsuppressorgene und gingen mit einem aktivierten, fibroblastenreichen Tumorstroma einher, was auf Empfindlichkeit gegenüber Platin‑ oder Taxan‑Chemotherapien hinweist, möglicherweise in Kombination mit Wirkstoffen, die das Stützgewebe anvisieren.
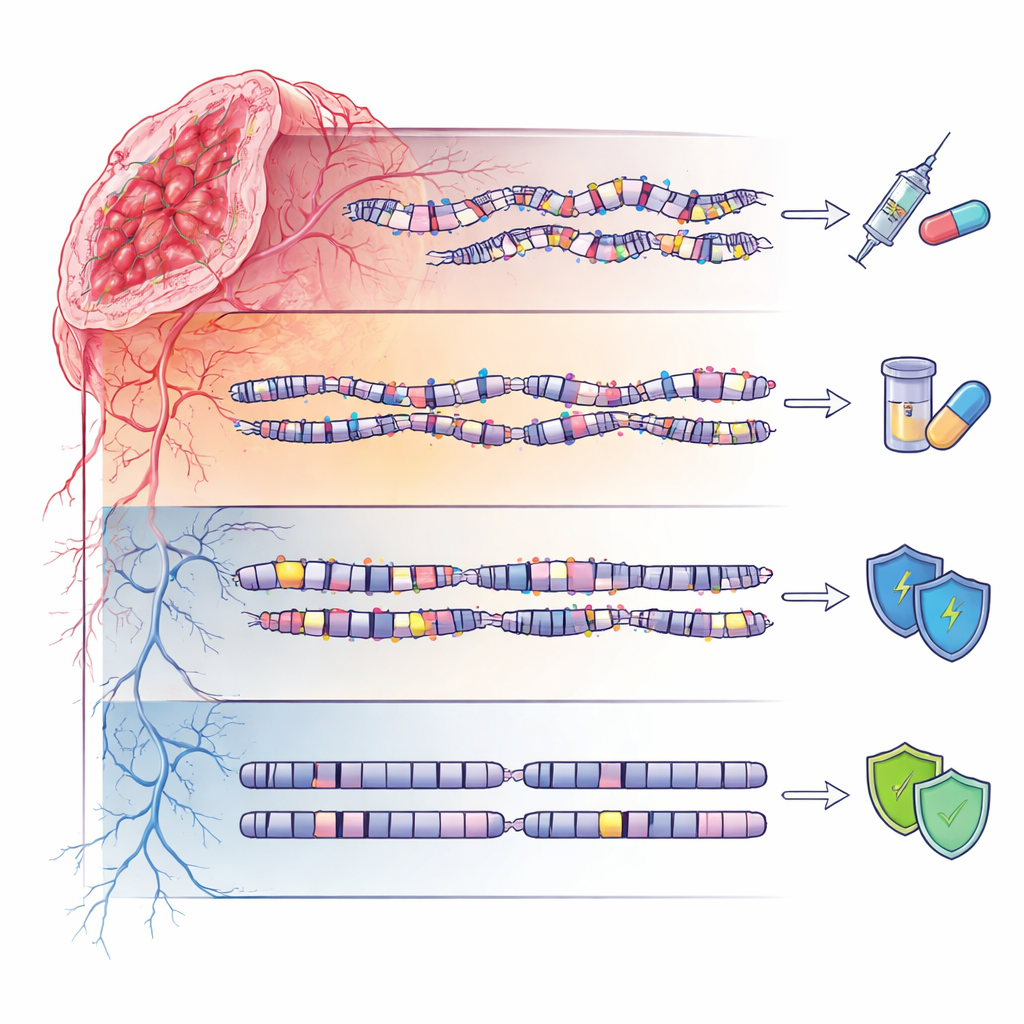
Ruhige Genome und vererbtes Risiko
Die vierte Gruppe, bezeichnet als genom‑stabil (GS), zeigte relativ ruhige DNA‑Landschaften mit wenigen Mutationen oder großskaligen Störungen. Dennoch waren diese Patientinnen nicht frei von erblichen Einflüssen: Sie wiesen eine Anreicherung seltener Keimbahnvarianten in mehreren DNA‑Reparatur‑bezogenen Genen auf, von denen viele noch als „Varianten von unklarer Bedeutung“ klassifiziert sind. Das deutet darauf hin, dass in einigen Familien subtile vererbte Veränderungen ein Krebsrisiko erhöhen können, ohne dramatisches genomisches Chaos zu erzeugen, und unterstreicht die Notwendigkeit einer sorgfältigen, auf die Abstammung abgestimmten Interpretation genetischer Testergebnisse, insbesondere in nicht‑europäischen Populationen.
Was das für die künftige Versorgung bedeutet
Indem die Studie über Einzelgen‑Tests und traditionelle expressionsbasierte Subtypen hinausgeht, schlägt sie einen „integrativen Index der genomischen Instabilität“ vor, der Reparaturdefekte, Mutationslast, Kopienzahlanomalien und strukturelle Signaturen kombiniert, um erbliche Brustkrebserkrankungen in vier mechanistische Gruppen einzuordnen. Praktisch bedeutet das: HRD‑Tumoren mit PARP‑Inhibitoren zu matchen, CN‑getriebene Tumoren mit bestimmten Chemotherapien und stroma‑gerichteten Strategien zu behandeln und mutationsreiche Tumoren für Immuntherapien in Betracht zu ziehen — gleichzeitig aber die fortlaufende Neubewertung von Keimbahnvarianten in genom‑stabilen Fällen zu betonen. Für Patientinnen und Klinikteams weist die Studie auf eine Zukunft hin, in der die Versorgung bei erblich bedingtem Brustkrebs nicht allein vom BRCA‑Status abhängt, sondern von einem umfassenderen Bild darüber, wie die DNA jedes Tumors fehlgeht.
Zitation: Kim, S., Lee, S., Kim, H. et al. Delineation of the heterogeneity underlying genomic instability in hereditary breast cancers reveals four disease subtypes. Exp Mol Med 58, 1254–1268 (2026). https://doi.org/10.1038/s12276-026-01693-4
Schlüsselwörter: erblicher Brustkrebs, genomische Instabilität, BRCA‑negativ, Tumor‑Subtypen, personalisierte Therapie