Clear Sky Science · pt
Delineamento da heterogeneidade subjacente à instabilidade genômica em cânceres hereditários de mama revela quatro subtipos da doença
Por que esta pesquisa importa para famílias
Muitas mulheres que desenvolvem câncer de mama têm forte histórico familiar da doença, mas não apresentam mutação nos conhecidos genes BRCA1 ou BRCA2. Os médicos sabem que esses tumores frequentemente se comportam de forma diferente e podem responder de modos específicos ao tratamento, mas as razões eram pouco claras. Este estudo utiliza análise do genoma completo para mostrar que os cânceres hereditários de mama sem mutações em BRCA1/2 não constituem uma única entidade, mas se dividem em quatro grupos genéticos bem definidos, cada um com seu padrão de dano ao DNA e potenciais vulnerabilidades terapêuticas. Compreender essas diferenças ocultas pode ajudar a adaptar terapias de maneira muito mais precisa para pacientes e seus familiares.
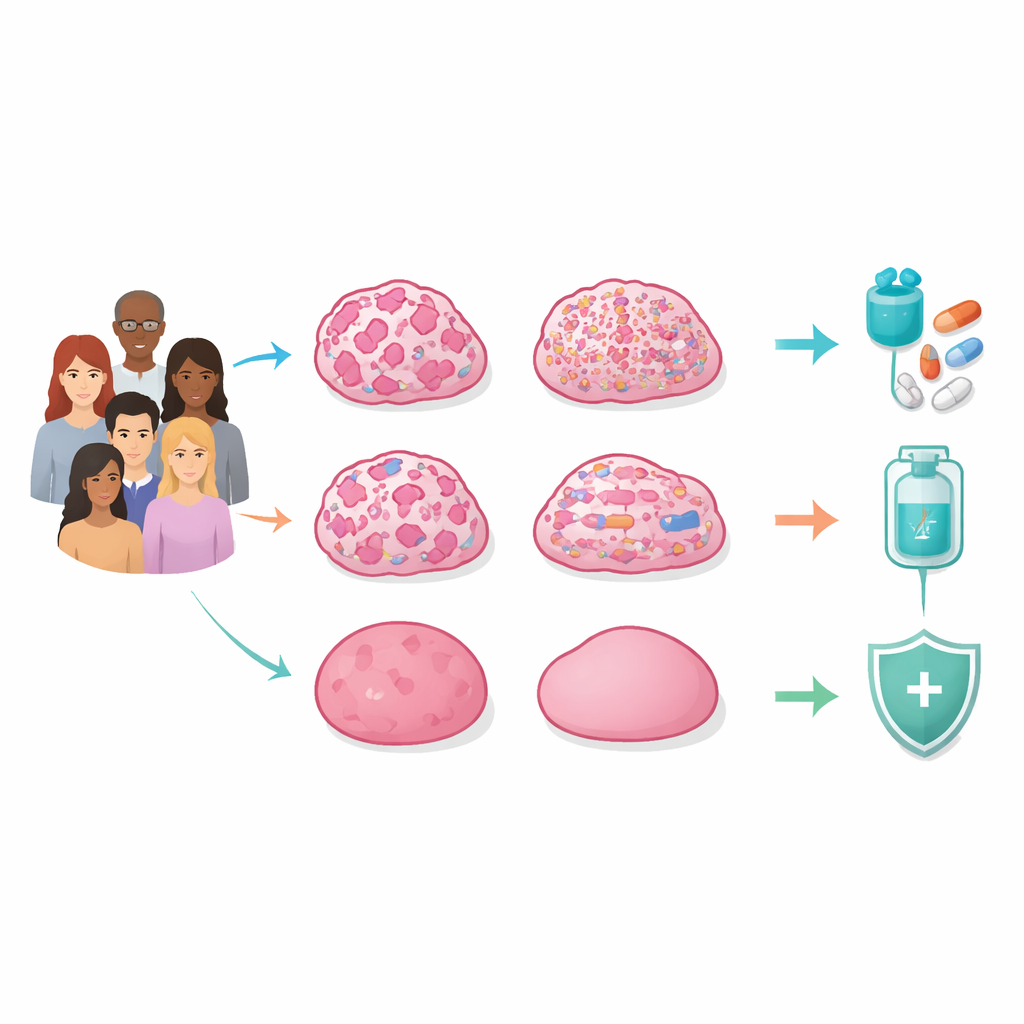
Quatro padrões ocultos dentro de tumores hereditários
Os pesquisadores sequenciaram os genomas inteiros de tumores e tecido normal de 129 mulheres coreanas com suspeita de câncer de mama hereditário que testaram negativo para variantes deletérias em BRCA1/2. Eles analisaram não apenas mutações em genes individuais, mas também quebras grandes e pequenas, perdas, ganhos e rearranjos ao longo dos cromossomos, além de marcas químicas no DNA e atividade gênica. Ao integrar todas essas camadas, descobriram que a característica central que distingue os tumores não é um único gene, mas o padrão geral de instabilidade genômica — quão danificado e desordenado o DNA se tornou.
Falha na reparação do DNA, tempestades de mutação e genomas silenciosos
Um grupo majoritário, chamado subtipo com deficiência de recombinação homóloga (HRD), apresentou amplas “cicatrizes cromossômicas” causadas pela falha de um sistema chave de reparo do DNA. Mesmo sem mutações herdadas em BRCA1/2, muitos desses tumores perderam a função BRCA pela perda da cópia remanescente ou pela silenciação do promotor do gene por metilação adicional. Seus cromossomos estavam fortemente rearranjados, frequentemente com eventos catastróficos de fragmentação, e carregavam mutações em TP53 com frequência. Esses tumores tendiam a ser cânceres de mama triplo-negativos e apresentar pior sobrevida, mas também pareciam especialmente vulneráveis a fármacos que exploram a fraqueza na reparação do DNA, como os inibidores de PARP.
Cânceres com alta carga de mutações e com predomínio de número de cópias
Um segundo grupo, o subtipo dominante em mutações (MUT), apresentou escores de HRD comparativamente baixos, mas carregava um número incomumente alto de mutações pontuais. Muitas dessas alterações mostraram a assinatura das enzimas APOBEC, que podem provocar “tempestades” locais de mutações conhecidas como kataegis. Tumores MUT exibiram fortes sinais de ativação imune, incluindo genes usados por células T citotóxicas e marcadores de macrófagos pró-inflamatórios, sugerindo que podem ser particularmente bons candidatos para imunoterapia, mesmo que muitos sejam classificados como receptor-hormonal-positivos por testes padrão. Um terceiro grupo, o subtipo dominante em número de cópias (CN), acumulou muitas pequenas perdas e ganhos de DNA enquanto mantinha uma contagem cromossômica global próxima do normal. Essas alterações focais frequentemente removiam genes supressores tumorais clássicos e eram acompanhadas por um estroma tumoral ativado e rico em fibroblastos, indicando sensibilidade potencial a quimioterapias à base de platina ou taxanos, possivelmente em combinação com drogas que miram o tecido de suporte.
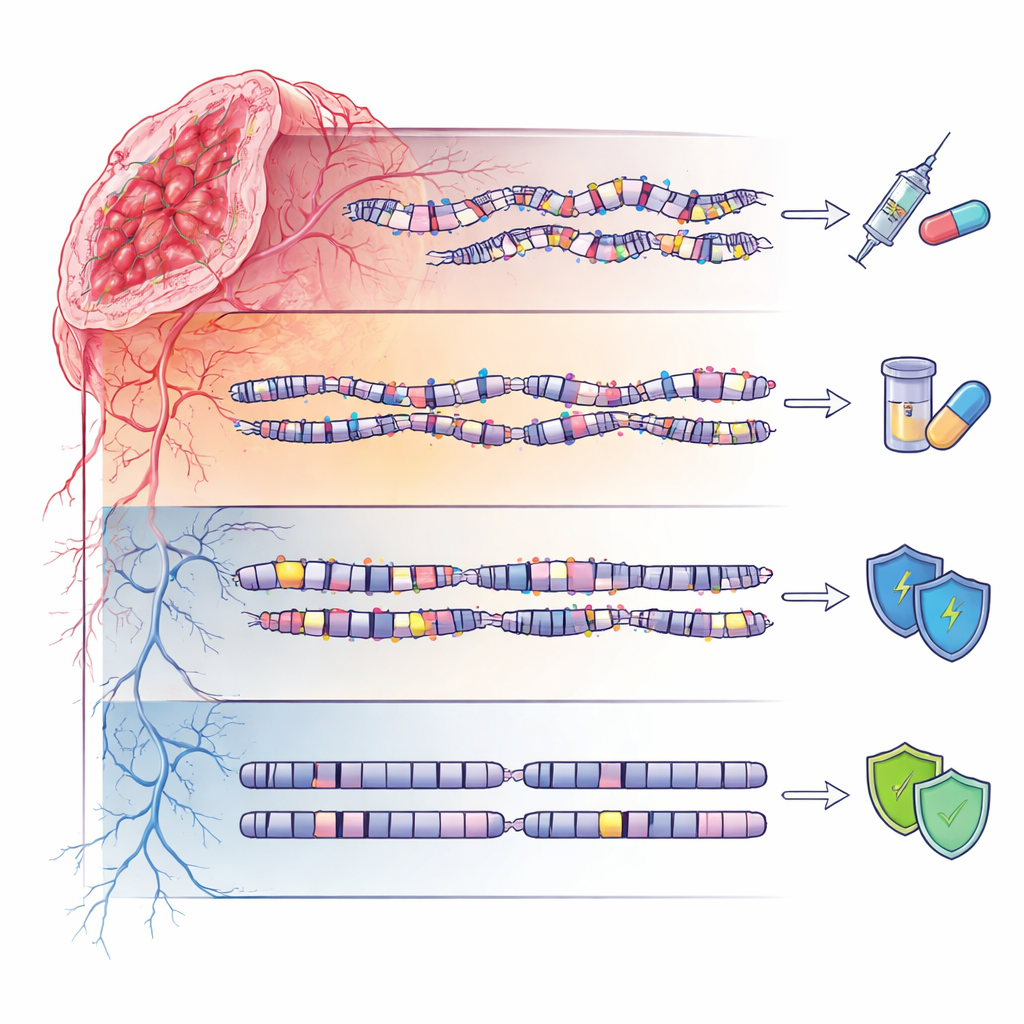
Genomas silenciosos e risco herdado
O quarto grupo, denominado estável-genômico (GS), mostrou paisagens de DNA relativamente calmas, com poucas mutações ou perturbações em grande escala. Ainda assim, essas pacientes não estavam livres de influências herdadas: houve enriquecimento por variantes germinativas raras em vários genes relacionados à reparação do DNA, muitas das quais ainda são classificadas como “variantes de significado incerto”. Isso sugere que, em algumas famílias, mudanças herdadas sutis podem predispor ao câncer sem produzir caos genômico dramático, enfatizando a necessidade de interpretação cuidadosa e sensível à ancestralidade dos resultados de testes genéticos, especialmente em populações não europeias.
O que isso significa para o cuidado futuro
Ao ir além de testes de gene único e subtipos tradicionais baseados em expressão, este trabalho propõe um “índice integrativo de instabilidade genômica” que combina defeitos de reparo, carga de mutações, alterações no número de cópias e assinaturas estruturais para classificar cânceres hereditários de mama em quatro grupos mecanísticos. Em termos práticos, apoia o direcionamento de tumores HRD para inibidores de PARP, tumores dirigidos por CN para quimioterapias específicas e estratégias que atinjam o estroma, e tumores com alta carga de mutação para imunoterapia, ao mesmo tempo que ressalta a necessidade de reavaliação contínua de variantes germinativas nos casos estáveis-genômicos. Para pacientes e clínicos, o estudo aponta para um futuro em que o cuidado do câncer de mama hereditário é orientado não apenas pelo status BRCA, mas por uma imagem mais rica de como o DNA de cada tumor foi comprometido.
Citação: Kim, S., Lee, S., Kim, H. et al. Delineation of the heterogeneity underlying genomic instability in hereditary breast cancers reveals four disease subtypes. Exp Mol Med 58, 1254–1268 (2026). https://doi.org/10.1038/s12276-026-01693-4
Palavras-chave: câncer de mama hereditário, instabilidade genômica, BRCA-negativo, subtipos tumorais, terapia personalizada