Clear Sky Science · es
Delimitación de la heterogeneidad subyacente a la inestabilidad genómica en cánceres de mama hereditarios revela cuatro subtipos de la enfermedad
Por qué esta investigación importa para las familias
Muchas mujeres que desarrollan cáncer de mama tienen una fuerte historia familiar de la enfermedad pero no presentan mutaciones en los conocidos genes BRCA1 o BRCA2. Los médicos saben que estos tumores suelen comportarse de forma diferente y pueden responder de manera particular a ciertos tratamientos, pero las razones no estaban claras. Este estudio utiliza análisis del genoma completo para mostrar que los cánceres de mama hereditarios sin mutaciones en BRCA1/2 no constituyen una sola entidad, sino que se agrupan en cuatro grupos genéticos bien diferenciados, cada uno con su propio patrón de daño en el ADN y posibles vulnerabilidades terapéuticas. Comprender estas diferencias ocultas podría ayudar a adaptar las terapias con mucha más precisión para pacientes y sus familiares.
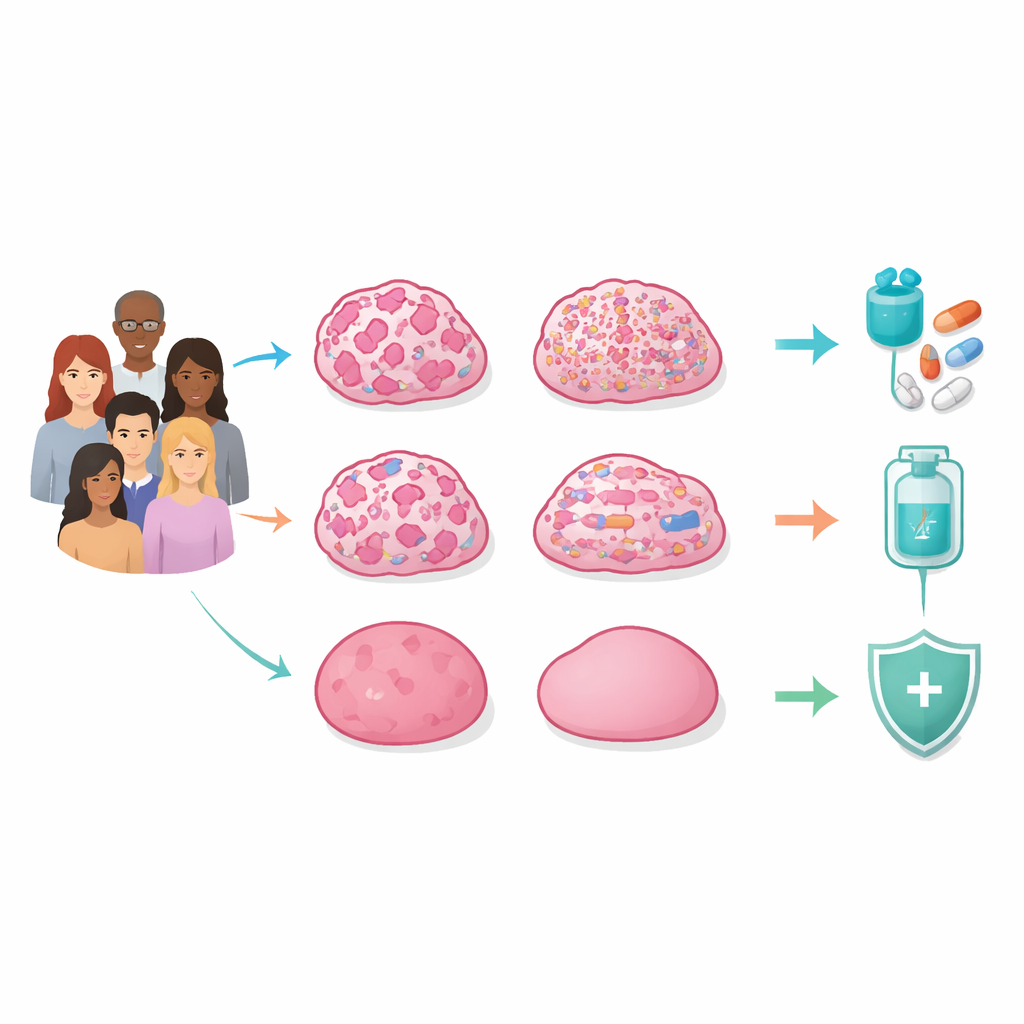
Cuatro patrones ocultos dentro de los tumores heredados
Los investigadores secuenciaron los genomas completos de tumores y tejido normal de 129 mujeres coreanas con sospecha de cáncer de mama hereditario que dieron negativo en pruebas de variantes dañinas en BRCA1/2. No se limitaron a buscar mutaciones en genes individuales, sino también grandes y pequeños roturas, pérdidas, ganancias y reordenamientos en los cromosomas, así como marcas químicas sobre el ADN y la actividad génica. Al integrar todas estas capas, encontraron que la característica central que distinguía a los tumores no era un único gen, sino el patrón global de inestabilidad genómica: hasta qué punto el ADN estaba dañado y desordenado.
Fallo en la reparación del ADN, tormentas de mutaciones y genomas tranquilos
Un grupo principal, denominado subtipo deficiente en recombinación homóloga (HRD), mostró extensas “cicatrices cromosómicas” causadas por el fallo de un sistema clave de reparación del ADN. Incluso sin mutaciones heredadas en BRCA1/2, muchos de estos tumores habían perdido la función de BRCA mediante la pérdida de la copia restante o por silenciamiento del promotor del gen mediante metilación adicional. Sus cromosomas estaban muy reordenados, a menudo con eventos catastróficos de fragmentación, y con frecuencia presentaban mutaciones en TP53. Estos tumores tendían a ser cánceres de mama triple negativos y a asociarse con peor supervivencia, pero también parecían especialmente vulnerables a fármacos que explotan la debilidad en la reparación del ADN, como los inhibidores de PARP.
Cánceres dominados por mutaciones y por cambios en el número de copias
Un segundo grupo, el subtipo dominante en mutaciones (MUT), tenía puntuaciones HRD comparativamente bajas pero presentaba un número inusualmente alto de mutaciones puntuales. Muchas de estas alteraciones mostraban la huella de las enzimas APOBEC, que pueden provocar “tormentas” locales de mutaciones conocidas como kataegis. Los tumores MUT mostraron señales sólidas de activación inmune, incluyendo genes empleados por linfocitos T citotóxicos y marcadores de macrófagos proinflamatorios, lo que sugiere que podrían ser candidatos especialmente adecuados para la inmunoterapia, aun cuando muchos se clasificarían como positivos para receptores hormonales según las pruebas estándar. Un tercer grupo, el subtipo dominante en número de copias (CN), en cambio acumuló muchas pérdidas y ganancias de ADN focales manteniendo un recuento cromosómico global cercano a la normalidad. Estos cambios focales a menudo eliminaban genes supresores clásicos y se acompañaban de un estroma tumoral activado y rico en fibroblastos, lo que apunta a una posible sensibilidad a quimioterapias con platino o taxanos, potencialmente en combinación con fármacos dirigidos al tejido de sostén.
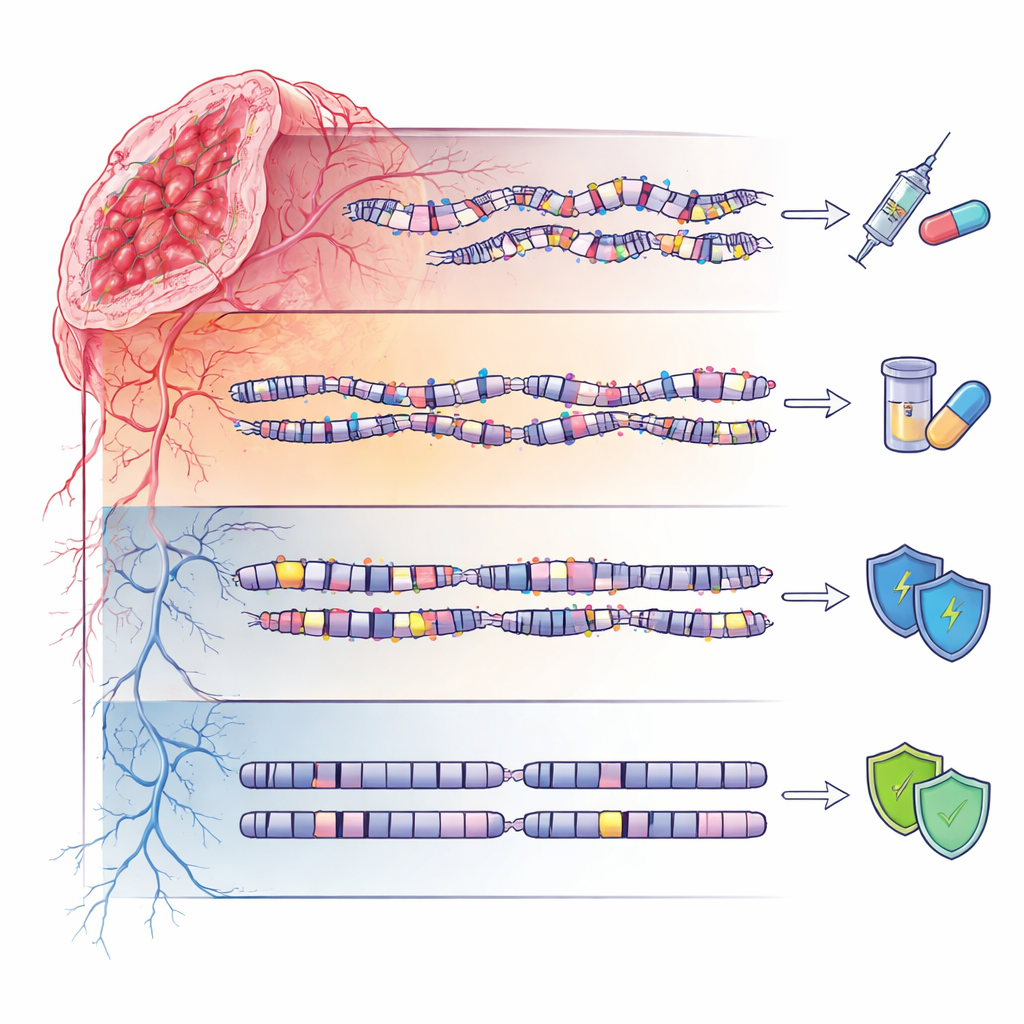
Genomas tranquilos y riesgo heredado
El cuarto grupo, denominado genoma‑estable (GS), mostró paisajes de ADN relativamente tranquilos, con pocas mutaciones o alteraciones a gran escala. Aun así, estas pacientes no estaban exentas de influencias hereditarias: presentaban una mayor frecuencia de variantes germinales raras en varios genes relacionados con la reparación del ADN, muchas de las cuales aún se clasifican como “variantes de significado incierto”. Esto sugiere que en algunas familias cambios hereditarios sutiles pueden predisponer al cáncer sin producir un caos genómico dramático, subrayando la necesidad de interpretar con cuidado y con atención al origen ancestral los resultados de las pruebas genéticas, especialmente en poblaciones no europeas.
Qué significa esto para la atención futura
Al ir más allá de las pruebas de un solo gen y de los subtipos tradicionales basados en la expresión, este trabajo propone un “índice integrador de inestabilidad genómica” que combina defectos de reparación, carga de mutaciones, cambios en el número de copias y firmas estructurales para situar los cánceres de mama hereditarios en cuatro grupos mecanísticos. En términos prácticos, respalda emparejar tumores HRD con inhibidores de PARP, tumores impulsados por CN con quimioterapias específicas y estrategias dirigidas al estroma, y tumores ricos en mutaciones con inmunoterapia, al tiempo que destaca la necesidad de reevaluación continua de las variantes germinales en los casos genoma‑estables. Para pacientes y clínicos, el estudio apunta a un futuro en el que la atención del cáncer de mama hereditario se oriente no solo por el estado BRCA, sino por una imagen más rica de cómo ha fallado el ADN de cada tumor.
Cita: Kim, S., Lee, S., Kim, H. et al. Delineation of the heterogeneity underlying genomic instability in hereditary breast cancers reveals four disease subtypes. Exp Mol Med 58, 1254–1268 (2026). https://doi.org/10.1038/s12276-026-01693-4
Palabras clave: cáncer de mama hereditario, inestabilidad genómica, BRCA-negativo, subtipos tumorales, terapia personalizada