Clear Sky Science · it
Delimitazione dell’eterogeneità alla base dell’instabilità genomica nei tumori ereditari della mammella rivela quattro sottotipi di malattia
Perché questa ricerca è importante per le famiglie
Molte donne che sviluppano il cancro alla mammella hanno una forte storia familiare della malattia ma non presentano una mutazione nei noti geni BRCA1 o BRCA2. I medici sanno che questi tumori spesso si comportano in modo diverso e possono rispondere in modi particolari ai trattamenti, ma le ragioni sono rimaste poco chiare. Questo studio utilizza l’analisi dell’intero genoma per mostrare che i tumori ereditari della mammella privi di mutazioni BRCA1/2 non costituiscono un’unica entità, bensì ricadono in quattro gruppi genetici distinti, ognuno con un proprio schema di danno al DNA e potenziali vulnerabilità terapeutiche. Comprendere queste differenze nascoste potrebbe aiutare a personalizzare molto meglio le terapie per le pazienti e i loro familiari.
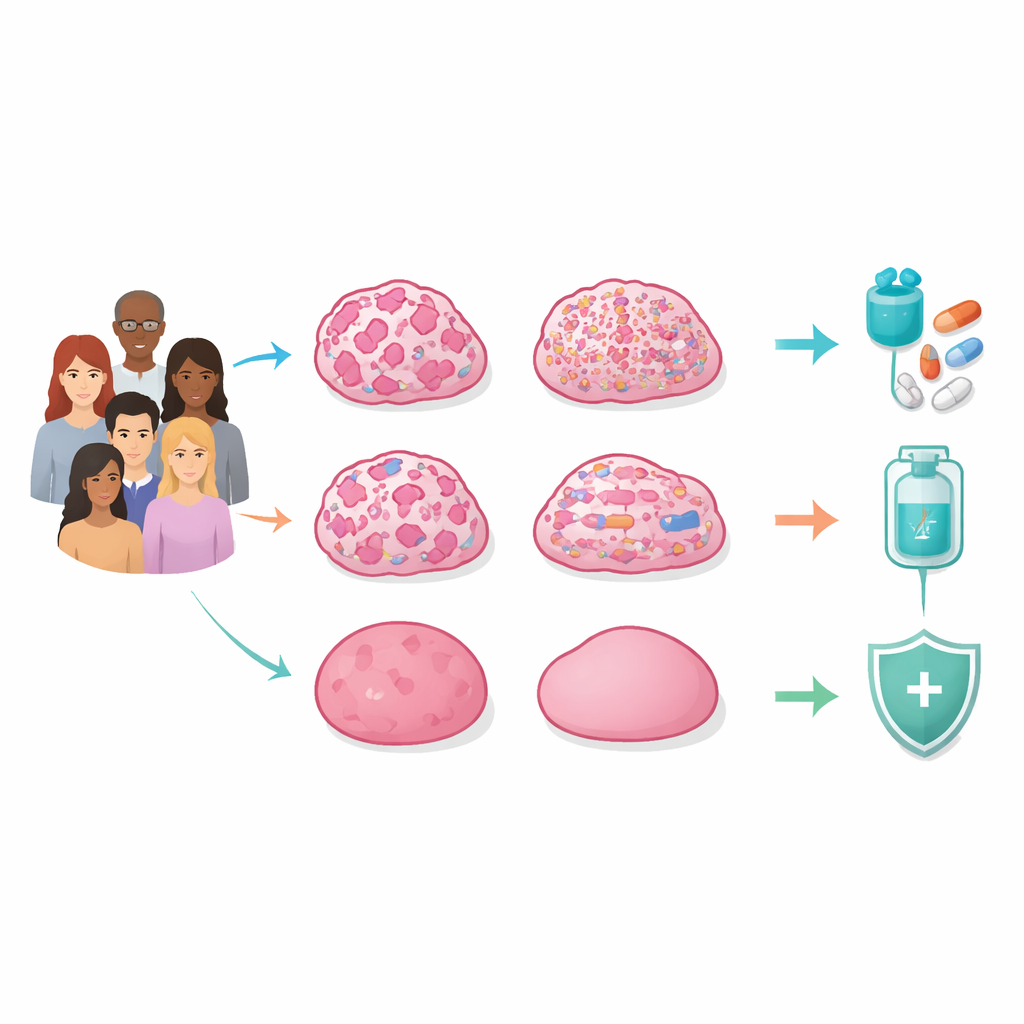
Quattro schemi nascosti all’interno dei tumori ereditari
I ricercatori hanno sequenziato l’intero genoma dei tumori e dei tessuti normali di 129 donne coreane con sospetto cancro ereditario della mammella risultate negative per varianti dannose in BRCA1/2. Hanno esaminato non solo le singole mutazioni geniche, ma anche rotture grandi e piccole, perdite, acquisizioni e riarrangiamenti nei cromosomi, oltre ai marcatori chimici sul DNA e all’attività genica. Integrando tutti questi livelli, hanno scoperto che la caratteristica centrale che distingue i tumori non è un singolo gene, ma il modello complessivo di instabilità genomica—quanto il DNA è stato danneggiato e disordinato.
Fallimento della riparazione del DNA, tempeste di mutazioni e genomi tranquilli
Un grande gruppo, denominato sottotipo deficiente nella ricombinazione omologa (HRD), mostrava diffuse “cicatrici cromosomiche” causate dal malfunzionamento di un importante sistema di riparazione del DNA. Anche in assenza di mutazioni ereditarie in BRCA1/2, molti di questi tumori avevano perso la funzione di BRCA tramite perdita della copia rimanente o tramite silenziamento del promotore del gene mediante ipermetilazione. I loro cromosomi erano fortemente riarrangiati, spesso con eventi catastrofici di frammentazione, e presentavano frequentemente mutazioni di TP53. Questi tumori tendevano ad essere carcinomi mammari triplo-negativi e a mostrare una sopravvivenza peggiore, ma apparivano anche particolarmente vulnerabili a farmaci che sfruttano la debolezza nella riparazione del DNA, come gli inibitori di PARP.
Tumori ricchi di mutazioni e tumori ricchi di alterazioni del numero di copie
Un secondo gruppo, il sottotipo a predominanza di mutazioni (MUT), aveva punteggi HRD relativamente bassi ma presentava un numero insolitamente elevato di mutazioni puntiformi. Molti di questi cambiamenti portavano la firma delle enzimi APOBEC, che possono scatenare “tempeste” locali di mutazioni note come kataegis. I tumori MUT mostravano forti segnali di attivazione immunitaria, inclusi geni usati dalle cellule T citotossiche e marcatori di macrofagi pro‑infiammatori, suggerendo che potrebbero essere particolarmente buoni candidati per l’immunoterapia, nonostante molti risulterebbero positivi per i recettori ormonali secondo i test standard. Un terzo gruppo, il sottotipo a predominanza di numero di copie (CN), accumulava invece molte piccole perdite e acquisizioni di DNA pur mantenendo un conteggio cromosomico complessivamente vicino alla normalità. Questi cambiamenti focali spesso eliminavano classici geni soppressori di tumore e erano accompagnati da uno stroma tumorale attivato e ricco di fibroblasti, suggerendo una sensibilità al platino o ai taxani, potenzialmente in combinazione con farmaci che prendono di mira il tessuto di supporto.
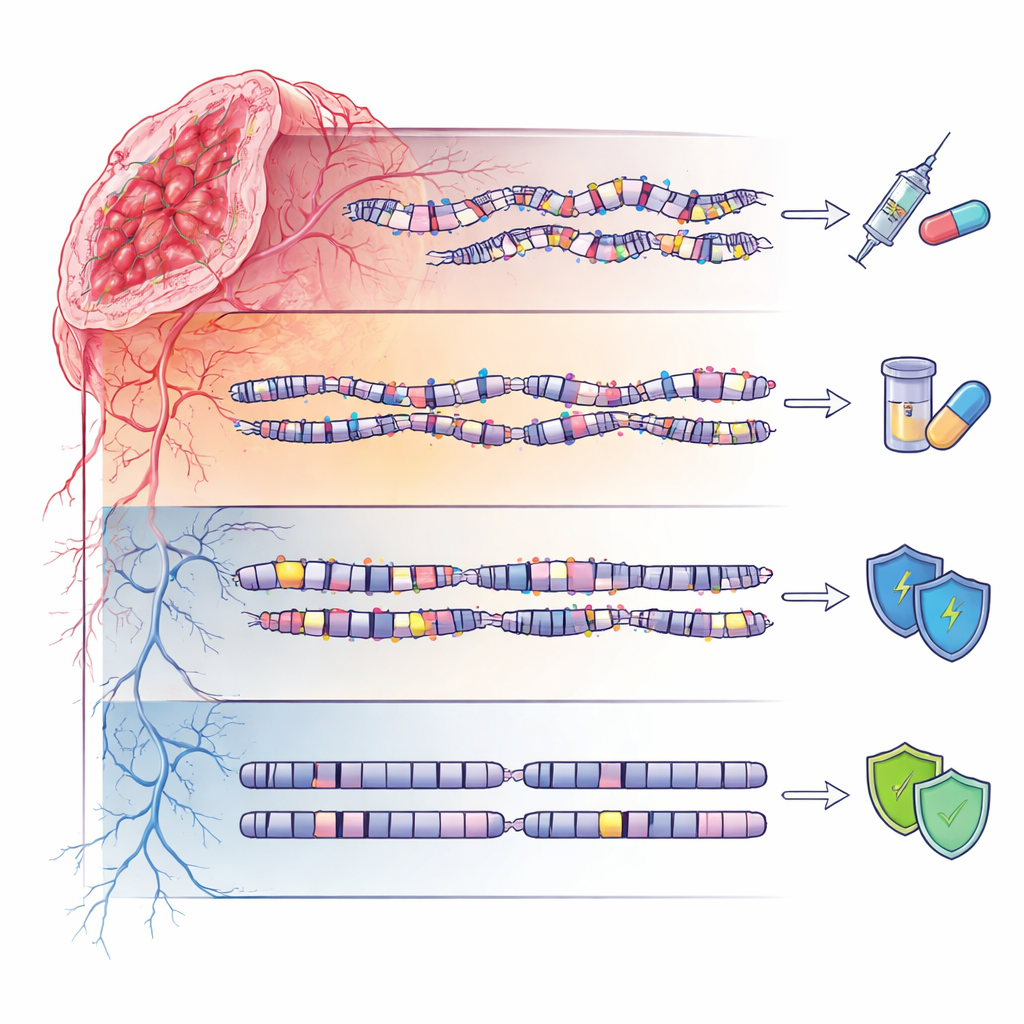
Genomi tranquilli e rischio ereditario
Il quarto gruppo, definito stabile a livello genomico (GS), mostrava paesaggi del DNA relativamente calmi, con poche mutazioni o disruption su larga scala. Eppure queste pazienti non erano prive di influenze ereditarie: erano arricchite per varianti germinali rare in diversi geni legati alla riparazione del DNA, molte delle quali sono ancora classificate come “varianti di significato incerto”. Ciò suggerisce che in alcune famiglie cambiamenti ereditari sottili possono predisporre al tumore senza provocare un caos genomico evidente, sottolineando la necessità di un’interpretazione attenta e sensibile alla provenienza ancestrale dei risultati dei test genetici, specialmente nelle popolazioni non europee.
Cosa significa per la cura futura
Superando i test su singoli geni e i sottotipi tradizionali basati sull’espressione, questo lavoro propone un “indice integrativo di instabilità genomica” che combina difetti di riparazione, carico mutazionale, cambiamenti nel numero di copie e firme strutturali per collocare i tumori ereditari della mammella in quattro gruppi meccanicistici. In termini pratici, supporta l’abbinamento dei tumori HRD agli inibitori di PARP, dei tumori guidati da alterazioni di numero di copie a specifiche chemioterapie e strategie di targeting dello stroma, e dei tumori ricchi di mutazioni all’immunoterapia, evidenziando al contempo la necessità di una rivalutazione continua delle varianti germinali nei casi genomicamente stabili. Per pazienti e clinici, lo studio indica un futuro in cui la gestione del cancro ereditario della mammella è guidata non solo dallo stato BRCA, ma da un quadro più ricco di come il DNA di ciascun tumore si è alterato.
Citazione: Kim, S., Lee, S., Kim, H. et al. Delineation of the heterogeneity underlying genomic instability in hereditary breast cancers reveals four disease subtypes. Exp Mol Med 58, 1254–1268 (2026). https://doi.org/10.1038/s12276-026-01693-4
Parole chiave: cancro ereditario della mammella, instabilità genomica, BRCA-negativo, sottotipi tumorali, terapia personalizzata