Clear Sky Science · nl
Afbakening van de heterogeniteit onderliggend aan genomische instabiliteit bij erfelijke borstkankers onthult vier ziekte‑subtypen
Waarom dit onderzoek belangrijk is voor families
Veel vrouwen die borstkanker ontwikkelen hebben een sterke familiegeschiedenis van de ziekte, maar geen mutatie in de bekende BRCA1‑ of BRCA2‑genen. Artsen weten dat deze tumoren zich vaak anders gedragen en op bijzondere wijze op behandeling kunnen reageren, maar de oorzaken daarvan waren onduidelijk. Deze studie gebruikt volledige genoomanalyse om aan te tonen dat erfelijke borstkankers zonder BRCA1/2‑mutaties geen eenduidige entiteit vormen, maar in vier duidelijke genetische groepen vallen, elk met een eigen patroon van DNA‑schade en potentiële therapeutische kwetsbaarheden. Het begrijpen van deze verborgen verschillen kan helpen therapieën veel preciezer af te stemmen voor patiënten en hun familieleden.
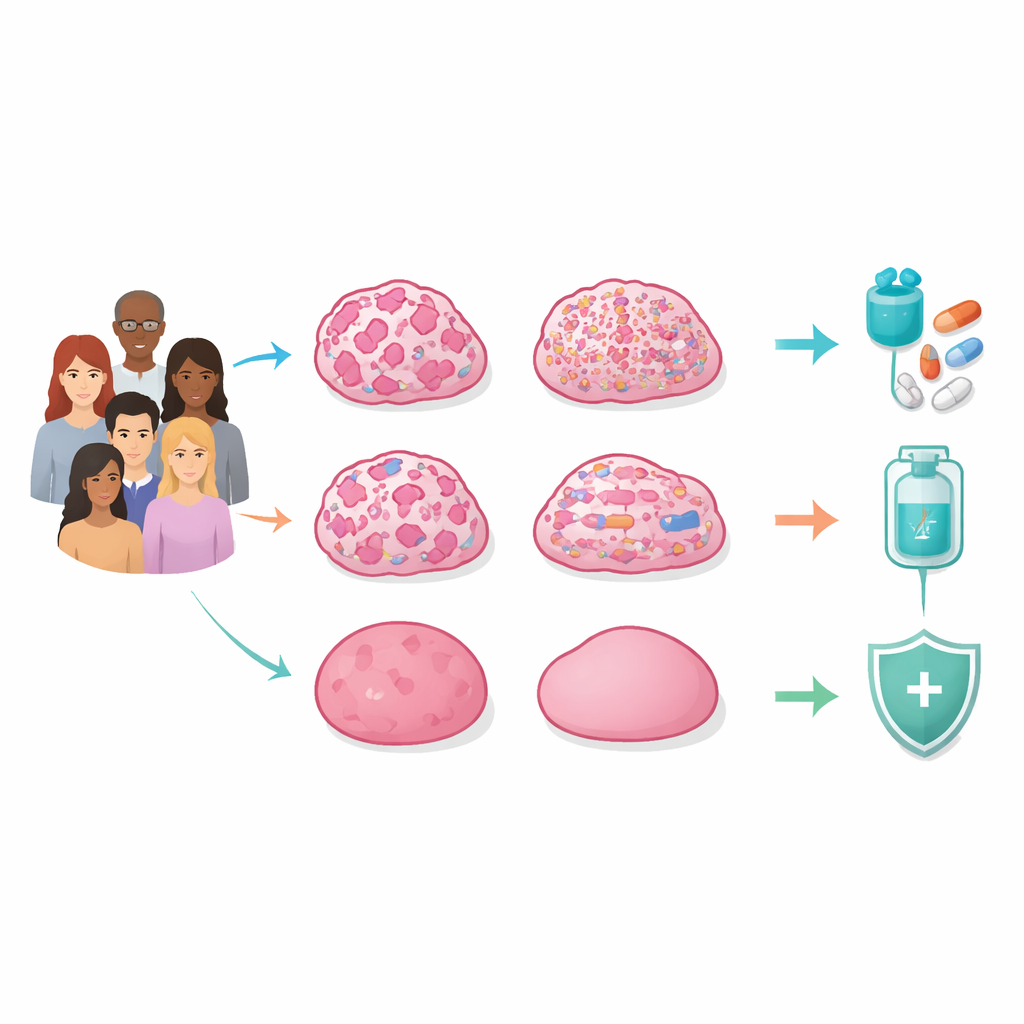
Vier verborgen patronen in erfelijke tumoren
De onderzoekers sequentieerden de volledige genomen van tumoren en normaal weefsel van 129 Koreaanse vrouwen met vermoedelijke erfelijke borstkanker die negatief testten op schadelijke BRCA1/2‑varianten. Ze bekeken niet alleen individuele genmutaties, maar ook grote en kleine breuken, verliezen, gains en herschikkingen over de chromosomen, en chemische labels op DNA en genactiviteit. Door al deze lagen te integreren, ontdekten zij dat het centrale kenmerk dat tumoren onderscheidt niet één enkel gen is, maar het algemene patroon van genomische instabiliteit — hoe beschadigd en ontregeld het DNA geworden is.
Falen van DNA‑herstel, mutatiestormen en rustige genomen
Een grote groep, aangeduid als het homologe recombinatie‑deficiënte (HRD) subtype, toonde wijdverspreide “chromosomale littekens” veroorzaakt door falen van een belangrijk DNA‑herstelsysteem. Zelfs zonder erfelijke BRCA1/2‑mutaties hadden veel van deze tumoren BRCA‑functie verloren door verlies van de overgebleven kopie of door het stilleggen van de promotor van het gen via extra methylatie. Hun chromosomen waren zwaar herschikt, vaak met catastrofale vergruizingsgebeurtenissen, en droegen vaak TP53‑mutaties. Deze tumoren neigden naar triple‑negatieve borstkankers en hadden een slechterere overleving, maar leken ook bijzonder kwetsbaar voor medicijnen die lenen van DNA‑herstelzwakte, zoals PARP‑remmers.
Mutatie‑rijke en kopie‑aantal‑rijke kankers
Een tweede groep, het mutatie‑dominante (MUT) subtype, had relatief lage HRD‑scores maar vertoonde uitzonderlijk veel puntmutaties. Veel van deze veranderingen droegen het kenmerk van APOBEC‑enzymen, die lokale “stormen” van mutaties kunnen veroorzaken, bekend als kataegis. MUT‑tumoren toonden sterke signalen van immuunactivatie, inclusief genen gebruikt door cytotoxische T‑cellen en merkers van pro‑inflammatoire macrofagen, wat suggereert dat ze bijzonder geschikte kandidaten voor immunotherapie kunnen zijn, ook al zouden velen volgens standaardtests als hormoonreceptor‑positief geclassificeerd worden. Een derde groep, het kopie‑aantal‑dominante (CN) subtype, verzamelde in plaats daarvan veel kleine DNA‑verliezen en ‑winstjes terwijl het totale chromosoomaantal grotendeels normaal bleef. Deze focale veranderingen verwijderden vaak klassieke tumorsuppressorgenen en gingen gepaard met een geactiveerd, fibroblast‑rijk tumormatrix, wat wijst op gevoeligheid voor platinum‑ of taxaanchemotherapie, mogelijk in combinatie met middelen die het ondersteunende weefsel richten.
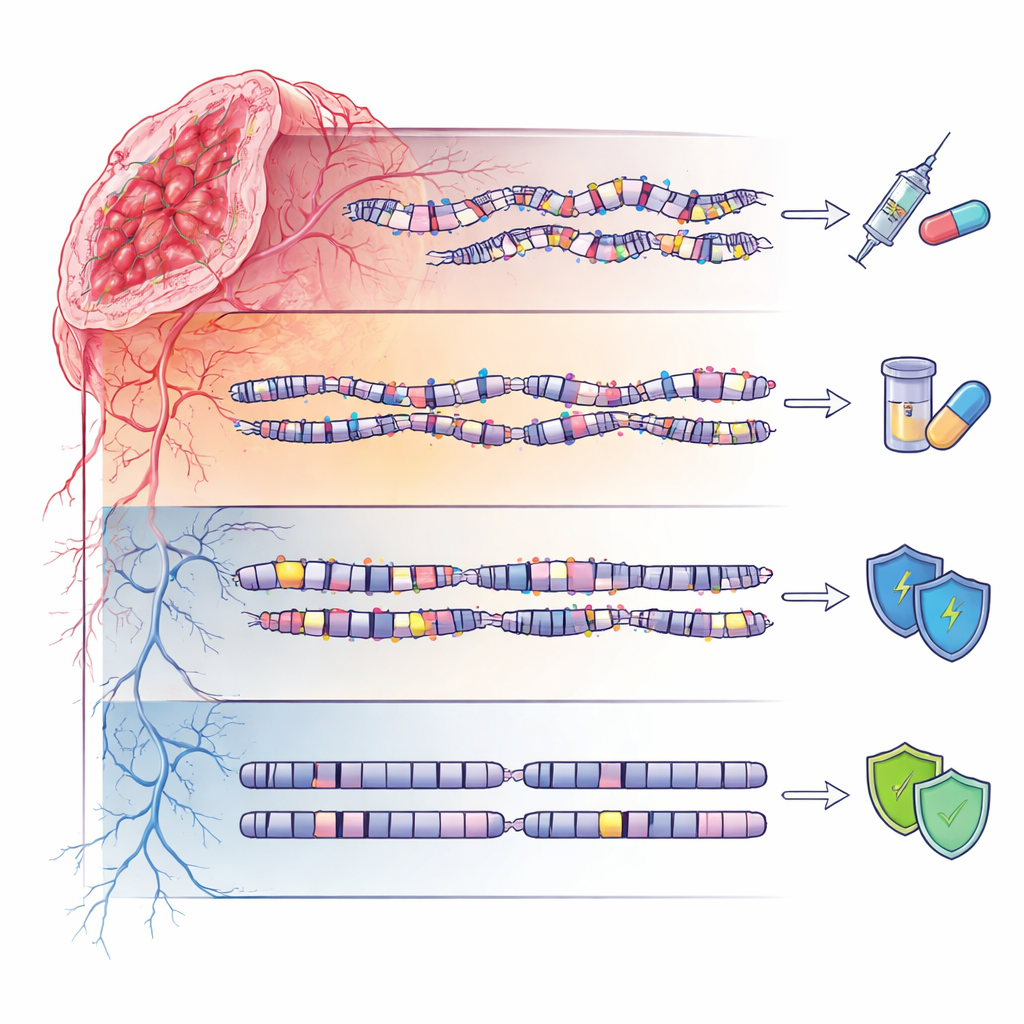
Rustige genomen en erfelijke risico's
De vierde groep, aangeduid als genoom‑stabiel (GS), vertoonde relatief rustige DNA‑landschappen met weinig mutaties of grootschalige verstoringen. Toch waren deze patiënten niet vrij van erfelijke invloeden: ze waren verrijkt voor zeldzame germinale varianten in meerdere genen die betrokken zijn bij DNA‑herstel, waarvan veel nog geclassificeerd zijn als “varianten van onzekere betekenis.” Dit suggereert dat in sommige families subtiele erfelijke veranderingen kunnen predisponeren tot kanker zonder dramatische genomische chaos te veroorzaken, wat het belang onderstreept van zorgvuldige, op afkomst gerichte interpretatie van genetische testresultaten, vooral in niet‑Europese populaties.
Wat dit betekent voor toekomstige zorg
Door verder te kijken dan testen op één gen en traditionele op expressie gebaseerde subtypen, stelt dit werk een “integratieve index voor genomische instabiliteit” voor die hersteldefecten, mutatiebelasting, kopie‑aantalveranderingen en structurele signaturen combineert om erfelijke borstkankers in vier mechanistische groepen te plaatsen. Praktisch gezien ondersteunt dit het koppelen van HRD‑tumoren aan PARP‑remmers, CN‑gedreven tumoren aan specifieke chemotherapieën en stroma‑gerichte strategieën, en mutatie‑rijke tumoren aan immunotherapie, terwijl het de noodzaak benadrukt van voortdurende herwaardering van germinale varianten in genoom‑stabiele gevallen. Voor patiënten en klinici wijst de studie op een toekomst waarin de zorg voor erfelijke borstkanker niet alleen door BRCA‑status wordt geleid, maar door een rijker beeld van hoe het DNA van elke tumor misgelopen is.
Bronvermelding: Kim, S., Lee, S., Kim, H. et al. Delineation of the heterogeneity underlying genomic instability in hereditary breast cancers reveals four disease subtypes. Exp Mol Med 58, 1254–1268 (2026). https://doi.org/10.1038/s12276-026-01693-4
Trefwoorden: erfelijke borstkanker, genomische instabiliteit, BRCA-negatief, tumor subtypen, gepersonaliseerde therapie