Clear Sky Science · tr
Miras yoluyla geçen meme kanserlerindeki genomik kararsızlığın altında yatan heterojenitenin belirlenmesi dört hastalık alt tipi ortaya koyuyor
Bu araştırma aileler için neden önemli
Meme kanseri geliştiren birçok kadının hastalık açısından güçlü bir aile öyküsü vardır, ancak iyi bilinen BRCA1 veya BRCA2 genlerinde bir mutasyon bulunmaz. Doktorlar bu tümörlerin sıklıkla farklı davrandığını ve tedaviye özel yanıtlar verebileceğini bilir, ancak nedenleri belirsiz kalmıştır. Bu çalışma tüm genom analizini kullanarak BRCA1/2 mutasyonu olmayan miras yoluyla geçen meme kanserlerinin tek bir varlık olmadığını, her birinin kendi DNA hasarı paterni ve potansiyel tedavi zayıflıkları olan dört açık genetik gruba ayrıldığını gösteriyor. Bu gizli farklılıkların anlaşılması, hastalar ve akrabaları için tedavilerin çok daha kesin şekilde uyarlanmasına yardımcı olabilir.
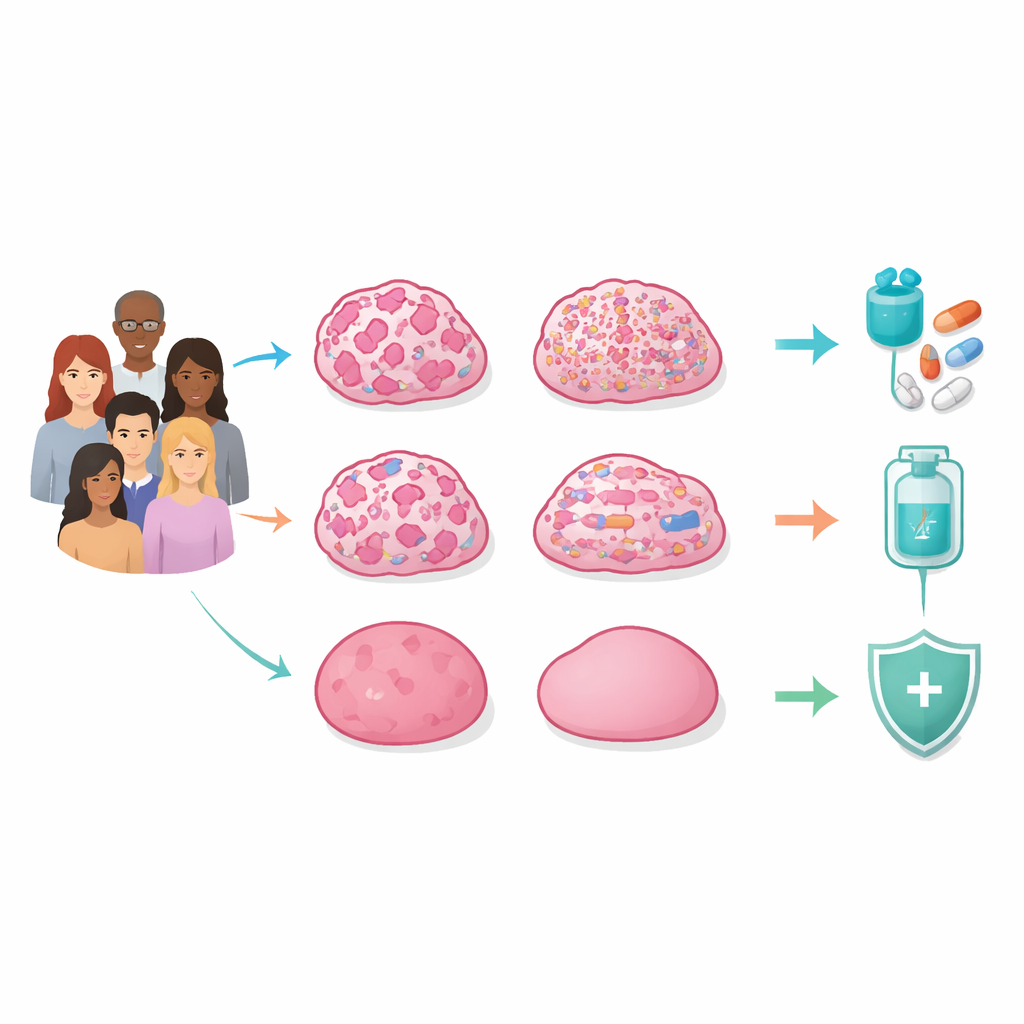
Miras alınan tümörlerin içindeki dört gizli desen
Araştırmacılar, zararlı BRCA1/2 varyantları için negatif çıkan şüpheli miras yoluyla geçen meme kanseri olan 129 Koreli kadının tümör ve normal dokusunun tamamını diziledi. Sadece tek tek gen mutasyonlarına bakmakla kalmayıp kromozomlar genelinde büyük ve küçük kırılmaları, kayıpları, kazanımları ve yeniden düzenlenmeleri ile DNA üzerindeki kimyasal etiketleri ve gen aktivitesini incelediler. Bu katmanların tümünü birleştirerek, tümörleri ayıran merkezi özelliğin tek bir gen değil, genomik kararsızlığın genel örüntüsü — DNA’nın ne kadar hasar görmüş ve düzensiz hale geldiği — olduğunu buldular.
DNA onarım başarısızlığı, mutasyon fırtınaları ve sakin genomlar
Bir ana grup, homolog rekombinasyon–yetersiz (HRD) alt tipi, anahtar bir DNA onarım sisteminin başarısızlığından kaynaklanan yaygın “kromozomal izler” gösterdi. Miras yoluyla geçen BRCA1/2 mutasyonları olmasa bile, bu tümörlerin birçoğu kalan kopyanın kaybı veya gen promotörünün fazladan metilasyonla susturulması yoluyla BRCA işlevini kaybetmişti. Kromozomları yoğun biçimde yeniden düzenlenmiş, sıklıkla yıkıcı parçalanma olayları geçirmiş ve sık sık TP53 mutasyonları taşıyordu. Bu tümörler genelde üçlü-negatif meme kanseri olma eğilimindeydi ve daha kötü sağkalımla ilişkiliydi, ancak PARP inhibitörleri gibi DNA onarım zayıflığını hedef alan ilaçlara karşı özellikle hassas görünüyordu.
Mutasyon ağırlıklı ve kopya sayısı ağırlıklı kanserler
İkinci bir grup olan mutasyon‑dominant (MUT) alt tipi, nispeten düşük HRD skorlarına rağmen olağanüstü yüksek sayıda nokta mutasyonu taşıyordu. Bu değişikliklerin birçoğu, lokal “kataegis” olarak bilinen mutasyon fırtınalarına yol açabilen APOBEC enzimlerinin ayırt edici izlerini taşıyordu. MUT tümörleri, katil T hücreleri tarafından kullanılan genler ve pro‑inflamatuar makrofaj işaretçileri dahil olmak üzere güçlü bağışıklık aktivasyon sinyalleri gösteriyordu; bu da standart testlerle birçok örnek hormon reseptör‑pozitif sınıfına girse bile bu tümörlerin immünoterapi için özellikle uygun adaylar olabileceğini düşündürüyor. Üçüncü grup olan kopya‑sayı‑dominant (CN) alt tipi ise genel olarak yakın‑normal kromozom sayısını korurken çok sayıda küçük DNA kaybı ve kazancı biriktiriyordu. Bu odaklanmış değişiklikler sıklıkla klasik tümör‑baskılayıcı genleri ortadan kaldırıyor ve etkinleşmiş, fibroblastça zengin bir tümör stroma ile birlikte görülüyordu; bu durum platinum veya taksan kemoterapilerine ve muhtemelen destekleyici doku hedefleyen ilaçlarla kombinasyon halinde duyarlılığa işaret ediyor.
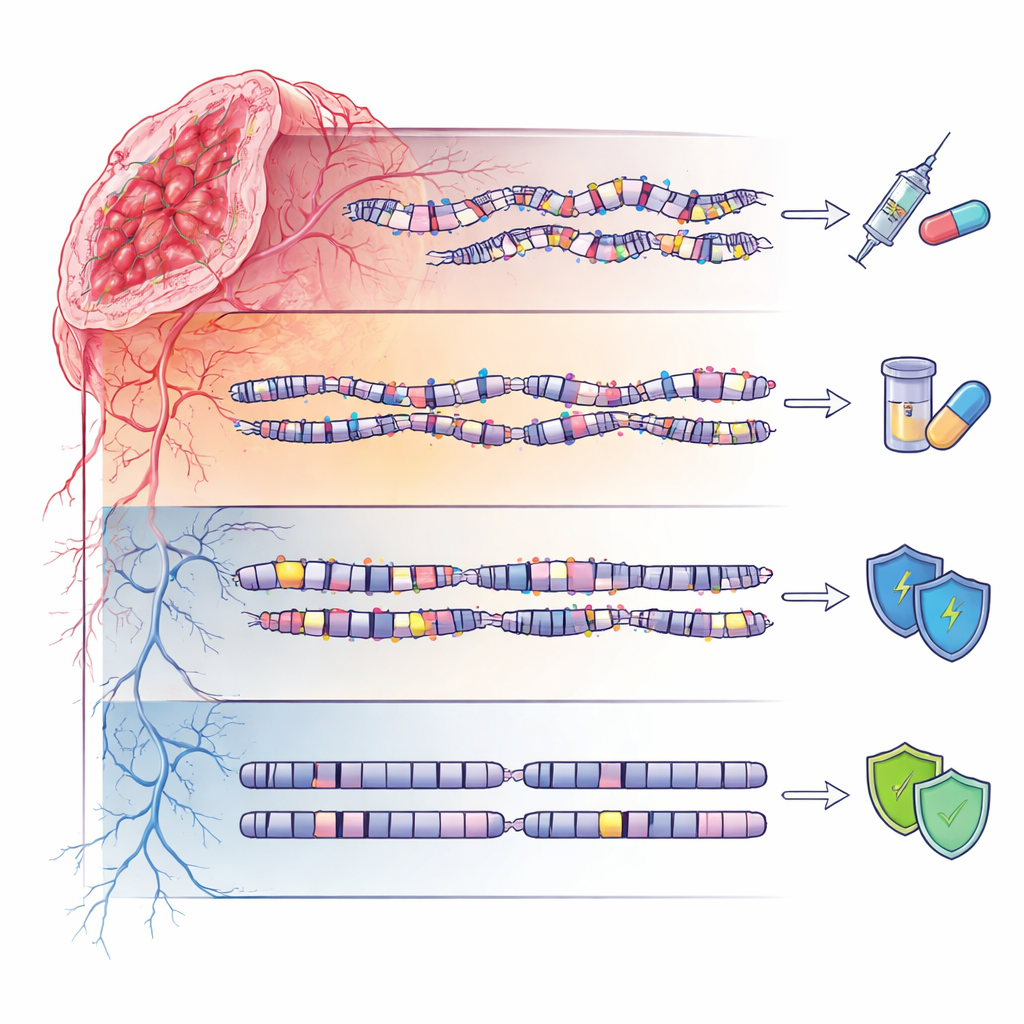
Sakin genomlar ve kalıtsal risk
Dördüncü grup, genom‑stabil (GS) olarak adlandırılan grup, az sayıda mutasyon veya büyük ölçekli bozulma ile nispeten sakin DNA manzaraları gösterdi. Yine de bu hastaların kalıtsal etkilerden muaf olmadığı görüldü: birkaç DNA onarım ilişkili gende nadir germline varyantlar açısından zenginleşmişlerdi; bunların birçoğu hâlâ “önem belirsiz varyantlar” olarak sınıflandırılıyor. Bu durum bazı ailelerde, dramatik genomik kaosa yol açmaksızın kansere yatkınlık veren ince kalıtsal değişikliklerin olabileceğini öne sürüyor ve özellikle Avrupa dışı popülasyonlarda genetik test sonuçlarının köken‑farkındalıklı dikkatle yorumlanması gerektiğini vurguluyor.
Gelecekteki bakım için ne anlama geliyor
Tek gen testlerinin ve geleneksel ifade‑tabanlı alt tiplerin ötesine geçerek bu çalışma, onarım kusurlarını, mutasyon yükünü, kopya‑sayı değişikliklerini ve yapısal imzaları birleştiren “bütünleştirici genomik kararsızlık indeksi” öneriyor ve miras yoluyla geçen meme kanserlerini dört mekanistik gruba yerleştiriyor. Pratik açıdan bu, HRD tümörlerinin PARP inhibitörleriyle, CN‑kaynaklı tümörlerin belirli kemoterapiler ve stromaya yönelik stratejilerle; mutasyon‑ağırlıklı tümörlerin ise immünoterapiyle eşleştirilmesini destekliyor ve genom‑stabil vakalarda germline varyantların sürekli yeniden değerlendirilmesi gereğini vurguluyor. Hastalar ve klinisyenler için çalışma, miras yoluyla geçen meme kanseri bakımının sadece BRCA durumuna değil, her tümörün DNA’sının nasıl bozulduğuna dair daha zengin bir resme göre yönlendirileceği bir geleceğe işaret ediyor.
Atıf: Kim, S., Lee, S., Kim, H. et al. Delineation of the heterogeneity underlying genomic instability in hereditary breast cancers reveals four disease subtypes. Exp Mol Med 58, 1254–1268 (2026). https://doi.org/10.1038/s12276-026-01693-4
Anahtar kelimeler: miras yoluyla geçen meme kanseri, genomik kararsızlık, BRCA-negatif, tümör alt tipleri, kişiselleştirilmiş tedavi