Clear Sky Science · zh
PARP 抑制剂与乳腺癌:从治疗突破到耐药挑战
这对患者和家庭为何重要
乳腺癌目前已成为全球女性中最常见的癌症,得益于更有效的药物,许多人存活时间更长。一类较新的药物——PARP 抑制剂,为肿瘤携带某些遗传缺陷的患者带来了新的希望。本文解释了这些药物的作用机制、为何它们能如此有效以及肿瘤如何随着时间学会“绕过”它们。理解这些内容可以让医生和患者对治疗有更清晰的预期,并指明未来可能延长对乳腺癌控制的治疗方向。
利用癌症薄弱环节的靶向药物
乳腺癌并非一种单一疾病,而是由多种亚型构成,行为各异、需要不同的治疗策略。缺乏激素受体或 HER2 信号的肿瘤,例如许多三阴性乳腺癌,尤其具有侵袭性且难以治疗。PARP 抑制剂旨在靶向那些本身就难以修复 DNA 的肿瘤,尤其是携带遗传或获得性 BRCA1 或 BRCA2 基因改变的肿瘤。通过阻断通常负责修补日常 DNA 损伤的 PARP 蛋白,这些药物使本已脆弱的癌细胞超出生存极限导致死亡,同时对大多数健康细胞的影响较小。像 OlympiA 和 EMBRACA 等大型临床试验显示,PARP 抑制剂可以在经选择的患者中延长疾病进展的时间。
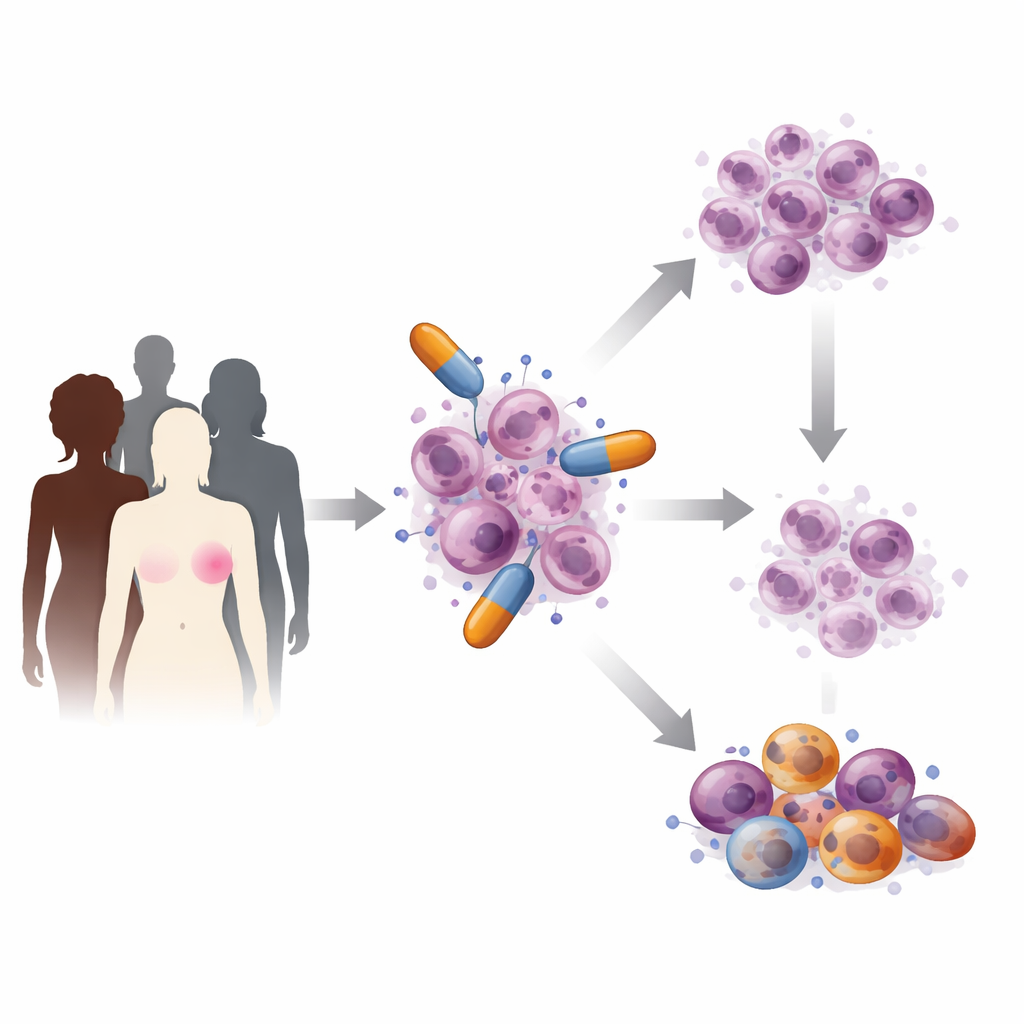
PARP 药物如何攻击癌细胞
在每个细胞内,DNA 不断受到切割并被修复。PARP 蛋白是某些类型断裂的“第一响应者”,它们呼唤修复机器并帮助维持 DNA 复制的正常进行。PARP 抑制剂进入这些蛋白的活性位点,阻断其修复活性或使其牢固地滞留在断裂的 DNA 上。结果,小的断裂累积并与细胞的 DNA 复制机器相冲突,导致对携带 BRCA 缺陷的细胞而言无法修复的更严重损伤。研究人员还发现,这些药物会干扰新DNA 链的完成,产生随后崩塌为危险断裂的间隙,改变细胞处理关键代谢物的方式,甚至触发免疫警报信号,有助于机体免疫识别并攻击肿瘤。
来自临床试验与真实世界治疗的证据
目前有几种 PARP 抑制剂在乳腺癌中获批或正在研究中。奥拉帕利(olaparib)和塔拉唑帕利(talazoparib)是针对晚期 HER2 阴性并携带 BRCA 突变患者的主要选择,也已在早期疾病中进行过试验。该家族的其他药物,如尼拉帕利、鲁卡帕利、维利帕利、富珠帕利和帕米帕利,正在不同情境或地区开展研究,有时与化疗联合。尽管许多试验报告显示肿瘤生长明显延缓,但对总生存期的获益存在变异,且低血细胞计数等副作用仍是关注点。文章还指出,受控试验之外的真实世界数据仍然有限,尤其针对较新药物和来自多样化患者群体的数据。
肿瘤如何学会抵抗 PARP 治疗
尽管早期疗效可观,许多患者最终仍会出现对 PARP 抑制剂的耐药。综述描述了肿瘤细胞采用的几种巧妙逃逸路线。有些肿瘤通过获得使 BRCA 功能恢复的新突变或通过改变 DNA 标记使基因重新激活,从而恢复 DNA 修复能力。另一些则保护脆弱的 DNA 复制结构以防止在压力下崩溃,或调整组织染色质的方式(如组蛋白的处理),使染色体更稳定。在某些情况下,癌细胞通过更有效地将药物泵出细胞来降低细胞内药物浓度。这些多层次的耐药策略有助解释为何疗效常随时间衰减以及为何相同药物在不同患者间的效果差异很大。
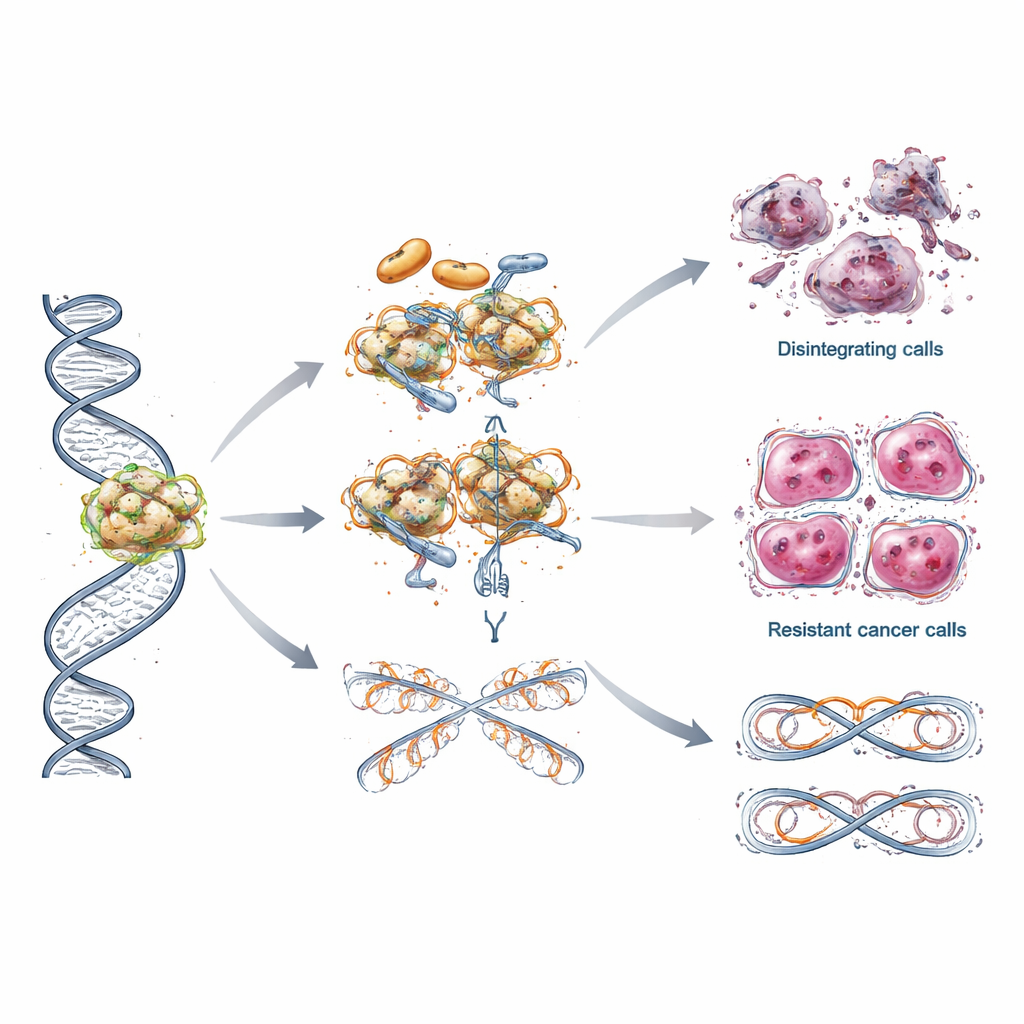
下一步:更聪明的组合与更广泛的可及性
为抢在耐药之前,研究者正在测试将 PARP 抑制剂与化疗、免疫检查点抑制剂以及阻断癌细胞其他应激通路的药物联合使用。希望是通过基因标志指导的合理组合,使肿瘤更难逃逸同时保持可控的副作用。作者还呼吁开发对健康血细胞更具选择性的下一代 PARP 药物、建立更好的预测工具以识别受益者,并关注在资源有限环境中这些治疗的成本与可及性。简单来说,PARP 抑制剂将某些乳腺癌的遗传脆弱性转化为真正的治疗机会,但要实现持久控制,需要理解并阻断肿瘤反击的多种方式。
引用: Wang, W., Cai, C., Qin, S. et al. PARP inhibitors and breast cancer: from therapeutic breakthrough to resistance challenge. Exp Mol Med 58, 981–992 (2026). https://doi.org/10.1038/s12276-026-01673-8
关键词: PARP 抑制剂, 乳腺癌, BRCA 突变, 药物耐药, 靶向治疗