Clear Sky Science · ar
مثبطات PARP وسرطان الثدي: من اختراق علاجي إلى تحدي المقاومة
لماذا يهم هذا المرضى والأسر
أصبح سرطان الثدي الآن أكثر أنواع السرطان شيوعًا بين النساء على مستوى العالم، ويعيش الكثيرون فترة أطول بفضل أدوية أفضل. قدم فئة أحدث من الأدوية، تُسمى مثبطات PARP، أملًا جديدًا للمرضى الذين تحمل أورامهم بعض العيوب الجينية. يشرح هذا المقال كيف تعمل هذه الأدوية، ولماذا يمكن أن تكون فعّالة للغاية، وكيف تتمكن الأورام تدريجيًا من التفوق عليها. إن فهم ذلك يزوّد الأطباء والمرضى بتوقعات أوضح ويشير إلى علاجات مستقبلية قد تحافظ على السيطرة على سرطان الثدي لفترات أطول.
أدوية موجهة تستغل نقاط ضعف السرطان
سرطان الثدي ليس مرضًا واحدًا، بل مجموعة من الأنماط الفرعية التي تتصرف بشكل مختلف وتتطلب رعاية مخصصة. الأورام التي تفتقر إلى إشارات الهرمونات أو HER2، مثل العديد من سرطانات الثدي الثلاثية السلبية، تكون عدوانية وصعبة العلاج بشكل خاص. طُوِّرت مثبطات PARP لاستهداف الأورام التي تواجه بالفعل صعوبة في إصلاح حمضها النووي، خصوصًا تلك التي تحوي تغيّرات موروثة أو مكتسبة في جينات BRCA1 أو BRCA2. عن طريق منع بروتينات PARP، التي تساعد عادةً في إصلاح الأضرار اليومية في الحمض النووي، تدفع هذه الأدوية الخلايا السرطانية الضعيفة بالفعل إلى تجاوز حدودها، مما يؤدي إلى موتها مع الحفاظ على معظم الخلايا السليمة. لقد أظهرت تجارب سريرية كبرى مثل OlympiA وEMBRACA أن مثبطات PARP يمكن أن تطيل الفترة قبل تفاقم المرض لدى مرضى محددين.
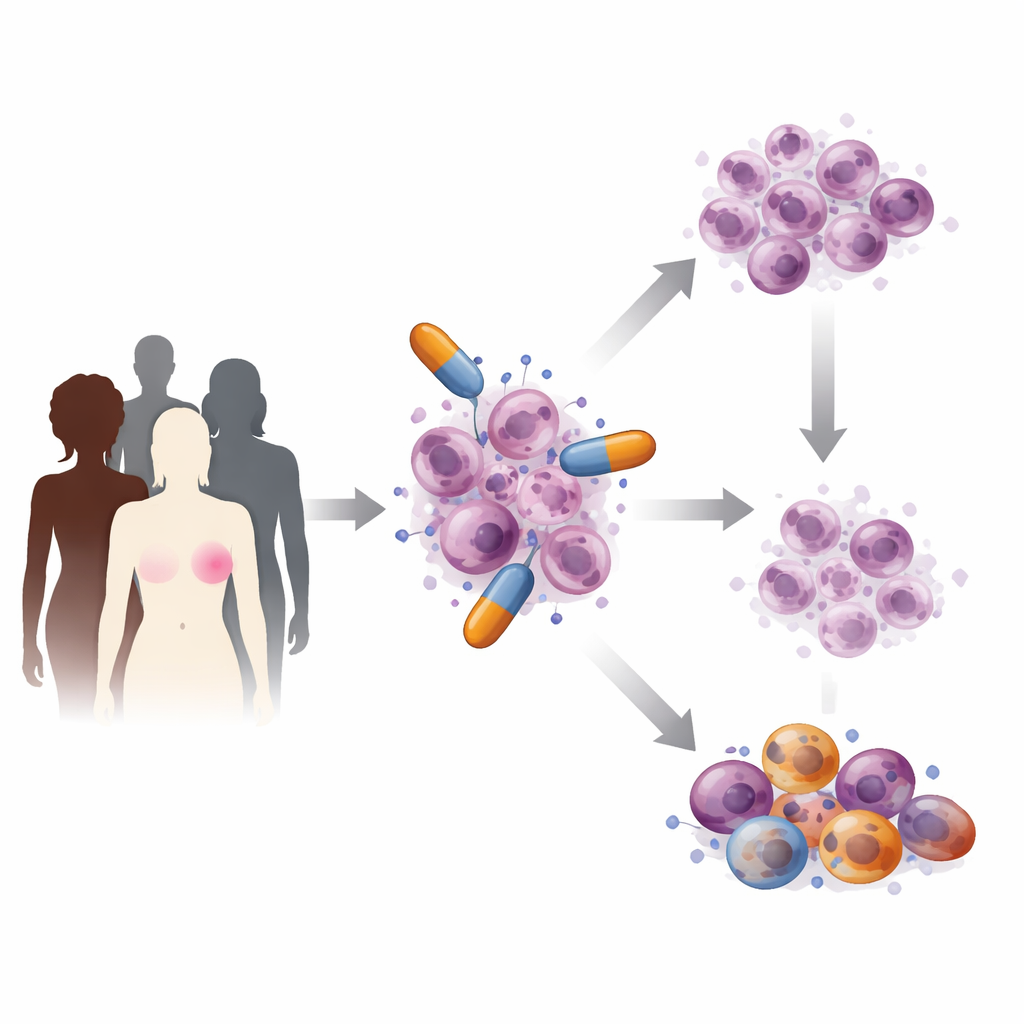
كيف تهاجم أدوية PARP الخلايا السرطانية
داخل كل خلية، يتعرّض الحمض النووي للشقوق والإصلاح باستمرار. تعمل بروتينات PARP كمستجيبين أوّليين لأنواع معيّنة من الكسور، فتستدعي آليات الإصلاح وتساعد في إبقاء نسخ الحمض النووي منظمة. تنزلق مثبطات PARP إلى الموقع النشط لهذه البروتينات وتمنع نشاطها الإصلاحي أو تتسبب في التصاقها بشدّة بالحمض النووي المكسور. نتيجة لذلك، تتراكم الشقوق الصغيرة وتتصادم مع آلية نسخ الحمض النووي في الخلية، مما يؤدي إلى أضرار أكثر خطورة لا تستطيع الخلايا ذات جينات BRCA المعطوبة إصلاحها. اكتشف العلماء أيضًا أن هذه الأدوية تشوّه كيفية إنهاء سلاسل الحمض النووي الجديدة، وتخلق فجوات تنهار لاحقًا إلى كسور خطيرة، وتغيّر كيفية تعامل الخلايا مع المغذيات الأساسية للتفاعلات الكيميائية، وتثير إشارات إنذار مناعية يمكن أن تساعد دفاعات الجسم في التعرف على الأورام ومهاجمتها.
الأدلة من التجارب والعلاج في العالم الواقعي
هناك عدة مثبطات PARP مستخدمة الآن أو قيد الدراسة لسرطان الثدي. أولاباريب وتالازوباريب هما الخياران الرئيسيان للمرضى ذوي المرض المتقدّم السلبي لـ HER2 والذين لديهم طفرات BRCA، كما تم اختباره أيضًا في مراحل أبكر من المرض. تُستَكشف أدوية أخرى في هذه الفئة، مثل نيراباريب، روكاباريب، فيليباريب، فوزولوباريب وباميباريب، في إعدادات أو مناطق مختلفة، أحيانًا بالاشتراك مع العلاج الكيميائي. في حين تُبلغ العديد من التجارب عن تأخيرات واضحة في نمو الورم، قد تختلف فوائد البقاء الإجمالي، وتظل الآثار الجانبية مثل انخفاض عدد خلايا الدم مصدر قلق. كما يشير المقال إلى أن البيانات من الممارسة اليومية، خارج التجارب المحكمة، لا تزال محدودة، لا سيما بالنسبة للعوامل الأحدث وللمرضى من خلفيات متنوعة.
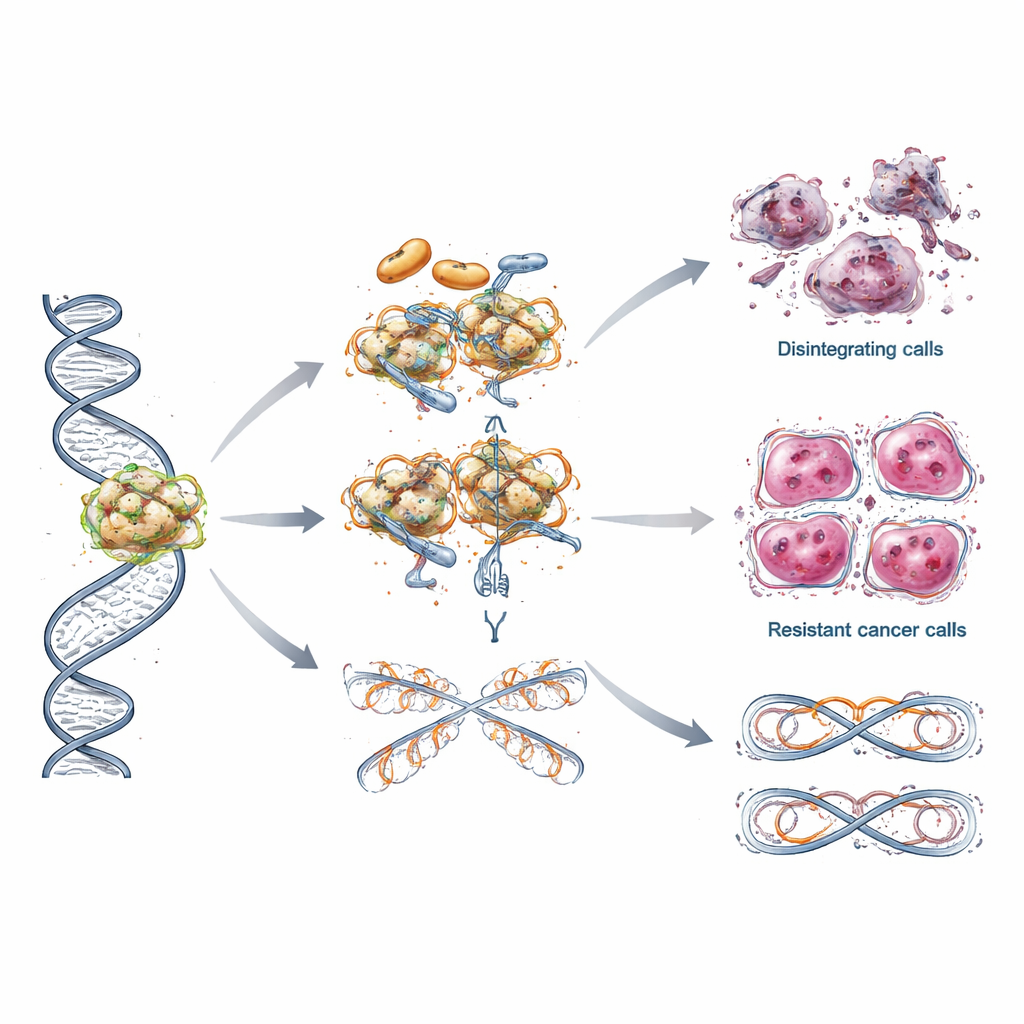
كيف تتعلم الأورام مقاومة علاج PARP
على الرغم من النجاح المبكّر، يرى كثير من المرضى في نهاية المطاف أن أورامهم تتوقّف عن الاستجابة لمثبطات PARP. يصف الاستعراض عدّة طرق هروب ذكية تستخدمها الخلايا الورمية. يستعيد بعضها قدرة إصلاح الحمض النووي من خلال اكتساب طفرات جديدة تُعيد وظيفة BRCA أو عن طريق إعادة تشغيل نشاط الجين عبر تغييرات في وسم الحمض النووي. يحمي آخرون آلية نسخ الحمض النووي الحسّاسة بحيث لا تنهار تحت الضغوط، أو يعدّلون كيفية التعامل مع بروتينات تغليف الحمض النووي المعروفة بالهيستونات حتى تظل كروموسوماتهم أكثر استقرارًا. في بعض الحالات، تضخ الخلايا السرطانية الدواء خارجها بكفاءة أكبر، مما يخفض تركيزه داخل الخلية. تساعد هذه الحيل المقاومة متعددة الطبقات في تفسير سبب تلاشي الاستجابات غالبًا ولماذا قد يعمل نفس الدواء بشكل مختلف من مريض لآخر.
الخطوات التالية: تراكيب أكثر ذكاءً ووصول أوسع
للبقاء أمام المقاومة، يختبر الباحثون مثبطات PARP جنبًا إلى جنب مع العلاج الكيميائي، وأدوية نقاط التفتيش المناعية، وأدوية تمنع مسارات استجابة الإجهاد الأخرى داخل الخلايا السرطانية. الأمل هو أن تجعل التركيبات المختارة جيدًا، والمدفوعة بعلامات جينية، هروب الأورام أكثر صعوبة مع الحفاظ على آثار جانبية قابلة للإدارة. كما يدعو المؤلفون إلى تطوير مثبطات PARP أكثر انتقائية من الجيل التالي تحمي خلايا الدم السليمة، وأدوات أفضل للتنبؤ بمن سيستفيد، وإيلاء الاهتمام لتكلفة وتوافر هذه العلاجات في البيئات قليلة الموارد. ببساطة، حولت مثبطات PARP نقطة ضعف جينية في بعض سرطانات الثدي إلى فرصة علاجية حقيقية، لكن السيطرة طويلة الأمد ستتطلب فهمًا وإحكامًا لسبل متعددة تكافح بها الأورام.
الاستشهاد: Wang, W., Cai, C., Qin, S. et al. PARP inhibitors and breast cancer: from therapeutic breakthrough to resistance challenge. Exp Mol Med 58, 981–992 (2026). https://doi.org/10.1038/s12276-026-01673-8
الكلمات المفتاحية: مثبطات PARP, سرطان الثدي, طفرات BRCA, مقاومة الأدوية, العلاج الموجَّه