Clear Sky Science · es
Inhibidores de PARP y cáncer de mama: del avance terapéutico al reto de la resistencia
Por qué esto importa para pacientes y familias
El cáncer de mama es hoy el tumor más frecuente en mujeres en todo el mundo, y muchas personas viven más tiempo gracias a tratamientos más eficaces. Una clase de medicamentos relativamente nueva, los inhibidores de PARP, ha ofrecido una nueva esperanza a pacientes cuyos tumores presentan ciertos defectos genéticos. Este artículo explica cómo funcionan estos fármacos, por qué pueden ser tan efectivos y cómo los cánceres consiguen eludirlos con el tiempo. Entenderlo dota a médicos y pacientes de expectativas más claras y apunta a tratamientos futuros que podrían mantener el cáncer de mama controlado durante más tiempo.
Fármacos dirigidos que explotan las debilidades del cáncer
El cáncer de mama no es una sola enfermedad, sino un conjunto de subtipos que se comportan de forma distinta y requieren cuidados personalizados. Los tumores que carecen de señales hormonales o de HER2, como muchos carcinomas triple negativos, son especialmente agresivos y difíciles de tratar. Los inhibidores de PARP se desarrollaron para atacar tumores que ya tienen problemas para reparar su ADN, en especial aquellos con alteraciones hereditarias o adquiridas en los genes BRCA1 o BRCA2. Al bloquear las proteínas PARP, que normalmente ayudan a reparar los daños cotidianos del ADN, estos fármacos llevan a las células cancerosas ya vulnerables más allá de su límite, provocando su muerte mientras suelen preservar la mayoría de las células sanas. Ensayos clínicos importantes como OlympiA y EMBRACA han mostrado que los inhibidores de PARP pueden prolongar el tiempo hasta la progresión de la enfermedad en pacientes seleccionados.
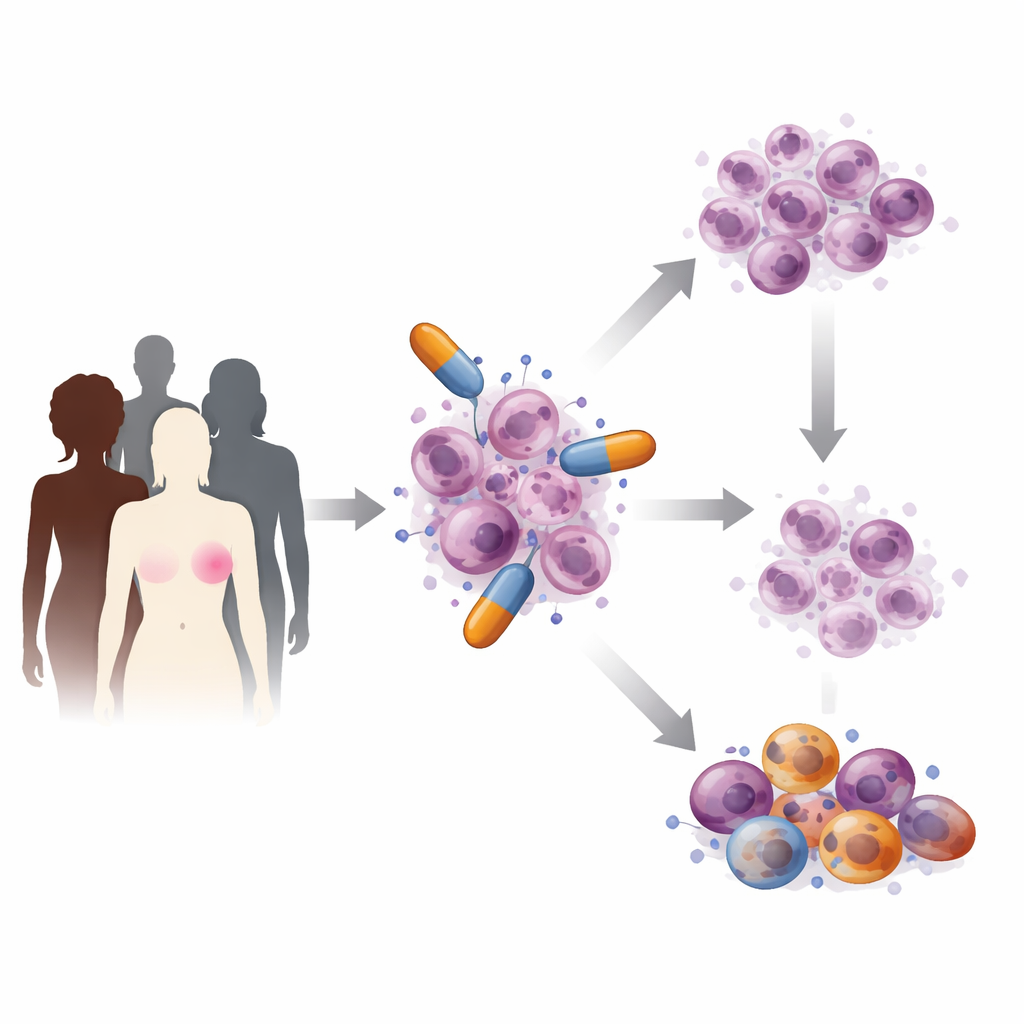
Cómo atacan las células cancerosas los fármacos PARP
Dentro de cada célula, el ADN sufre constantemente roturas y reparaciones. Las proteínas PARP actúan como los primeros intervinientes ante ciertos tipos de roturas, reclutando a los equipos de reparación y ayudando a mantener el proceso de copia del ADN. Los inhibidores de PARP se introducen en el sitio activo de estas proteínas y bloquean su actividad reparadora o hacen que queden fuertemente adheridas al ADN roto. Como resultado, las pequeñas roturas se acumulan y colisionan con la maquinaria de replicación del ADN, provocando daños más graves que las células con genes BRCA defectuosos no pueden reparar. Los científicos también han descubierto que estos fármacos alteran la finalización de las nuevas cadenas de ADN, generan huecos que después colapsan en roturas peligrosas, modifican el manejo de nutrientes clave para reacciones químicas celulares e incluso desencadenan señales inmunitarias que pueden ayudar a las defensas del organismo a reconocer y atacar los tumores.
Evidencia de ensayos y del tratamiento en la práctica clínica
Varios inhibidores de PARP están actualmente en uso o en estudio para el cáncer de mama. Olaparib y talazoparib son las principales opciones para pacientes con enfermedad avanzada HER2 negativa y mutaciones BRCA, y también se han testeado en estadios más precoces del cáncer. Otros fármacos de esta familia, como niraparib, rucaparib, veliparib, fuzuloparib y pamiparib, se exploran en distintos contextos o regiones, a veces en combinación con quimioterapia. Aunque muchos ensayos muestran demoras claras en el crecimiento tumoral, los beneficios en supervivencia global pueden variar, y los efectos secundarios como la disminución de las células sanguíneas siguen siendo una preocupación. El artículo también señala que los datos procedentes de la práctica clínica diaria, más allá de los ensayos controlados, siguen siendo limitados, especialmente para agentes más nuevos y para pacientes de orígenes diversos.
Cómo los tumores aprenden a resistir el tratamiento con PARP
A pesar del éxito inicial, muchos pacientes finalmente ven cómo su cáncer deja de responder a los inhibidores de PARP. La revisión describe varias vías de escape ingeniosas empleadas por las células tumorales. Algunas vuelven a recuperar la capacidad de reparar el ADN adquiriendo nuevas mutaciones que restauran la función de BRCA o reactivando la expresión génica mediante cambios en el marcado del ADN. Otras protegen la delicada maquinaria de replicación para que no colapse bajo estrés, o ajustan el manejo de las proteínas que empaquetan el ADN, llamadas histonas, de modo que sus cromosomas permanecen más estables. En algunos casos, las células cancerosas simplemente bombean el fármaco hacia fuera con mayor eficacia, reduciendo su concentración intracelular. Estas estrategias de resistencia en capas ayudan a explicar por qué las respuestas suelen desvanecerse y por qué el mismo fármaco puede funcionar de forma distinta entre pacientes.
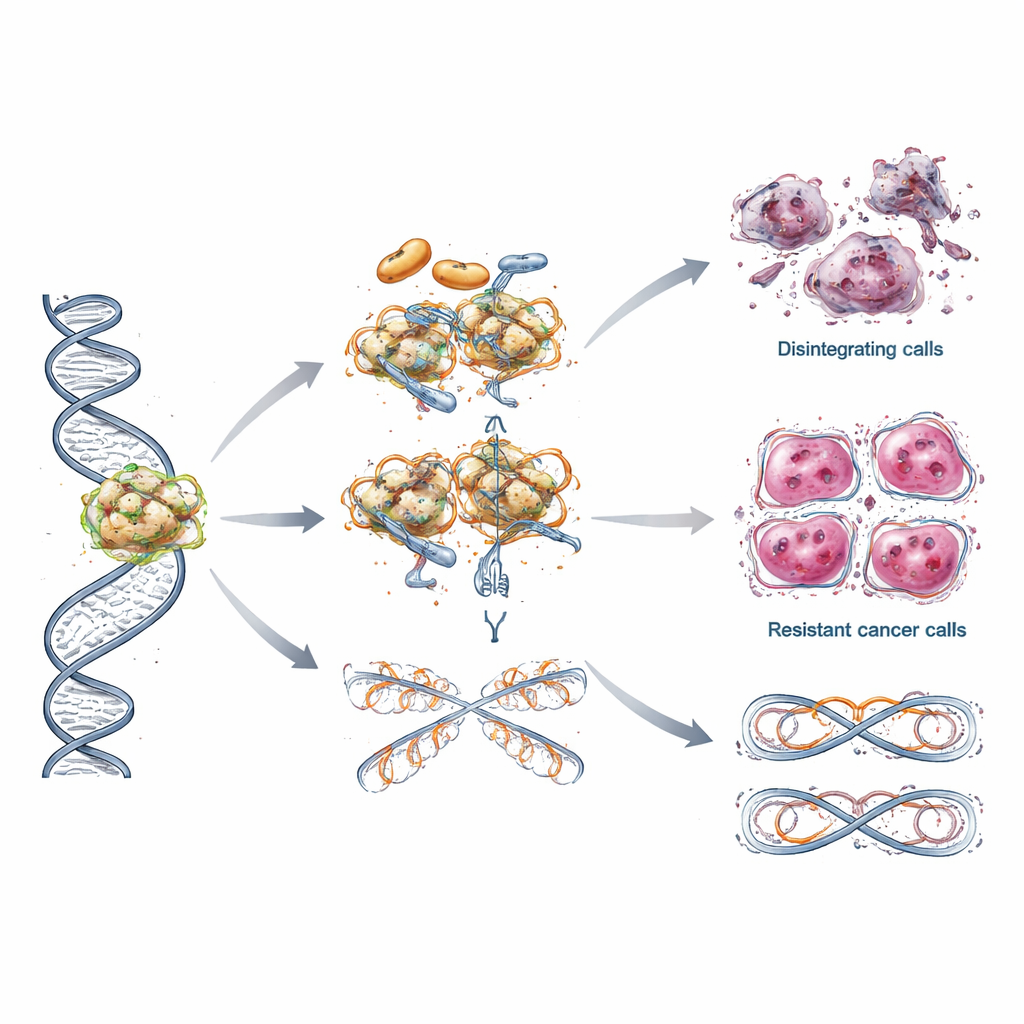
Próximos pasos: combinaciones más inteligentes y mayor acceso
Para adelantarse a la resistencia, los investigadores están probando los inhibidores de PARP junto con quimioterapia, fármacos inmunoterapéuticos que actúan sobre puntos de control inmunitario y medicamentos que bloquean otras rutas de respuesta al estrés dentro de las células cancerosas. La esperanza es que combinaciones bien elegidas, guiadas por marcadores genéticos, dificulten la fuga de los tumores a la vez que mantienen los efectos adversos manejables. Los autores también reclaman inhibidores de PARP de próxima generación más selectivos que preserven las células sanguíneas sanas, mejores herramientas para predecir quién se beneficiará y atención al coste y la disponibilidad de estos tratamientos en entornos con recursos limitados. En términos sencillos, los inhibidores de PARP han convertido una vulnerabilidad genética en algunos cánceres de mama en una oportunidad terapéutica real, pero el control duradero requerirá entender y bloquear las múltiples formas en que los tumores contraatacan.
Cita: Wang, W., Cai, C., Qin, S. et al. PARP inhibitors and breast cancer: from therapeutic breakthrough to resistance challenge. Exp Mol Med 58, 981–992 (2026). https://doi.org/10.1038/s12276-026-01673-8
Palabras clave: inhibidores de PARP, cáncer de mama, mutaciones BRCA, resistencia a fármacos, terapia dirigida