Clear Sky Science · nl
PARP-remmers en borstkanker: van therapeutische doorbraak naar het probleem van resistentie
Waarom dit belangrijk is voor patiënten en families
Borstkanker is nu de meest voorkomende kanker bij vrouwen wereldwijd, en veel mensen leven langer dankzij betere geneesmiddelen. Een relatief nieuwe klasse medicijnen, PARP-remmers genoemd, heeft nieuwe hoop geboden aan patiënten van wie de tumoren bepaalde genetische afwijkingen dragen. Dit artikel legt uit hoe deze middelen werken, waarom ze zo effectief kunnen zijn en hoe kankers ze na verloop van tijd weten te omzeilen. Inzicht hierin biedt zowel artsen als patiënten duidelijkere verwachtingen en wijst op toekomstige behandelingen die borstkanker langer onder controle kunnen houden.
Gerichte middelen die gebruikmaken van zwakke plekken van de kanker
Borstkanker is geen enkele ziekte, maar een verzameling subtypes die zich verschillend gedragen en maatwerkzorg vragen. Tumoren die hormoon- of HER2-signalen missen, zoals veel triple-negatieve borstkankers, zijn bijzonder agressief en moeilijk te behandelen. PARP-remmers werden ontwikkeld om tumoren aan te pakken die al moeite hebben met het repareren van hun DNA, vooral die met erfelijke of verworven veranderingen in de BRCA1- of BRCA2-genen. Door PARP-eiwitten te blokkeren, die normaal helpen dagelijkse DNA-schade te herstellen, duwen deze middelen al kwetsbare kankercellen voorbij hun grenzen, wat leidt tot celdood terwijl de meeste gezonde cellen gespaard blijven. Grote klinische trials zoals OlympiA en EMBRACA hebben aangetoond dat PARP-remmers bij geselecteerde patiënten de tijd vóór achteruitgang van de ziekte kunnen verlengen.
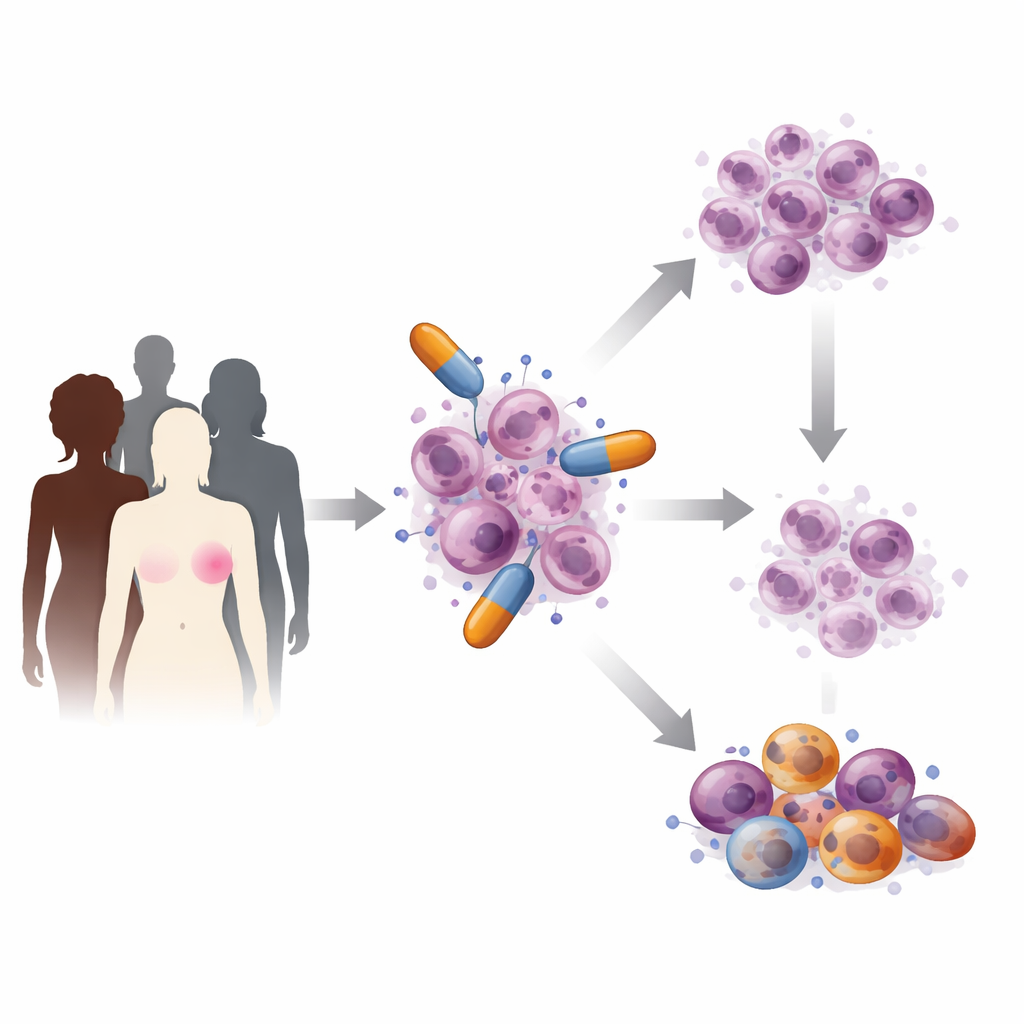
Hoe PARP-middelen kankercellen aanvallen
In elke cel wordt DNA voortdurend beschadigd en hersteld. PARP-eiwitten fungeren als eerstelijnsresponders bij bepaalde soorten breuken: ze roepen reparatieteams op en helpen bij het in goede banen leiden van DNA-replicatie. PARP-remmers schuiven in de actieve plek van deze eiwitten en blokkeren hun herstelactiviteit of zorgen ervoor dat ze stevig op gebroken DNA vast blijven zitten. Daardoor hopen kleine breuken zich op en botsen ze met het DNA-replicatiemechanisme van de cel, wat leidt tot ernstigere schade die cellen met defecte BRCA-genen niet kunnen repareren. Wetenschappers ontdekten ook dat deze middelen verstoringen veroorzaken bij het afmaken van nieuwe DNA-strengen, gaten creëren die later instorten tot gevaarlijke breuken, invloed hebben op hoe cellen belangrijke voedingsstoffen voor chemische reacties verwerken en zelfs immuunwaarschuwingssignalen kunnen opwekken die het afweersysteem helpen tumoren herkennen en aanvallen.
Bewijslast uit trials en dagelijkse praktijk
Verschillende PARP-remmers worden nu gebruikt of bestudeerd voor borstkanker. Olaparib en talazoparib zijn de belangrijkste opties voor patiënten met gevorderde HER2-negatieve ziekte en BRCA-mutaties, en zijn ook getest in eerdere stadia van kanker. Andere middelen uit deze familie, zoals niraparib, rucaparib, veliparib, fuzuloparib en pamiparib, worden in verschillende settings of regio’s onderzocht, soms in combinatie met chemotherapie. Hoewel veel trials duidelijke vertragingen in tumorprogressie rapporteren, kunnen overlevingsvoordelen variëren en blijven bijwerkingen zoals een laag aantal bloedcellen een punt van zorg. Het artikel merkt ook op dat gegevens uit de dagelijkse praktijk, buiten gecontroleerde trials, nog beperkt zijn, vooral voor nieuwere middelen en voor patiënten uit diverse achtergronden.
Hoe tumoren leren resistent te worden tegen PARP-behandeling
Ondanks vroege successen zien veel patiënten uiteindelijk dat hun kanker niet meer reageert op PARP-remmers. De review beschrijft verschillende slimme ontsnappingsroutes die tumorcellen gebruiken. Sommige herstellen het DNA-herstelvermogen door nieuwe mutaties te verwerven die de BRCA-functie herstellen of door genactiviteit weer aan te zetten via veranderingen in DNA-markering. Anderen beschermen het fragiele DNA-replicatiemechanisme zodat het niet instort onder stress, of passen aan hoe DNA-verpakkingsproteïnen, histonen genoemd, worden behandeld zodat hun chromosomen stabieler blijven. In sommige gevallen pompen kankercellen het medicijn gewoon efficiënter weg, waardoor de concentratie binnen de cel daalt. Deze gelaagde resistentiemechanismen helpen verklaren waarom responsen vaak vervagen en waarom hetzelfde middel bij verschillende patiënten anders kan werken.
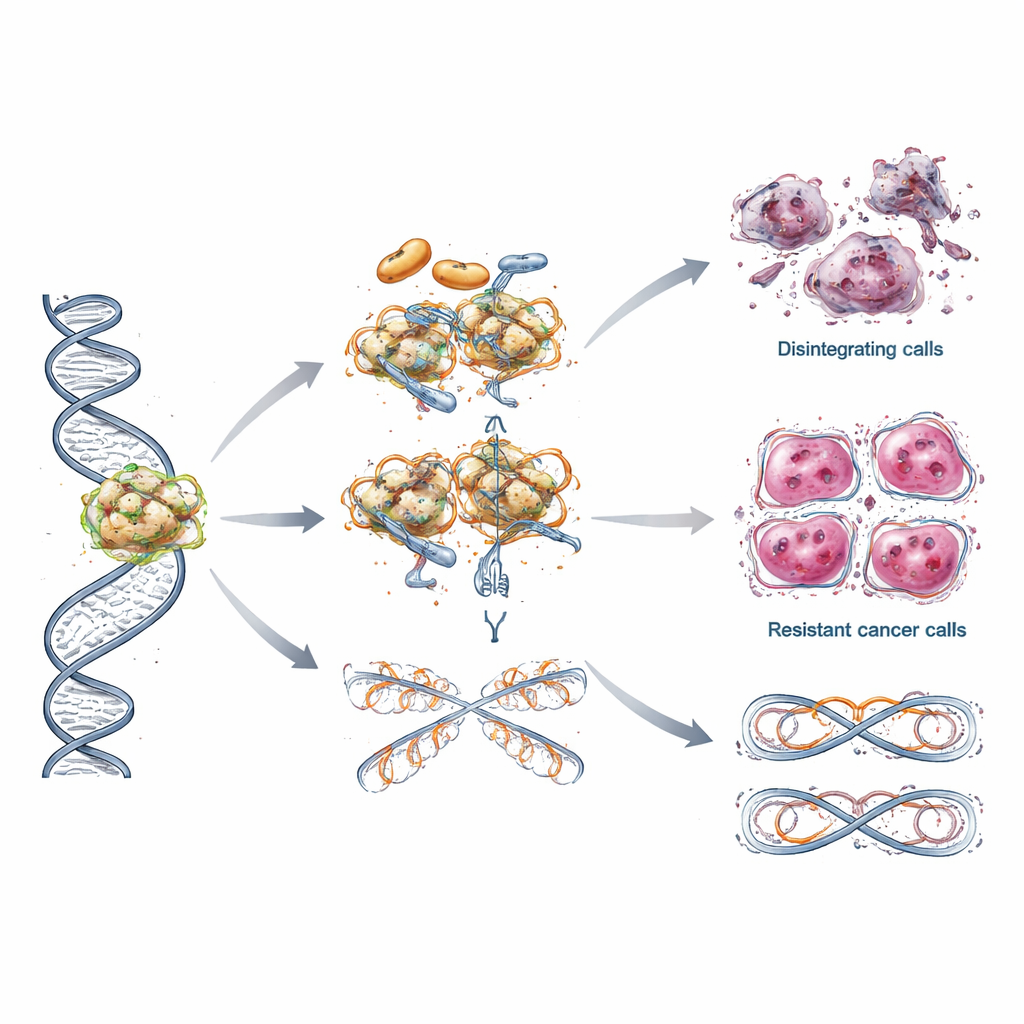
Volgende stappen: slim samenspel en bredere toegang
Om de resistentie voor te blijven, testen onderzoekers PARP-remmers samen met chemotherapie, immuuncheckpointremmers en middelen die andere stresstolerantieroutes in kankercellen blokkeren. De hoop is dat goed gekozen combinaties, gestuurd door genetische markers, het voor tumoren moeilijker maken te ontsnappen, terwijl bijwerkingen beheersbaar blijven. De auteurs pleiten ook voor selectieve PARP-middelen van de volgende generatie die gezonde bloedcellen sparen, betere tools om te voorspellen wie baat heeft, en aandacht voor kosten en beschikbaarheid van deze behandelingen in gebieden met beperkte middelen. Simpel gezegd hebben PARP-remmers een genetische kwetsbaarheid in sommige borstkankers veranderd in een reële therapeutische kans, maar langdurige controle vereist inzicht in en het blokkeren van de vele manieren waarop tumoren terugvechten.
Bronvermelding: Wang, W., Cai, C., Qin, S. et al. PARP inhibitors and breast cancer: from therapeutic breakthrough to resistance challenge. Exp Mol Med 58, 981–992 (2026). https://doi.org/10.1038/s12276-026-01673-8
Trefwoorden: PARP-remmers, borstkanker, BRCA-mutaties, medicatieresistentie, gerichte therapie