Clear Sky Science · de
PARP-Inhibitor und Brustkrebs: vom therapeutischen Durchbruch zur Herausforderung durch Resistenz
Warum das für Patienten und Familien wichtig ist
Brustkrebs ist heute weltweit die häufigste Krebserkrankung bei Frauen, und dank besserer Therapien leben viele Betroffene länger. Eine neuere Medikamentenklasse, die sogenannten PARP-Inhibitoren, hat Patienten mit bestimmten genetischen Defekten neue Hoffnung gegeben. Dieser Artikel erläutert, wie diese Wirkstoffe funktionieren, warum sie so wirksam sein können und wie Tumoren es mit der Zeit schaffen, sie zu umgehen. Dieses Verständnis gibt Ärzten und Patientinnen/Patienten klarere Erwartungen und weist auf künftige Behandlungsansätze hin, die Brustkrebs länger unter Kontrolle halten könnten.
Zielgerichtete Medikamente, die Schwachstellen des Krebses ausnutzen
Brustkrebs ist keine einzelne Krankheit, sondern eine Sammlung von Subtypen, die sich unterschiedlich verhalten und eine angepasste Versorgung brauchen. Tumoren ohne Hormon- oder HER2-Signale, wie viele triple-negativen Brustkrebserkrankungen, sind besonders aggressiv und schwer zu behandeln. PARP-Inhibitoren wurden entwickelt, um Tumoren anzugreifen, die bereits Probleme mit der DNA-Reparatur haben, insbesondere solche mit erblichen oder erworbenen Veränderungen in den BRCA1- oder BRCA2-Genen. Indem sie PARP-Proteine blockieren, die normalerweise alltägliche DNA-Schäden reparieren, treiben diese Medikamente bereits verwundbare Krebszellen über ihre Belastungsgrenze und führen zu ihrem Tod, während die meisten gesunden Zellen verschont bleiben. Große klinische Studien wie OlympiA und EMBRACA haben gezeigt, dass PARP-Inhibitoren bei ausgewählten Patientinnen und Patienten die Zeit bis zum Nachlassen der Erkrankung verlängern können.
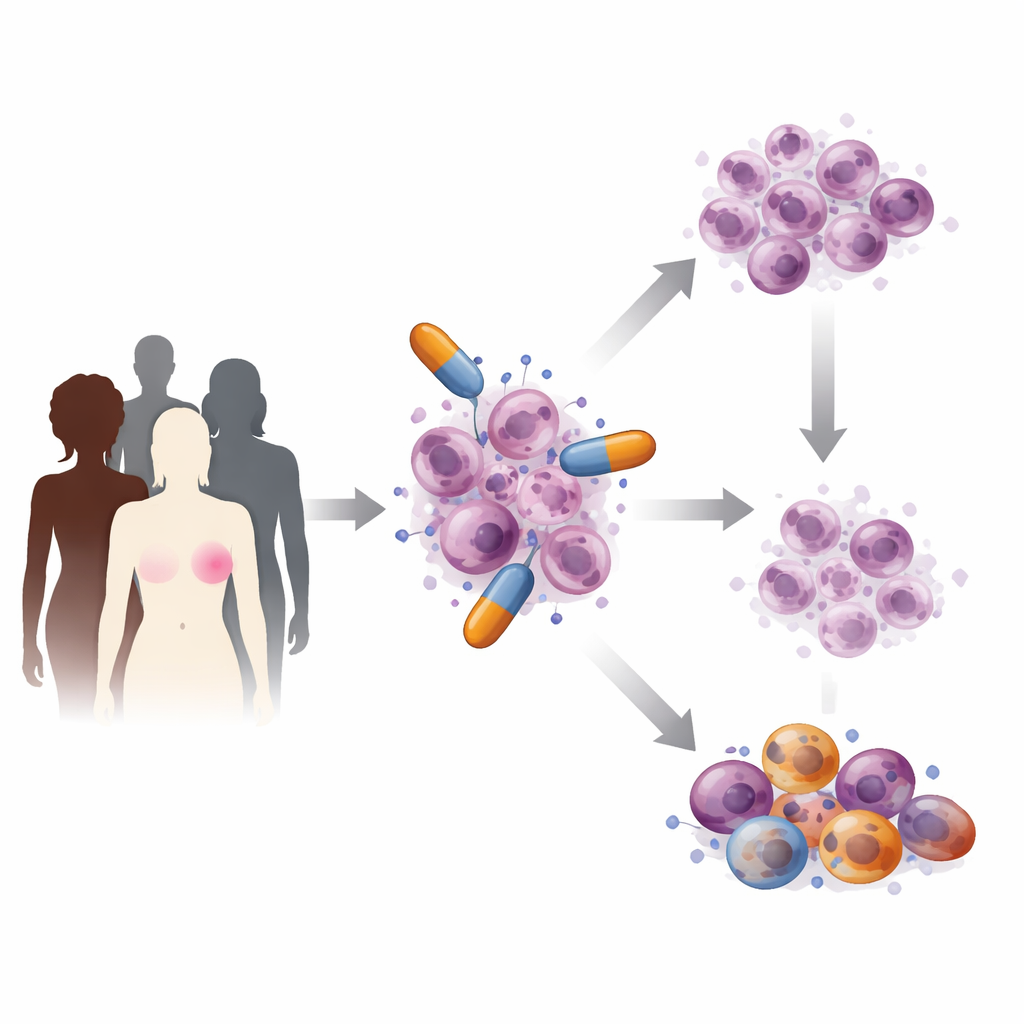
Wie PARP-Wirkstoffe Krebszellen angreifen
In jeder Zelle wird DNA ständig eingerissen und repariert. PARP-Proteine fungieren als Ersthelfer bei bestimmten Bruchtypen, sie rekrutieren Reparaturmannschaften und helfen, die DNA-Vervielfältigung im Takt zu halten. PARP-Inhibitoren schlüpfen in das aktive Zentrum dieser Proteine und blockieren entweder deren Reparaturaktivität oder führen dazu, dass sie fest an gebrochene DNA gebunden bleiben. Dadurch häufen sich kleine Brüche an und kollidieren mit der DNA-Replikationsmaschinerie, was zu ernsteren Schäden führt, die Zellen mit fehlerhaften BRCA-Genen nicht beheben können. Forscher haben außerdem entdeckt, dass diese Medikamente die Fertigstellung neuer DNA-Stränge stören, Lücken erzeugen, die später in gefährliche Brüche zusammenfallen, den Umgang der Zellen mit wichtigen Nährstoffen für chemische Reaktionen verändern und sogar Immunwarnsignale auslösen können, die dem Immunsystem helfen, Tumoren zu erkennen und anzugreifen.
Erkenntnisse aus Studien und der Praxis
Mehrere PARP-Inhibitoren werden inzwischen beim Brustkrebs eingesetzt oder untersucht. Olaparib und Talazoparib sind die Hauptoptionen für Patientinnen und Patienten mit fortgeschrittener HER2-negativer Erkrankung und BRCA-Mutationen und wurden auch in früheren Krankheitsstadien geprüft. Weitere Wirkstoffe dieser Klasse, wie Niraparib, Rucaparib, Veliparib, Fuzuloparib und Pamiparib, werden in verschiedenen Settings oder Regionen erforscht, teils in Kombination mit Chemotherapie. Während viele Studien eine deutliche Verzögerung des Tumorwachstums berichten, können Gesamtüberlebensvorteile variieren, und Nebenwirkungen wie niedrige Blutwerte bleiben ein Thema. Der Artikel weist auch darauf hin, dass Daten aus der routinemäßigen Versorgung außerhalb kontrollierter Studien noch begrenzt sind, insbesondere zu neueren Substanzen und Patientengruppen mit unterschiedlichem Hintergrund.
Wie Tumoren lernen, PARP-Behandlung zu widerstehen
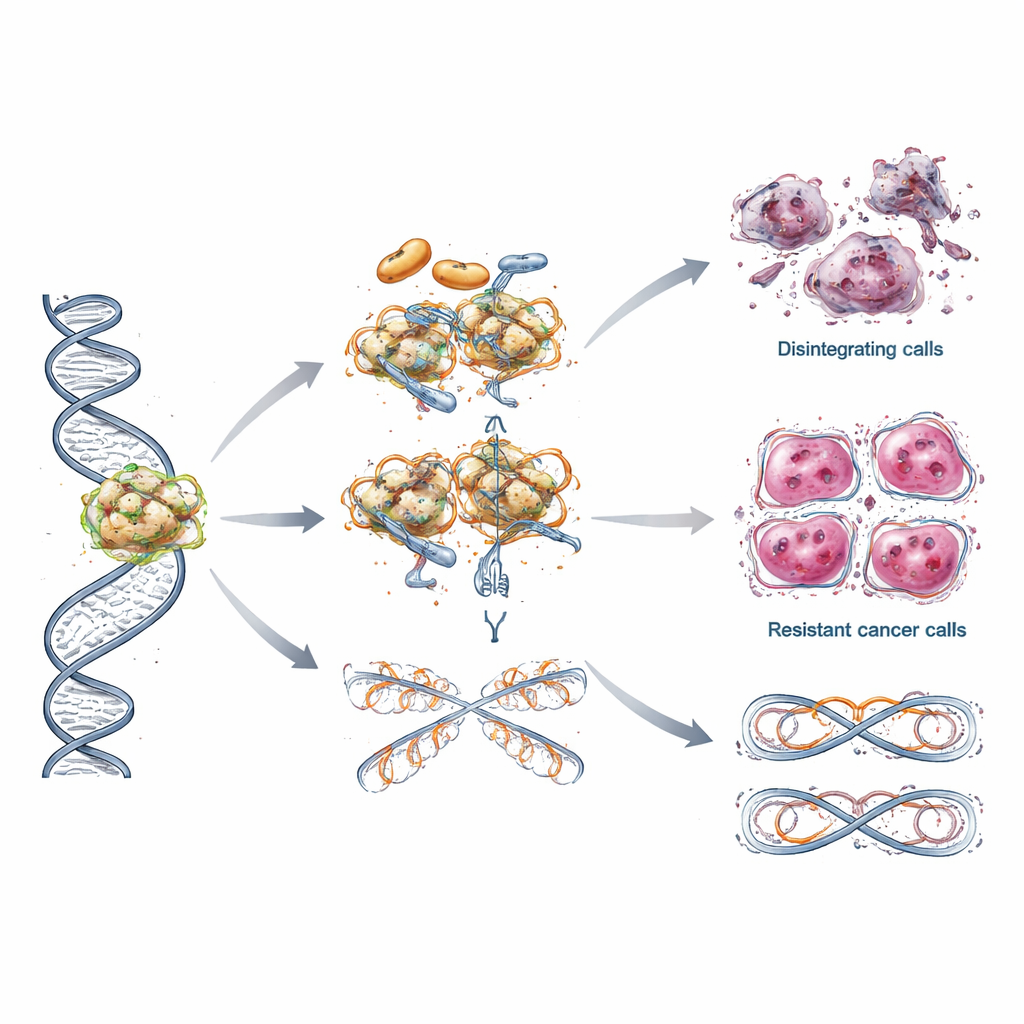
Trotz anfänglicher Erfolge sprechen viele Patientinnen und Patienten mit der Zeit nicht mehr auf PARP-Inhibitoren an. Die Übersichtsarbeit beschreibt mehrere clevere Fluchtwege, die Tumorzellen nutzen. Manche gewinnen die Fähigkeit zur DNA-Reparatur zurück, indem sie neue Mutationen erwerben, die die BRCA-Funktion wiederherstellen, oder indem sie Genaktivität durch Änderungen an der DNA-Markierung erneut einschalten. Andere schützen die fragile Replikationsmaschinerie so, dass sie unter Stress nicht zusammenbricht, oder passen den Umgang mit DNA-Verpackungsproteinen, den Histonen, an, sodass ihre Chromosomen stabiler bleiben. In einigen Fällen pumpen Krebszellen das Medikament einfach effizienter aus der Zelle, wodurch dessen intrazelluläre Konzentration sinkt. Diese vielschichtigen Resistenztricks helfen zu erklären, warum Ansprechen oft nachlässt und warum dasselbe Medikament bei verschiedenen Patientinnen und Patienten unterschiedlich wirkt.
Nächste Schritte: klügere Kombinationen und breiterer Zugang
Um der Resistenz einen Schritt voraus zu sein, prüfen Forschende PARP-Inhibitoren in Kombination mit Chemotherapie, Immun-Checkpoint-Inhibitoren und Medikamenten, die andere Stressantwortwege in Krebszellen blockieren. Die Hoffnung ist, dass gut gewählte Kombinationen, gesteuert durch genetische Marker, es Tumoren schwerer machen, zu entkommen, und gleichzeitig die Nebenwirkungen beherrschbar bleiben. Die Autorinnen und Autoren fordern zudem selektivere PARP-Wirkstoffe der nächsten Generation, die gesunde Blutzellen schonen, bessere Werkzeuge, um vorherzusagen, wer profitieren wird, sowie Aufmerksamkeit für Kosten und Verfügbarkeit dieser Therapien in ressourcenarmen Regionen. Kurz gesagt: PARP-Inhibitoren haben eine genetische Verwundbarkeit mancher Brustkrebse in eine reale therapeutische Chance verwandelt, aber dauerhafte Kontrolle erfordert das Verständnis und das Blockieren der vielen Wege, über die Tumoren zurückschlagen.
Zitation: Wang, W., Cai, C., Qin, S. et al. PARP inhibitors and breast cancer: from therapeutic breakthrough to resistance challenge. Exp Mol Med 58, 981–992 (2026). https://doi.org/10.1038/s12276-026-01673-8
Schlüsselwörter: PARP-Inhibitoren, Brustkrebs, BRCA-Mutationen, Arzneimittelresistenz, zielgerichtete Therapie