Clear Sky Science · sv
PARP‑hämmare och bröstcancer: från terapeutiskt genombrott till resistensutmaning
Varför detta spelar roll för patienter och familjer
Bröstcancer är nu den vanligaste cancerformen bland kvinnor globalt, och många lever längre tack vare bättre läkemedel. En nyare läkemedelsgrupp, kallad PARP‑hämmare, har gett nytt hopp åt patienter vars tumörer bär vissa genetiska fel. Denna artikel förklarar hur dessa läkemedel fungerar, varför de kan vara så effektiva och hur cancer över tiden kan lista ut sätt att kringgå dem. Att förstå detta ger både läkare och patienter klarare förväntningar och pekar mot framtida behandlingar som kan hålla bröstcancer under kontroll längre.
Målinriktade läkemedel som utnyttjar cancerns svaga punkter
Bröstcancer är inte en enda sjukdom, utan en samling undergrupper som beter sig olika och kräver skräddarsydd vård. Tumörer som saknar hormon‑ eller HER2‑signaler, såsom många trippelnegativa bröstcancerformer, är särskilt aggressiva och svåra att behandla. PARP‑hämmare utvecklades för att rikta in sig på tumörer som redan har svårt att reparera sitt DNA, framförallt de med ärftliga eller förvärvade förändringar i BRCA1 eller BRCA2‑generna. Genom att blockera PARP‑proteiner, som normalt hjälper till att laga vardagliga DNA‑skador, pressar dessa läkemedel redan sårbara cancerceller över gränsen så att de dör, samtidigt som de flesta friska celler skonas. Stora kliniska studier som OlympiA och EMBRACA har visat att PARP‑hämmare kan förlänga tiden innan sjukdomen försämras hos utvalda patienter.
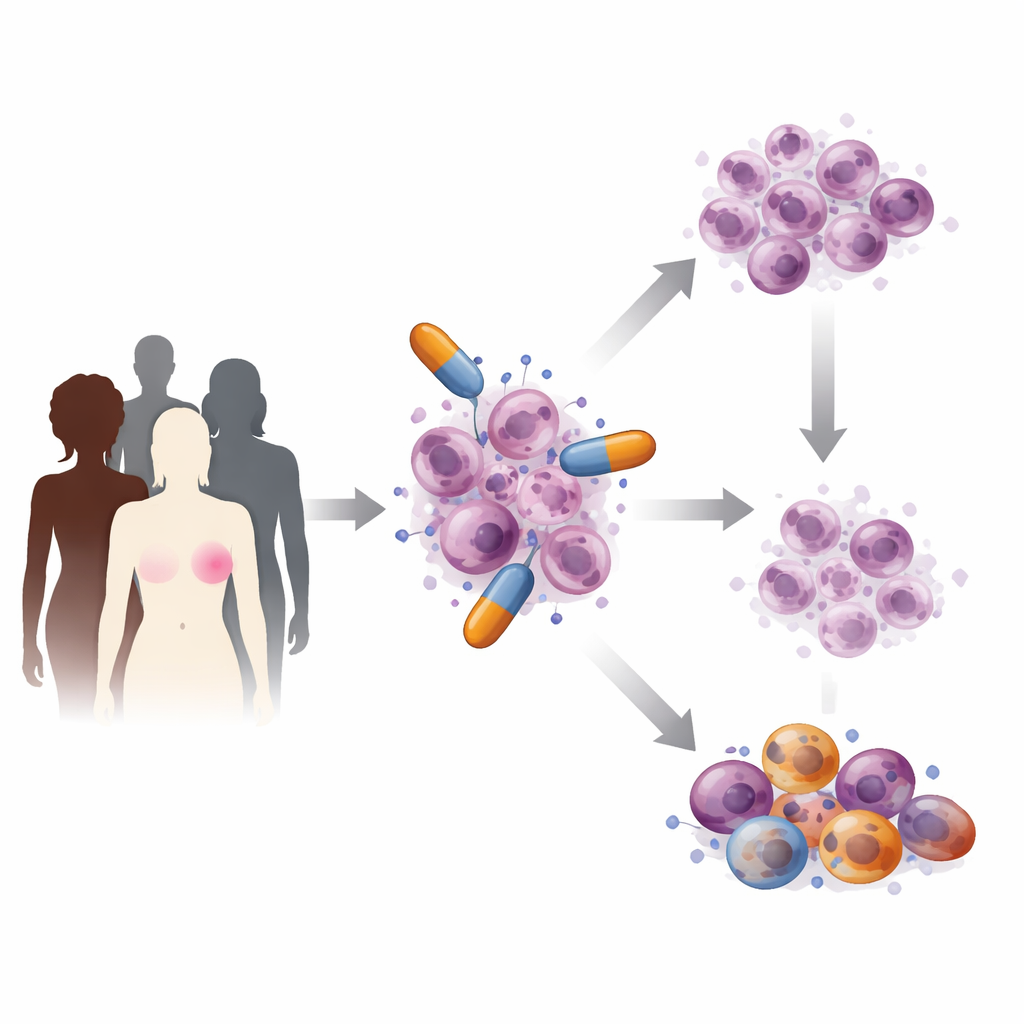
Hur PARP‑läkemedel angriper cancerceller
Inne i varje cell blir DNA ständigt skadat och reparerat. PARP‑proteiner fungerar som första insatspersonal vid vissa typer av brott, de kallar in reparationslag och hjälper till att hålla DNA‑kopieringen på rätt spår. PARP‑hämmare smyger in i dessa proteiners aktiva yta och blockerar antingen deras reparationsaktivitet eller gör så att de fastnar tätt på brutet DNA. Som en följd ackumuleras små brott som kolliderar med cellens DNA‑kopieringsmaskineri, vilket leder till allvarligare skador som celler med defekta BRCA‑gener inte kan laga. Forskare har också upptäckt att dessa läkemedel stör hur nya DNA‑strängar avslutas, skapar luckor som senare kollapsar till farliga brott, påverkar hur celler hanterar viktiga näringsämnen för kemiska reaktioner och till och med väcker immunologiska larm som kan hjälpa kroppens försvar att identifiera och angripa tumörer.
Bevis från studier och vardaglig behandling
Flera PARP‑hämmare används nu eller utreds för bröstcancer. Olaparib och talazoparib är huvudalternativen för patienter med avancerad HER2‑negativ sjukdom och BRCA‑mutationer, och har också prövats i tidigare stadier av cancer. Andra läkemedel i denna familj, såsom niraparib, rucaparib, veliparib, fuzuloparib och pamiparib, undersöks i olika sammanhang eller regioner, ibland i kombination med cytostatika. Medan många prövningar rapporterar tydliga förseningar i tumörtillväxt, kan vinster i total överlevnad variera, och biverkningar som låga blodvärden kvarstår som en oro. Artikeln noterar också att data från vardagligt kliniskt bruk, utöver kontrollerade studier, fortfarande är begränsade, särskilt för nyare preparat och för patienter från skiftande bakgrunder.
Hur tumörer lär sig att motstå PARP‑behandling
Trots tidiga framgångar slutar många patienters cancer till sist att svara på PARP‑hämmare. Översikten beskriver flera smarta flyktvägar som tumörceller använder. Vissa återfår DNA‑reparationsförmåga genom att få nya mutationer som återställer BRCA‑funktionen eller genom att återaktivera genuttryck via förändringar i DNA‑märkning. Andra skyddar det känsliga DNA‑kopieringsmaskineriet så att det inte kollapsar under stress, eller anpassar hur DNA‑paketeringsproteiner, kallade histoner, hanteras så att deras kromosomer förblir stabilare. I vissa fall pumpar cancerceller helt enkelt ut läkemedlet mer effektivt och sänker dess koncentration inne i cellen. Dessa lager av resistensmekanismer hjälper till att förklara varför svaren ofta avtar och varför samma läkemedel kan fungera olika från patient till patient.
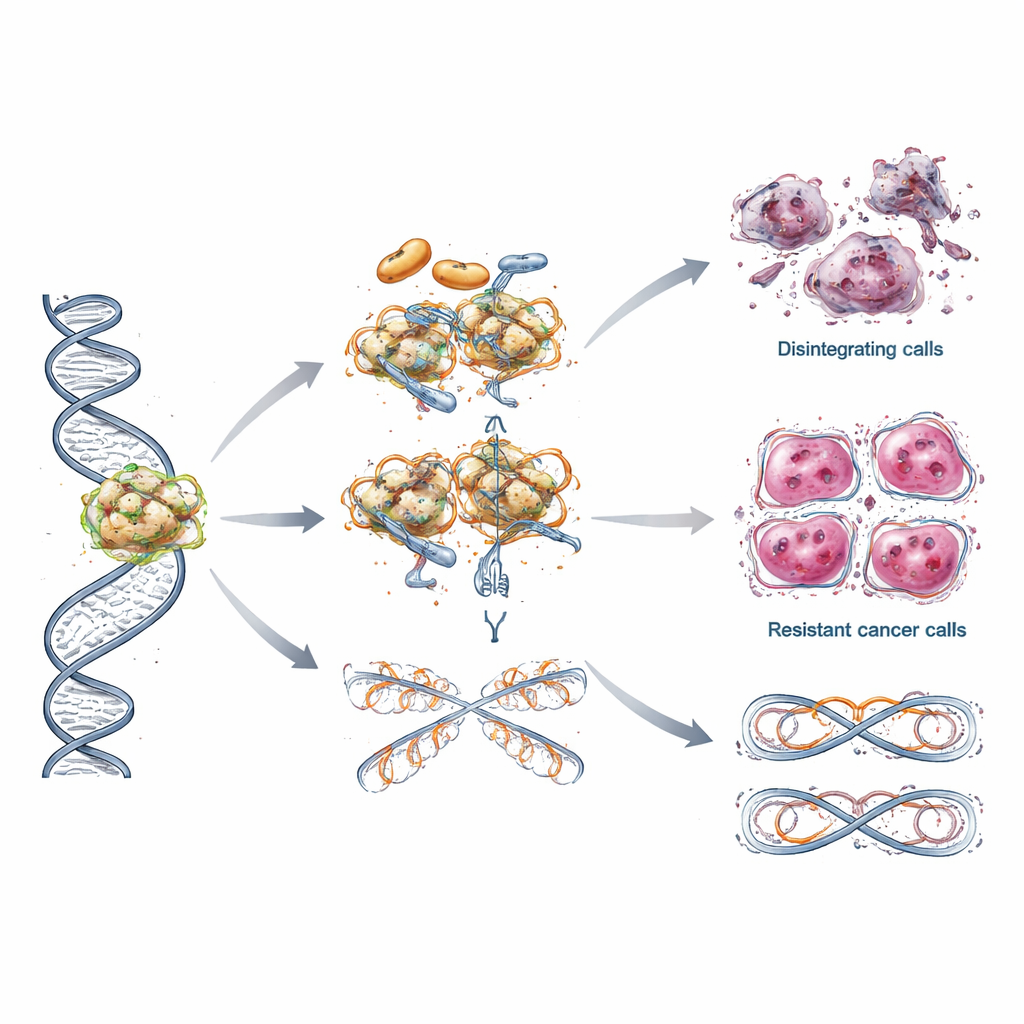
Nästa steg: smartare kombinationer och bredare tillgång
För att ligga steget före resistens testar forskare PARP‑hämmare tillsammans med cytostatika, immuncheckpoint‑läkemedel och preparat som blockerar andra stresstoleransvägar inne i cancerceller. Förhoppningen är att väl valda kombinationer, styrda av genetiska markörer, ska göra det svårare för tumörer att fly samtidigt som biverkningarna hålls hanterbara. Författarna efterlyser också mer selektiva nästa generations PARP‑läkemedel som skonar friska blodceller, bättre verktyg för att förutsäga vilka som får nytta, samt uppmärksamhet på kostnad och tillgänglighet för dessa behandlingar i resurssvaga miljöer. Enkelt uttryckt har PARP‑hämmare förvandlat en genetisk sårbarhet i vissa bröstcancerformer till en verklig terapeutisk möjlighet, men långvarig kontroll kräver att man förstår och blockerar de många sätt tumörer slåss tillbaka på.
Citering: Wang, W., Cai, C., Qin, S. et al. PARP inhibitors and breast cancer: from therapeutic breakthrough to resistance challenge. Exp Mol Med 58, 981–992 (2026). https://doi.org/10.1038/s12276-026-01673-8
Nyckelord: PARP‑hämmare, bröstcancer, BRCA‑mutationer, läkemedelsresistens, målinriktad terapi