Clear Sky Science · fr
Inhibiteurs de PARP et cancer du sein : du progrès thérapeutique au défi de la résistance
Pourquoi cela compte pour les patientes et leurs familles
Le cancer du sein est aujourd’hui le cancer le plus fréquent chez les femmes dans le monde, et de nombreuses personnes vivent plus longtemps grâce à de meilleurs traitements. Une classe de médicaments plus récente, les inhibiteurs de PARP, a apporté un nouvel espoir aux patientes dont les tumeurs présentent certains défauts génétiques. Cet article explique comment ces médicaments agissent, pourquoi ils peuvent être si efficaces, et comment les cancers finissent par leur échapper au fil du temps. Comprendre ces mécanismes permet aux médecins et aux patientes d’avoir des attentes plus claires et oriente vers des traitements futurs susceptibles de contrôler le cancer du sein plus longtemps.
Médicaments ciblés qui exploitent les points faibles du cancer
Le cancer du sein n’est pas une maladie unique, mais un ensemble de sous-types qui se comportent différemment et nécessitent des soins adaptés. Les tumeurs dépourvues de récepteurs hormonaux ou de signalisation HER2, comme de nombreux cancers du sein triple négatifs, sont particulièrement agressives et difficiles à traiter. Les inhibiteurs de PARP ont été développés pour cibler les tumeurs déjà déficientes dans la réparation de l’ADN, en particulier celles portant des altérations héréditaires ou acquises des gènes BRCA1 ou BRCA2. En bloquant les protéines PARP, qui aident normalement à réparer les dommages quotidiens de l’ADN, ces médicaments poussent des cellules cancéreuses déjà fragiles au-delà de leur capacité, entraînant leur mort tout en épargnant la plupart des cellules saines. De grands essais cliniques, comme OlympiA et EMBRACA, ont montré que les inhibiteurs de PARP peuvent prolonger le délai avant l’aggravation de la maladie chez des patientes sélectionnées.
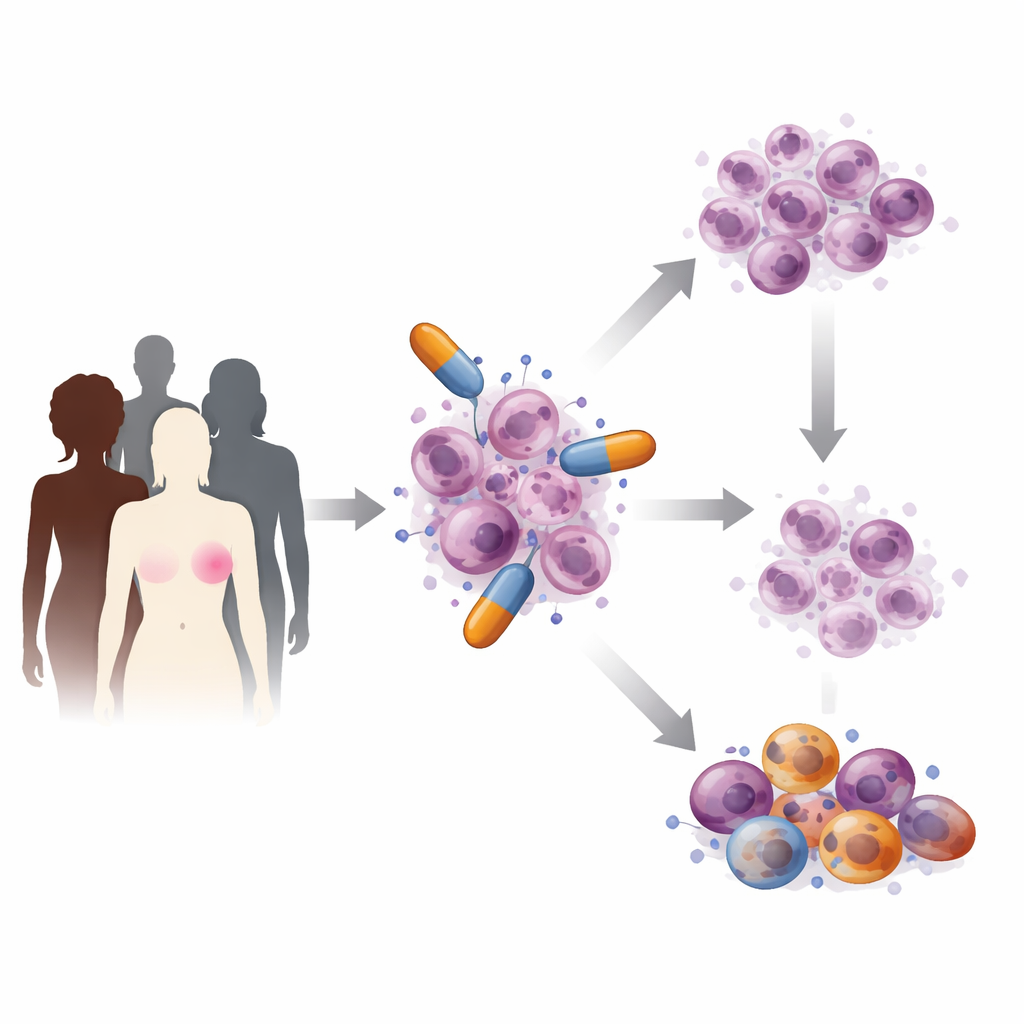
Comment les médicaments PARP attaquent les cellules cancéreuses
À l’intérieur de chaque cellule, l’ADN subit en permanence des coupures et des réparations. Les protéines PARP jouent le rôle de premiers intervenants pour certains types de cassures, recrutant les équipes de réparation et contribuant à maintenir la copie de l’ADN. Les inhibiteurs de PARP se glissent dans le site actif de ces protéines et bloquent soit leur activité réparatrice, soit les font rester liés de façon rigide à l’ADN endommagé. En conséquence, de petites cassures s’accumulent et entrent en collision avec la machinerie de réplication de l’ADN, provoquant des lésions plus graves que les cellules déficientes en BRCA ne peuvent pas réparer. Les chercheurs ont également découvert que ces médicaments perturbent la finition des nouveaux brins d’ADN, créent des lacunes qui s’effondrent ensuite en cassures dangereuses, modifient la gestion par la cellule des cofacteurs nécessaires aux réactions chimiques, et peuvent même déclencher des signaux immunitaires qui aident les défenses de l’organisme à reconnaître et attaquer les tumeurs.
Preuves issues des essais et du traitement en pratique courante
Plusieurs inhibiteurs de PARP sont aujourd’hui utilisés ou étudiés dans le cancer du sein. L’olaparib et le talazoparib sont les principales options pour les patientes ayant une maladie avancée HER2 négative et des mutations BRCA, et ont également été testés à des stades précoces du cancer. D’autres médicaments de cette famille, tels que le niraparib, le rucaparib, le véliparib, le fuzuloparib et le pamiparib, sont explorés dans différents contextes ou régions, parfois en combinaison avec une chimiothérapie. Si de nombreux essais rapportent un délai clair de progression tumorale, les bénéfices en termes de survie globale peuvent varier, et des effets indésirables comme la baisse des cellules sanguines restent préoccupants. L’article souligne également que les données provenant de la pratique quotidienne, au-delà des essais contrôlés, restent limitées, en particulier pour les agents plus récents et pour des patientes issues de milieux divers.
Comment les tumeurs apprennent à résister au traitement par PARP
Malgré des succès initiaux, de nombreuses patientes voient finalement leur cancer cesser de répondre aux inhibiteurs de PARP. La revue décrit plusieurs voies d’échappement ingénieuses utilisées par les cellules tumorales. Certaines retrouvent la capacité de réparer l’ADN en acquérant de nouvelles mutations qui restaurent la fonction BRCA ou en réactivant l’expression génique via des modifications de marquage de l’ADN. D’autres protègent la fragile machinerie de réplication de l’ADN pour éviter son effondrement sous stress, ou ajustent la manière dont les protéines de conditionnement de l’ADN, appelées histones, sont gérées afin de stabiliser leurs chromosomes. Dans certains cas, les cellules cancéreuses expulsent simplement le médicament plus efficacement, réduisant sa concentration intracellulaire. Ces stratagèmes de résistance superposés expliquent en partie pourquoi les réponses s’estompent souvent et pourquoi un même médicament peut fonctionner différemment d’une patiente à l’autre.
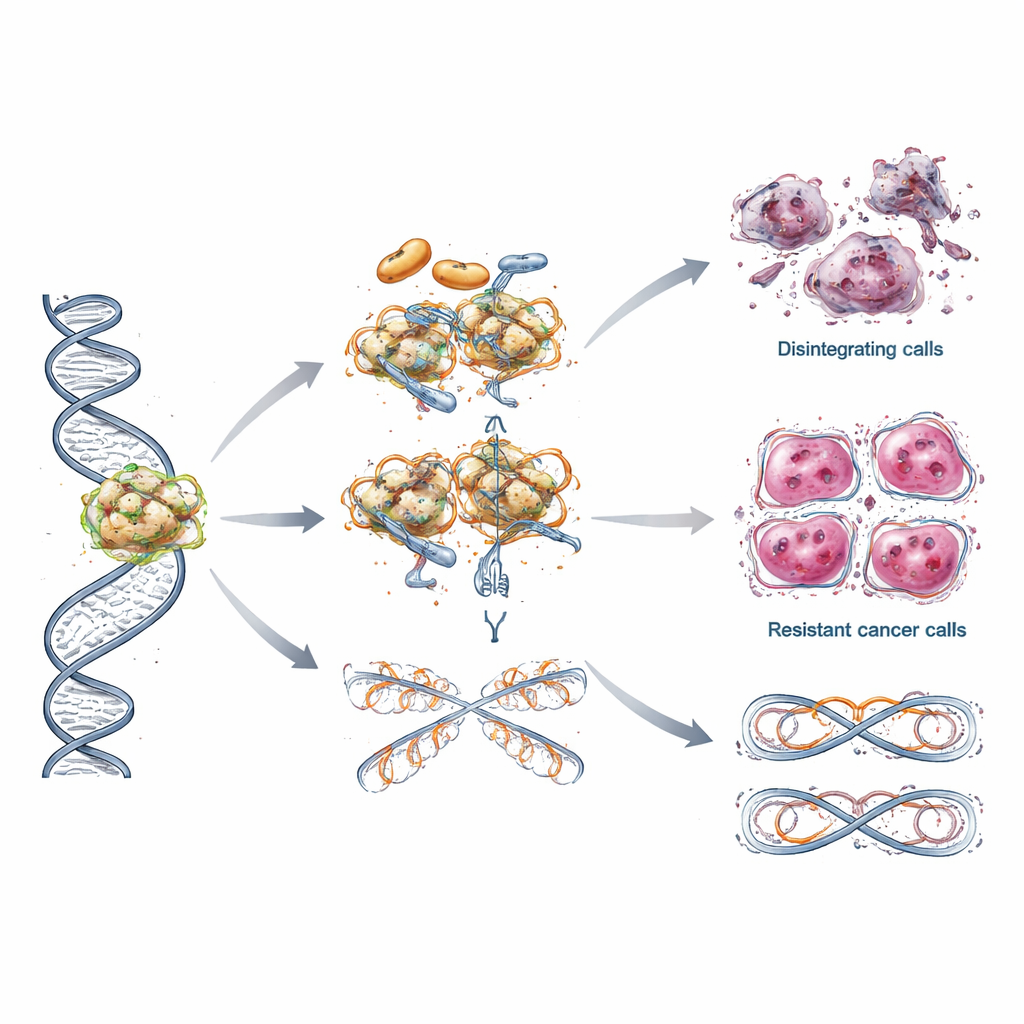
Prochaines étapes : combinaisons plus intelligentes et accès élargi
Pour garder une longueur d’avance sur la résistance, les chercheurs testent les inhibiteurs de PARP en association avec la chimiothérapie, les inhibiteurs de points de contrôle immunitaires et des médicaments qui bloquent d’autres voies de réponse au stress dans les cellules cancéreuses. L’espoir est que des associations bien choisies, guidées par des marqueurs génétiques, rendent plus difficile l’évasion des tumeurs tout en maintenant des effets secondaires maîtrisables. Les auteurs demandent également des inhibiteurs de PARP de nouvelle génération plus sélectifs qui préservent les cellules sanguines saines, de meilleurs outils pour prédire qui bénéficiera du traitement, et une attention au coût et à la disponibilité de ces traitements dans les milieux à ressources limitées. En termes simples, les inhibiteurs de PARP ont transformé une vulnérabilité génétique de certains cancers du sein en une véritable opportunité thérapeutique, mais un contrôle durable exigera de comprendre et de bloquer les nombreux mécanismes par lesquels les tumeurs se défendent.
Citation: Wang, W., Cai, C., Qin, S. et al. PARP inhibitors and breast cancer: from therapeutic breakthrough to resistance challenge. Exp Mol Med 58, 981–992 (2026). https://doi.org/10.1038/s12276-026-01673-8
Mots-clés: inhibiteurs de PARP, cancer du sein, mutations BRCA, résistance aux médicaments, thérapie ciblée