Clear Sky Science · pt
Inibidores de PARP e câncer de mama: da descoberta terapêutica ao desafio da resistência
Por que isto importa para pacientes e famílias
O câncer de mama é hoje o câncer mais comum entre mulheres no mundo, e muitas pessoas estão vivendo mais graças a medicamentos melhores. Uma classe mais recente de remédios, chamada inibidores de PARP, trouxe nova esperança a pacientes cujos tumores carregam certas falhas genéticas. Este artigo explica como esses medicamentos funcionam, por que podem ser tão eficazes e como os cânceres conseguem driblar esses fármacos ao longo do tempo. Compreender isso fornece tanto aos médicos quanto aos pacientes expectativas mais claras e aponta para tratamentos futuros que podem manter o câncer de mama sob controle por mais tempo.
Fármacos direcionados que exploram pontos fracos do câncer
O câncer de mama não é uma única doença, mas um conjunto de subtipos que se comportam de formas diferentes e exigem cuidados personalizados. Tumores que não expressam sinais hormonais nem HER2, como muitos carcinomas triplo negativos, são especialmente agressivos e difíceis de tratar. Os inibidores de PARP foram desenvolvidos para atingir tumores que já têm dificuldade em reparar seu DNA, especialmente aqueles com alterações herdadas ou adquiridas nos genes BRCA1 ou BRCA2. Ao bloquear as proteínas PARP, que normalmente ajudam a consertar danos cotidianos do DNA, esses fármacos levam células cancerosas já vulneráveis além de seu limite, resultando em morte celular enquanto poupam a maioria das células saudáveis. Grandes ensaios clínicos como OlympiA e EMBRACA mostraram que os inibidores de PARP podem prolongar o tempo até a progressão da doença em pacientes selecionados.
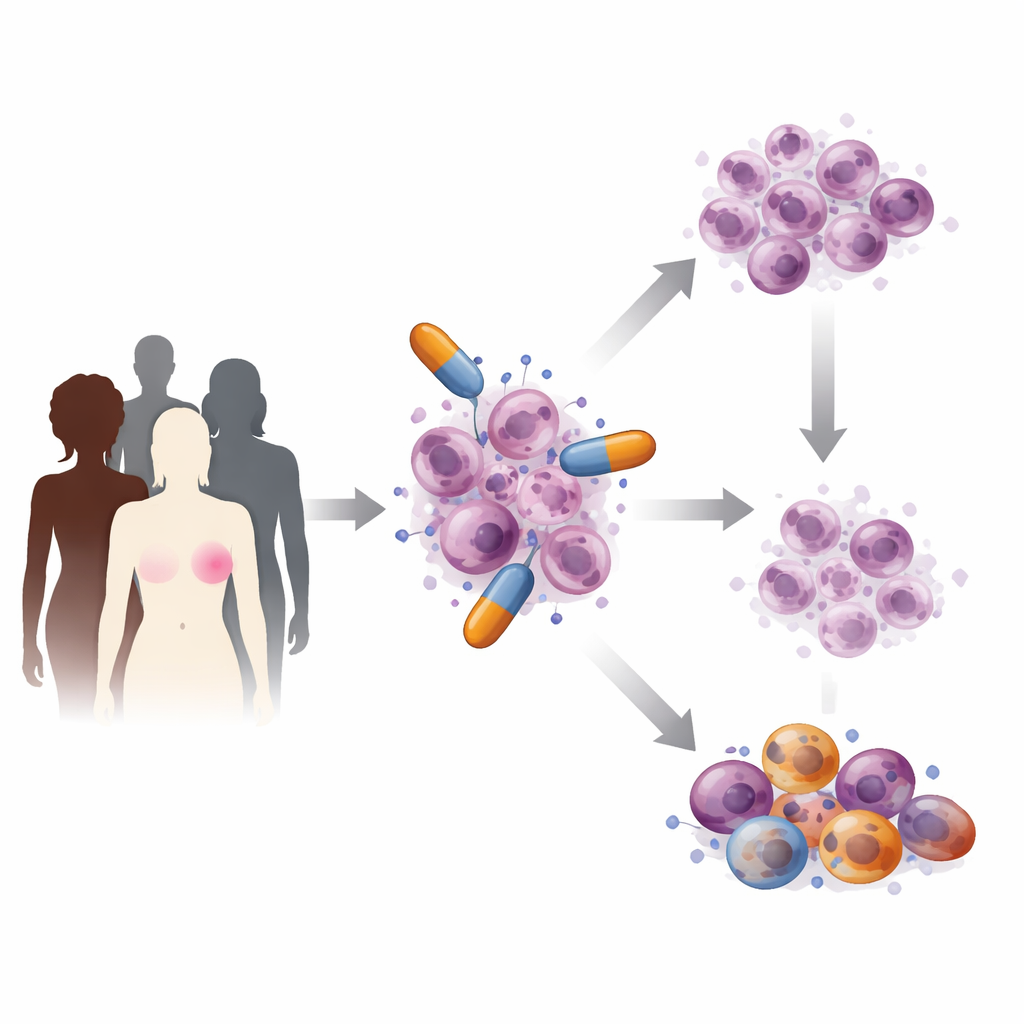
Como os fármacos PARP atacam as células cancerosas
Dentro de cada célula, o DNA é constantemente lesado e reparado. As proteínas PARP atuam como socorristas iniciais de certos tipos de quebras, recrutando equipes de reparo e ajudando a manter a replicação do DNA em ordem. Os inibidores de PARP se encaixam no sítio ativo dessas proteínas e ou bloqueiam sua atividade de reparo ou as fazem prender-se firmemente ao DNA quebrado. Como resultado, pequenas quebras se acumulam e colidem com a maquinaria de cópia do DNA da célula, levando a danos mais severos que células com genes BRCA defeituosos não conseguem reparar. Cientistas também descobriram que esses fármacos perturbam o término das novas fitas de DNA, criam lacunas que mais tarde colapsam em quebras perigosas, alteram o manejo de nutrientes essenciais para reações químicas e até desencadeiam sinais de alarme imune que podem ajudar as defesas do corpo a reconhecer e atacar os tumores.
Evidências de ensaios e do tratamento no mundo real
Vários inibidores de PARP estão agora em uso ou em estudo para câncer de mama. Olaparibe e talazoparibe são as principais opções para pacientes com doença avançada HER2 negativa e mutações BRCA, e também foram testados em estágios mais precoces do câncer. Outros fármacos dessa família, como niraparibe, rucaparibe, veliparibe, fuzuloparibe e pamiparibe, estão sendo explorados em diferentes contextos ou regiões, às vezes em combinação com quimioterapia. Embora muitos ensaios relatem atrasos claros no crescimento tumoral, os benefícios em sobrevida global podem variar, e efeitos colaterais como queda de células sanguíneas permanecem uma preocupação. O artigo também observa que os dados da prática clínica cotidiana, além dos ensaios controlados, ainda são limitados, especialmente para agentes mais novos e para pacientes de origens diversas.
Como os tumores aprendem a resistir ao tratamento com PARP
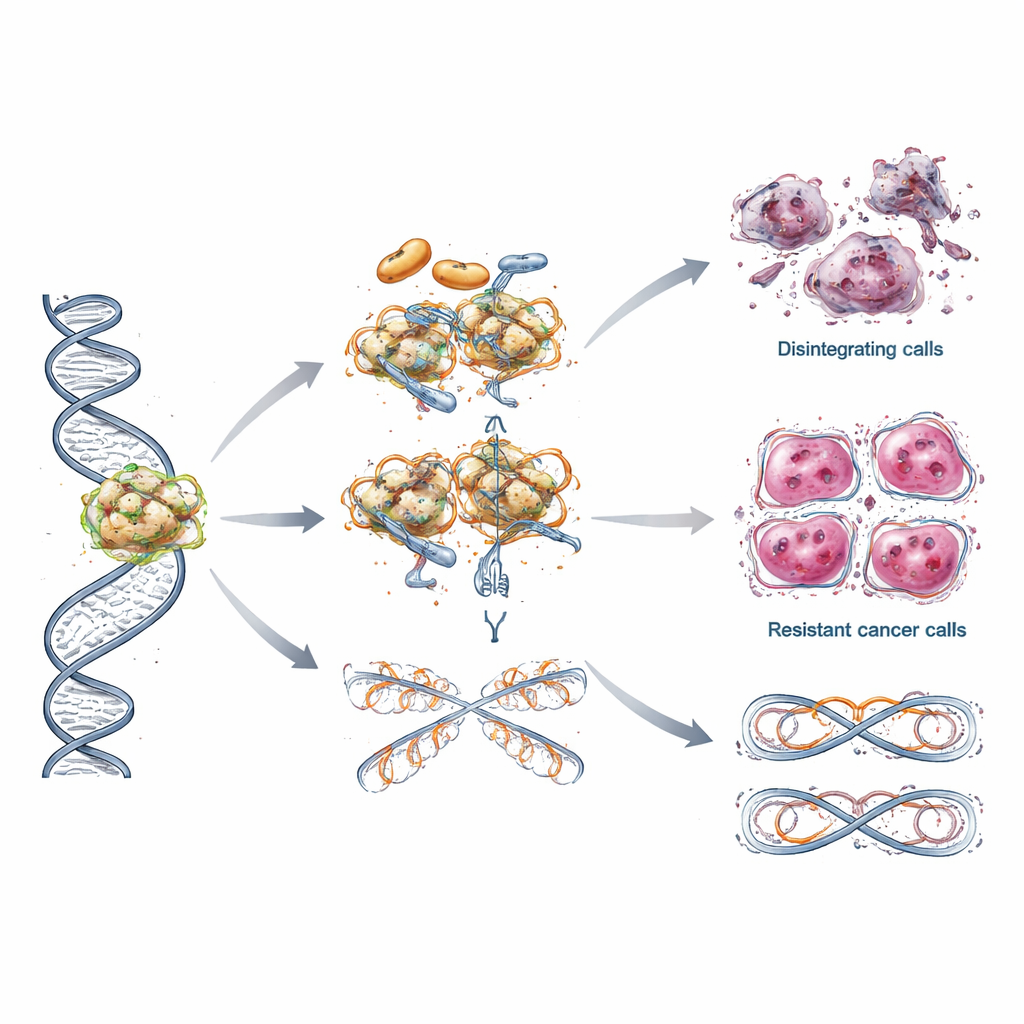
Apesar do sucesso inicial, muitos pacientes eventualmente veem seu câncer deixar de responder aos inibidores de PARP. A revisão descreve várias rotas de escape engenhosas usadas pelas células tumorais. Algumas recuperam a capacidade de reparar DNA adquirindo novas mutações que restauram a função BRCA ou reativando a expressão gênica por meio de mudanças nas marcações do DNA. Outras protegem a delicada maquinaria de replicação do DNA para que ela não entre em colapso sob estresse, ou ajustam o manejo de proteínas de embalagem do DNA, chamadas histonas, de modo que seus cromossomos permaneçam mais estáveis. Em alguns casos, as células cancerosas simplesmente bombeiam o fármaco para fora com mais eficiência, reduzindo sua concentração dentro da célula. Esses truques de resistência em camadas ajudam a explicar por que as respostas frequentemente desaparecem e por que o mesmo medicamento pode funcionar de forma diferente entre pacientes.
Próximos passos: combinações mais inteligentes e acesso ampliado
Para se antecipar à resistência, pesquisadores estão testando inibidores de PARP junto com quimioterapia, drogas que bloqueiam pontos de verificação imune e medicamentos que inibem outras vias de resposta ao estresse dentro das células cancerosas. A esperança é que combinações bem escolhidas, guiadas por marcadores genéticos, tornem mais difícil para os tumores escapar mantendo os efeitos colaterais manejáveis. Os autores também pedem por inibidores de PARP de próxima geração mais seletivos que preservem as células sanguíneas saudáveis, melhores ferramentas para prever quem se beneficiará e atenção ao custo e à disponibilidade desses tratamentos em ambientes de poucos recursos. Em termos simples, os inibidores de PARP transformaram uma vulnerabilidade genética em alguns cânceres de mama em uma oportunidade terapêutica real, mas o controle duradouro exigirá entender e bloquear as muitas formas pelas quais os tumores reagem.
Citação: Wang, W., Cai, C., Qin, S. et al. PARP inhibitors and breast cancer: from therapeutic breakthrough to resistance challenge. Exp Mol Med 58, 981–992 (2026). https://doi.org/10.1038/s12276-026-01673-8
Palavras-chave: inibidores de PARP, câncer de mama, mutações BRCA, resistência a fármacos, terapia alvo