Clear Sky Science · tr
Bağışıklık aktivitesini ve protein dönüşümünü “mikro‑yönetmek”: sağlık ve hastalık bağlamında mikroglial lizozomlar
Beyninizin Temizlik Ekibini İzlemek
Beynin derinliklerinde, mikroglia adı verilen küçük bağışıklık hücreleri hademe ve ilk müdahale ekibi gibi davranır. Yaşla veya Alzheimer gibi hastalıklarda birikebilen mikropları, ölü hücreleri ve yanlış katlanmış protein kümelerini yutarlar. Bu derleme makale, bu öykünün daha az bilinen bir bölümünü inceliyor: mikroglial lizozomların, yani hücrenin içsel “geri dönüşüm merkezlerinin” rolü. Bu bölmelerin nasıl düzenlendiğini, stres ve yaşlanmayla nasıl değiştiklerini ve hücre tipleri arasında nasıl farklılık gösterdiklerini izleyerek yazarlar, mikroglial lizozomların ince ayarının nörodejeneratif hastalıkları önlemede veya tedavi etmede anahtar olabileceğini gösteriyor.
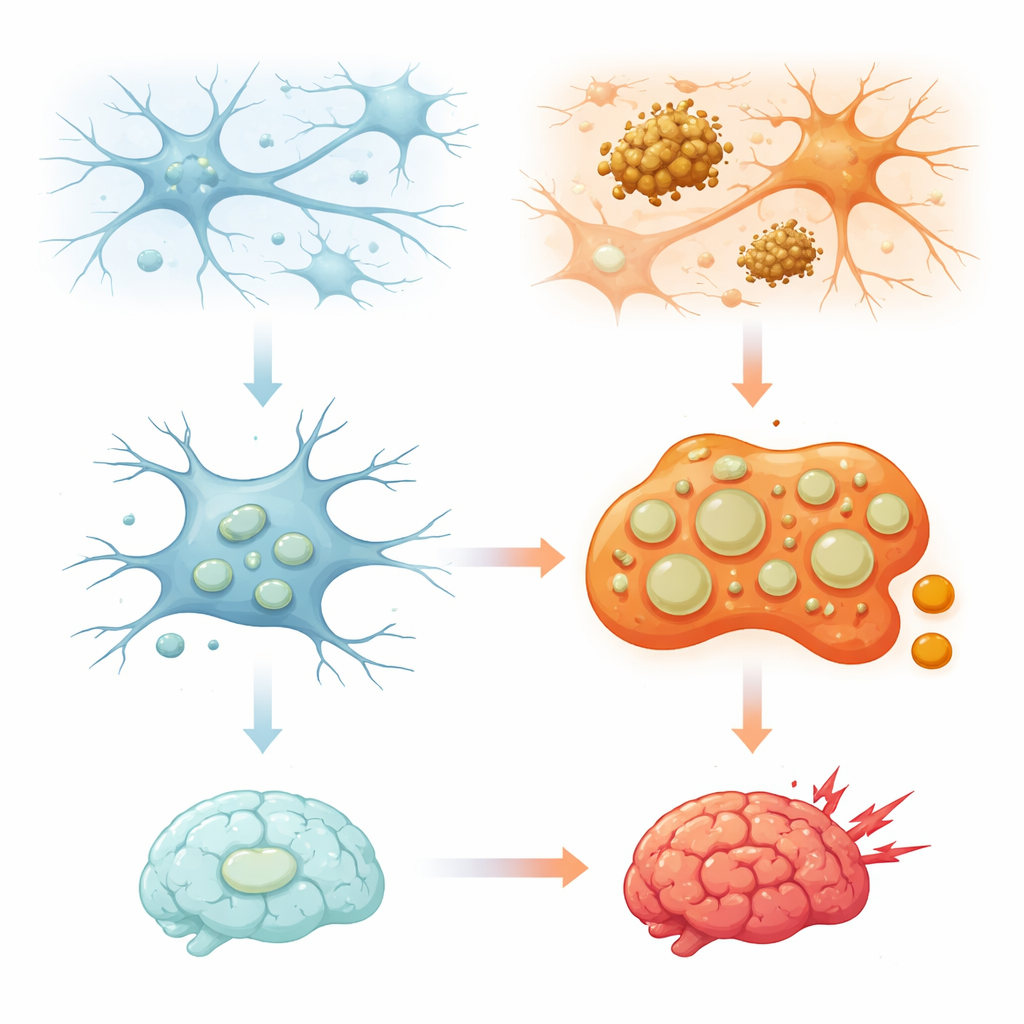
Beyin Hademeleri İçindeki Geri Dönüşüm Kutularını Nasıl Kullanır
Lizozomlar uzun süre eskimiş proteinleri ve organelleri parçalayan basit çöp kutuları olarak görülmüştür. Son on yılda daha karmaşık bir tablo ortaya çıktı: lizozomlar besinleri algılar, enerji kullanımını kontrollemeye yardımcı olur, bağışıklık tepkilerini şekillendirir ve hatta hücre ölümü kararlarına katılır. Sürekli beyni devriye gezen mikroglialarda bu bölmeler özellikle önemlidir çünkü mikroplardan protein agregatlarına ve budanmaya ihtiyaç duyan sinapslara kadar büyük miktarda yutulmuş materyali işlerler. Derleme, mikroglial lizozomların eşit olmadığını; kompozisyonları, hücre içindeki konumları ve davranışlarının stres, yaşlanma ve hastalıkla değişen farklı alt popülasyonlar oluşturduğunu açıklıyor. Bu çeşitliliğin nasıl inşa edildiğini ve korunduğunu anlamak, neden bazı beyin bölgelerinin veya hücre tiplerinin diğerlerinden daha savunmasız olduğunu kavramak için esastır.
Lizozomları Açıp Kapatan Anahtarlar
Genetik düzeyde mikroglial lizozomlar, özellikle TFEB dahil bir dizi transkripsiyon faktörünü içeren anahtar bir ağ tarafından kontrol edilir. Hücreler stres altındayken veya aşırı yüklenmişken TFEB çekirdeğe taşınır ve daha fazla lizozom inşa eden ve bunların aktivitesini artıran bir gen setini açar. Zebrafish ve fare modellerindeki çalışmalar, bu TFEB kaynaklı programın mikrogliaların uygun şekilde göç etmesi, lizozomlarını asitleştirmesi ve toksik Tau formları gibi protein agregatlarına karşı güçlü bir bağışıklık yanıtı oluşturması için kritik olduğunu gösterir. Diğer düzenleyiciler ters yönde etkiler. Örneğin, Parkinson ile ilişkilendirilen aşırı aktif bir enzim olan LRRK2, mikroglia ve makrofajlarda bu transkripsiyon faktörlerini çekirdekten uzak tutar, lizozomal parçalanmayı zayıflatır ve potansiyel olarak hastalık riskini artırır. Birlikte, bu bulgular stres altında lizozomal fonksiyonu artıran yollar ile günlük dengeyi korumak için onu sınırlayan yollar arasında bir çekişmeyi vurgular.
Koruyucu Temizlikten Zararlı İnflamasyona
Mikroglial lizozomlar atık giderimi ve inflamasyonun kesişme noktasında yer alır. Mikroglia bakteri bileşenleri, amiloid‑beta veya diğer protein agregatları gibi bağışıklık uyaran maddeleri yuttuğunda, lizozomları bu materyali parçalamakla kalmaz, aynı zamanda inflamatuar sinyallerin aktive edilmesine ve salınmasına da yardımcı olur. Normalde lizozomlarda sınırlı kalan kathepsin adı verilen proteazlar merkezi roller oynar: inaktif bağışıklık habercilerini aktif formlarına dönüştürmeye yardımcı olur, inflamatuar moleküllerin salımını teşvik eder ve sızıntı yaparlarsa veya salgılanırlarsa yakındaki nöronlara zarar verebilirler. Diğer bir lizozomal protein olan CD68 aktif, fagositik mikroglia için yaygın bir belirteç olarak kullanılır ve yaşlanma, oksidatif stres ve Alzheimer patolojisi ile artar. Ancak onun temizleme ve inflamasyondaki kesin işlevi belirsizliğini korur. Önemli olarak, lizozomal asitliği geri kazandıran ilaçlar veya mikroglial temizleme yollarına bağlanan antikorlar deney hayvanı modellerinde inflamasyonu yatıştırabilir ve protein temizliğini iyileştirebilir; bu da yeni terapötik yolların ipuçlarını verir.
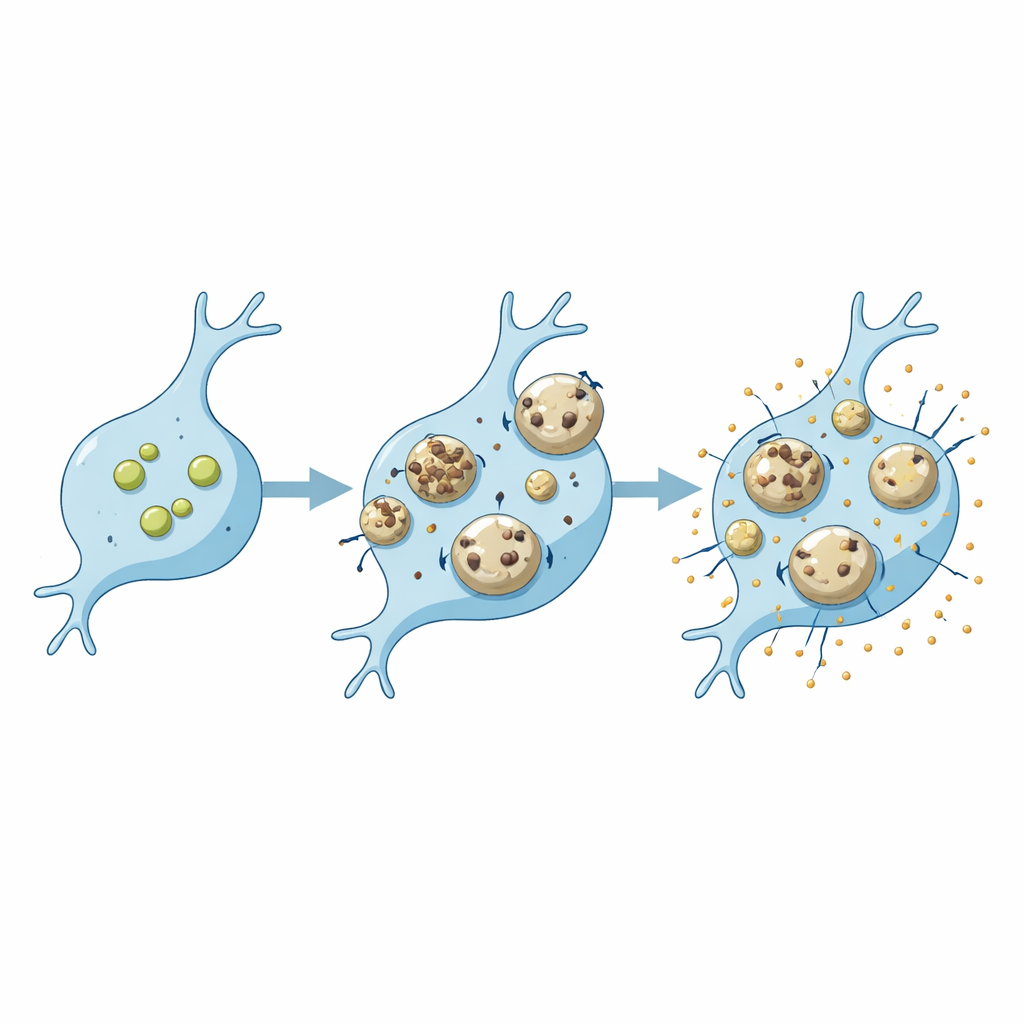
Farklı Hücreler, Farklı Savunmasızlıklar
Derleme aynı genetik kusurun mikroglial ve nöronal lizozomları farklı şekillerde etkileyebileceğini vurgular. Progranulin, SORLA veya C9ORF72 gibi demans veya motor nöron hastalığıyla bağlantılı proteinlerin kaybı, mikroglialarda bir lizozomal değişim desenine, nöronlarda başka bir desene yol açar. Mikroglialarda bu değişiklikler genellikle amiloid‑beta veya sinaptik döküntü gibi kargoyu ne kadar iyi parçaladıklarını ve ne kadar güçlü bir inflamatuar yanıt verdiklerini değiştirir. Lizozomlar, amiloid‑beta veya alfa‑sinüklein gibi yapışkan agregatlarla dolduklarında fiziksel hasara da yatkındır. Mikroglialarda bu tür hasar koruyucu onarım yollarını ve lizofaji adı verilen hedefe yönelik bir oto‑temizleme biçimini tetikleyebilir; bu korunma mekanizmaları başarısız olursa sızan enzimler hücre ölümünü ve daha fazla inflamasyonu tetikleyebilir. Kanıtlar mikrogliaların nöronlardan daha sağlam onarım seçeneklerine sahip olabileceğini öne sürer, ancak bunun yaşla veya hastalıkla nasıl değiştiği hâlâ araştırılmaktadır.
Mikroglial Hücrelerin İçindeki Gizli Çeşitlilik
Hücre tipleri arasındaki farklılıkların ötesinde, mikroglia kendileri arasında ve tek bir hücre içinde bile çarpıcı çeşitlilik gösterir. Fare ve maymunların yaşlanan beyinlerinde yapılan çalışmalar, birikirdikleri otofloresan, lizozom‑zengin depolama materyalinin miktarına göre iki geniş mikroglia sınıfı ortaya koymuştur. Bir alt grup zamanla karmaşık depolama cisimleri ve yüksek düzeyde lizozomal proteinler ve enzimler biriktirir, sonra çok ileri yaşlarda sayıca azalır. Tek tek mikrogliyada, uzun dallanmış süreçlerdeki lizozomlar hücre gövdesindekilerden farklı olabilir; bu, sinaps budama veya miyelin döküntüsüyle başa çıkma gibi yerel talepleri yansıtır. Yazarlar yanıtlanmamış soruları sıralar: dinlenme halindeki ve aktive olmuş lizozomlar nasıl farklıdır, aktivasyon yeni lizozomların doğuşunu tetikler mi, CD68‑pozitif lizozomlar nasıl özelleşmiştir ve bazı lizozomal havuzlar salgıya mı adanmıştır yoksa diğerleri sindirime mi odaklanır. Bu soruların yanıtlanması ileri görüntüleme ve moleküler araçlar gerektirecek, ancak beyin sağlığı anlayışımızı derinleştirme sözü veriyor.
Bu Küçük Bölmelerin Beyin Sağlığı İçin Neden Önemi Var
Genel olarak derleme, mikroglial lizozomları temizlik, metabolizma ve bağışıklığın kesiştiği ince ayarlı merkezler olarak tasvir eder. Bu bölmeler iyi çalıştığında, mikrogliaların döküntüleri temizleyerek ve tehditleri sınırlayarak beyin devrelerini sessizce korumalarına yardımcı olurlar. Aşırı yüklendiklerinde, genetik olarak bozulduklarında veya toksik agregatlar tarafından fiziksel olarak zarar gördüklerinde, koruyucu geri dönüşüm merkezlerinden kronik inflamasyon ve nöronal hasar kaynaklarına dönüşebilirler. Mikroglial lizozomların düzenleyici ağlarını, hasar yanıtlarını ve gizli çeşitliliğini haritalandırarak yazarlar, gelecekteki terapilerin bu sistemleri seçici olarak güçlendirip yeniden dengeleyebileceğini—yararlı temizlemeyi artırırken zararlı inflamasyonu sınırlayarak—nörodejeneratif hastalıkları yavaşlatma veya önleme potansiyeline sahip olabileceğini savunuyorlar.
Atıf: Somodji, E.A., Gowrishankar, S. “Micro-managing” immune activation and protein turnover: microglial lysosomes in the context of health and disease. npj Dement. 2, 35 (2026). https://doi.org/10.1038/s44400-026-00086-8
Anahtar kelimeler: mikroglia, lizozomlar, nöroinflamasyon, Alzheimer hastalığı, protein agregasyonu