Clear Sky Science · fr
« Micro‑gestion » de l’activation immunitaire et du renouvellement protéique : les lysosomes microgliaux dans le contexte de la santé et de la maladie
Observer l’équipe de nettoyage du cerveau
Au cœur du cerveau, de minuscules cellules immunitaires appelées microglies jouent le rôle de nettoyeurs et d’intervenants de première ligne. Elles engloutissent des agents pathogènes, des cellules mortes et des amas de protéines mal repliées qui peuvent s’accumuler avec l’âge ou dans des maladies comme la maladie d’Alzheimer. Cet article de synthèse explore un volet moins connu de cette histoire : le rôle des lysosomes microgliaux, ces « centres de recyclage » internes à la cellule. En retraçant la manière dont ces compartiments sont régulés, comment ils changent sous l’effet du stress et du vieillissement et comment ils varient selon les types cellulaires, les auteurs montrent pourquoi l’ajustement fin des lysosomes microgliaux pourrait être essentiel pour prévenir ou traiter les maladies neurodégénératives.
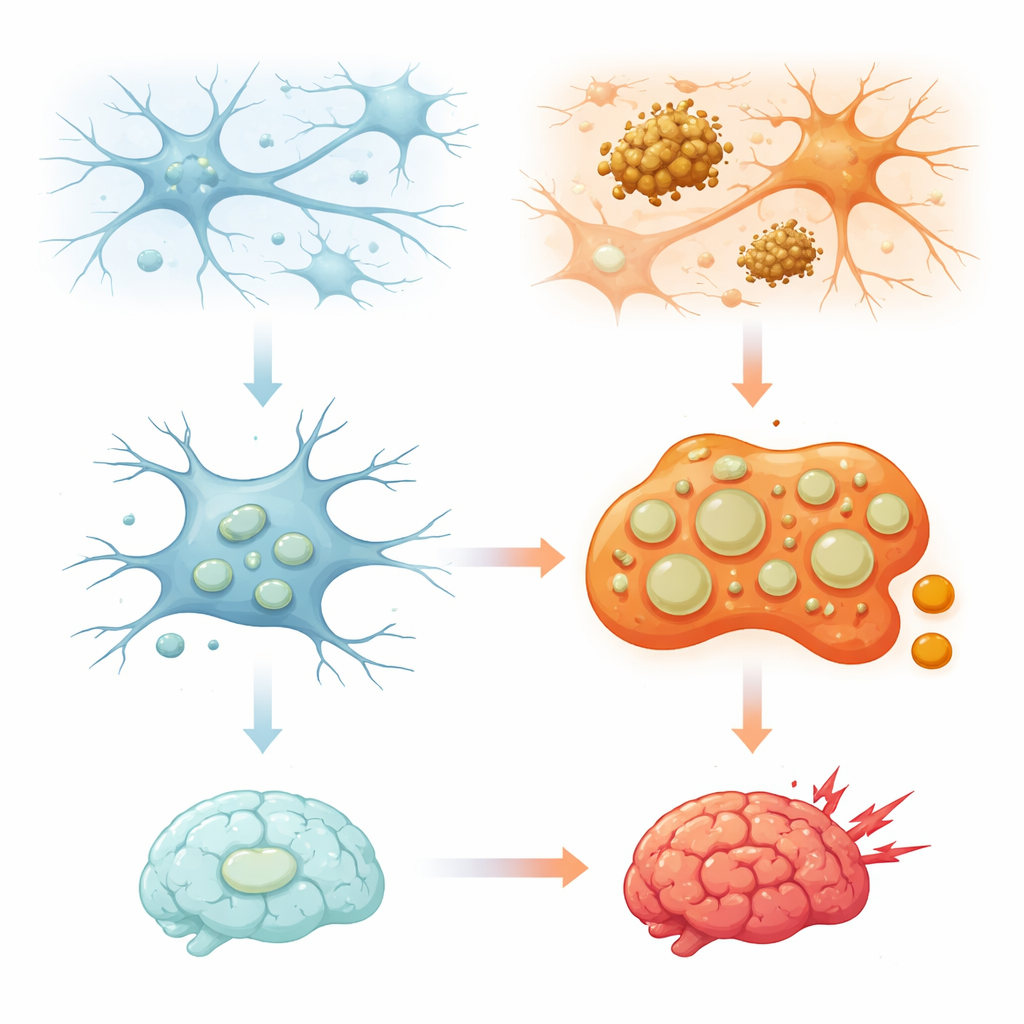
Comment les nettoyeurs du cerveau utilisent leurs bacs de recyclage internes
Les lysosomes ont longtemps été considérés comme de simples poubelles dégradant les protéines et organites usés. La dernière décennie a révélé un tableau plus complexe : les lysosomes détectent aussi les nutriments, aident à contrôler l’utilisation énergétique, modulent les réponses immunitaires et participent même aux décisions de mort cellulaire. Chez la microglie, qui patrouille constamment dans le cerveau, ces compartiments sont particulièrement importants car ils traitent de grandes quantités de matériel ingéré, des microbes aux agrégats protéiques en passant par les synapses à élaguer. La revue explique que les lysosomes microgliaux ne sont pas tous identiques ; ils forment des sous‑populations dont la composition, la position intracellulaire et le comportement évoluent sous l’effet du stress, du vieillissement et de la maladie. Comprendre comment cette diversité se construit et se maintient est essentiel pour saisir pourquoi certaines régions cérébrales ou certains types cellulaires sont plus vulnérables que d’autres.
Interrupteurs qui augmentent ou diminuent l’activité lysosomale
Au niveau génétique, les lysosomes microgliaux sont contrôlés par un réseau d’interrupteurs maîtres, en particulier une famille de facteurs de transcription qui comprend TFEB. Lorsque les cellules sont stressées ou surchargées, TFEB migre vers le noyau et active un ensemble de gènes qui construisent davantage de lysosomes et renforcent leur activité. Des études chez le poisson zèbre et chez la souris montrent que ce programme piloté par TFEB est crucial pour que les microglies migrent correctement, acidifient leurs lysosomes et montent une réponse immunitaire robuste contre des agrégats protéiques comme les formes toxiques de Tau. D’autres régulateurs vont dans le sens opposé. Par exemple, une enzyme liée à la maladie de Parkinson, LRRK2, hyperactive, empêche ces facteurs de transcription d’entrer dans le noyau des microglies et des macrophages, affaiblissant la dégradation lysosomale et augmentant potentiellement le risque de maladie. Ensemble, ces observations soulignent un jeu de tiraillement entre des voies qui améliorent la fonction lysosomale sous stress et d’autres qui la restreignent pour préserver l’équilibre quotidien.
Du nettoyage protecteur à l’inflammation dommageable
Les lysosomes microgliaux se situent à la croisée de l’élimination des déchets et de l’inflammation. Lorsque les microglies engulfent des substances immunostimulantes — telles que des composants bactériens, l’amyloïde‑bêta ou d’autres agrégats protéiques —, leurs lysosomes non seulement dégradent ce matériel, mais contribuent aussi à activer et libérer des signaux inflammatoires. Des protéases appelées cathépsines, normalement confinées aux lysosomes, jouent des rôles centraux : elles aident à convertir des messagers immunitaires inactifs en formes actives, favorisent la libération de molécules inflammatoires et, lorsqu’elles fuient ou sont sécrétées, peuvent même endommager les neurones voisins. Une autre protéine lysosomale, CD68, est largement utilisée comme marqueur des microglies actives et phagocytaires et augmente avec l’âge, le stress oxydatif et la pathologie d’Alzheimer. Pourtant, sa fonction exacte dans l’élimination et l’inflammation reste incertaine. Il est important de noter que des médicaments qui restaurent l’acidité lysosomale ou des anticorps qui ciblent les voies d’élimination microgliale peuvent calmer l’inflammation et améliorer l’élimination des protéines dans des modèles animaux, suggérant de nouvelles pistes thérapeutiques.
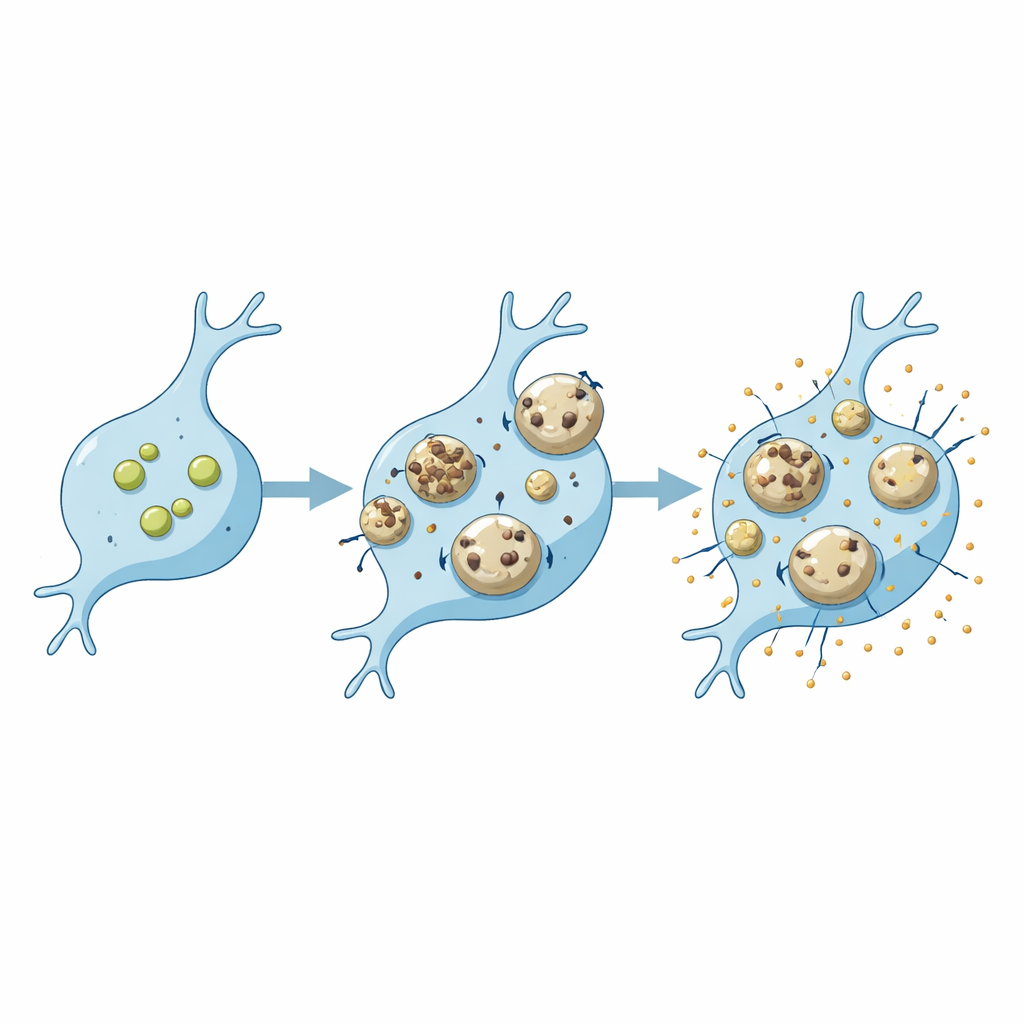
Cellules différentes, vulnérabilités différentes
La revue souligne que le même défaut génétique peut affecter différemment les lysosomes des microglies et des neurones. La perte de protéines telles que la progranuline, SORLA ou C9ORF72, toutes liées à la démence ou aux maladies du motoneurone, entraîne un profil de modifications lysosomales chez la microglie et un autre chez le neurone. Chez la microglie, ces changements altèrent souvent la capacité à dégrader des cargaisons comme l’amyloïde‑bêta ou les débris synaptiques et modulent l’intensité des réponses inflammatoires. Les lysosomes sont aussi vulnérables aux dommages physiques lorsqu’ils sont saturés d’agrégats collants comme l’amyloïde‑bêta ou l’alpha‑synucléine. Chez la microglie, de tels dommages peuvent déclencher des voies de réparation protectrices et une forme d’auto‑nettoyage ciblé appelée lysophagie ; si ces mécanismes échouent, des enzymes fuitées peuvent provoquer la mort cellulaire et aggraver l’inflammation. Les données suggèrent que les microglies pourraient disposer d’options de réparation plus robustes que les neurones, mais la façon dont cela évolue avec l’âge ou la maladie reste à explorer.
Diversité cachée à l’intérieur des cellules microgliales
Au‑delà des différences entre types cellulaires, les microglies présentent une variation frappante entre elles et même au sein d’une même cellule. Des travaux sur des cerveaux vieillissants de souris et de singes ont mis au jour deux grandes classes de microglies distinguées par la quantité de matériel de stockage autofluorescent riche en lysosomes qu’elles accumulent. Un sous‑ensemble accumule des corps de stockage complexes et de forts niveaux de protéines et d’enzymes lysosomales au fil du temps, puis décline en nombre à des âges très avancés. À l’intérieur des microglies individuelles, les lysosomes situés dans les longs prolongements branchés peuvent différer de ceux du corps cellulaire, reflétant des demandes locales pour l’élagage des synapses ou la prise en charge des débris de myéline. Les auteurs énoncent des questions ouvertes : en quoi les lysosomes au repos diffèrent‑ils de ceux activés, l’activation déclenche‑t‑elle la naissance de nouveaux lysosomes, comment les lysosomes CD68‑positifs sont‑ils spécialisés et certains pools lysosomaux sont‑ils dédiés à la sécrétion tandis que d’autres se concentrent sur la digestion ? Répondre à ces questions exigera des outils d’imagerie et moléculaires avancés, mais promet d’approfondir notre compréhension de la santé cérébrale.
Pourquoi ces minuscules compartiments comptent pour la santé du cerveau
Dans l’ensemble, la revue présente les lysosomes microgliaux comme des carrefours finement réglés où se rencontrent nettoyage, métabolisme et immunité. Lorsqu’ils fonctionnent correctement, ces compartiments aident les microglies à maintenir silencieusement les circuits cérébraux en éliminant les débris et en maîtrisant les menaces. Lorsqu’ils sont surchargés, génétiquement compromis ou endommagés par des agrégats toxiques, ils peuvent basculer de centres de recyclage protecteurs en sources d’inflammation chronique et de lésions neuronales. En cartographiant les réseaux de régulation, les réponses aux dommages et la diversité cachée des lysosomes microgliaux, les auteurs soutiennent que des thérapies futures pourraient renforcer ou rééquilibrer sélectivement ces systèmes — améliorer l’élimination bénéfique tout en limitant l’inflammation nocive — afin de ralentir ou prévenir les maladies neurodégénératives.
Citation: Somodji, E.A., Gowrishankar, S. “Micro-managing” immune activation and protein turnover: microglial lysosomes in the context of health and disease. npj Dement. 2, 35 (2026). https://doi.org/10.1038/s44400-026-00086-8
Mots-clés: microglie, lysosomes, neuroinflammation, maladie d’Alzheimer, agrégation protéique