Clear Sky Science · he
"ניהול־מיקרו" של הפעלת מערכת החיסון ומחזור חלבונים: ליזוזומים של מיקרוגליה בהקשר של בריאות ומחלה
מביטים בצוות הניקיון של המוח
לעומק המוח פועלות תאי חיסון זעירים הנקראים מיקרוגליה, שפועלים כשוטפי־רוח וכמגיבים ראשונים. הם בולעים פתוגנים, תאים מתים וטלאים של חלבונים מקופלים בצורה שגויה שיכולים להצטבר עם הגיל או במחלות כמו אלצהיימר. מאמר הסקירה הזה בוחן חלק פחות מוכר של הסיפור: תפקידם של הליזוזומים במיקרוגליה, "מרכזי המיחזור" הפנימיים של התא. בעזרת המעקב אחרי האופן שבו מחלקות אלה נשלטות, כיצד הן משתנות במצב של סטרס והזדקנות, וכיצד הן שונות בין סוגי תאים, המחברים מראים מדוע כוונון עדין של הליזוזומים המיקרוגליאליים עשוי להיות המפתח למניעה או לטיפול במחלות נוירו־דגנרטיביות.
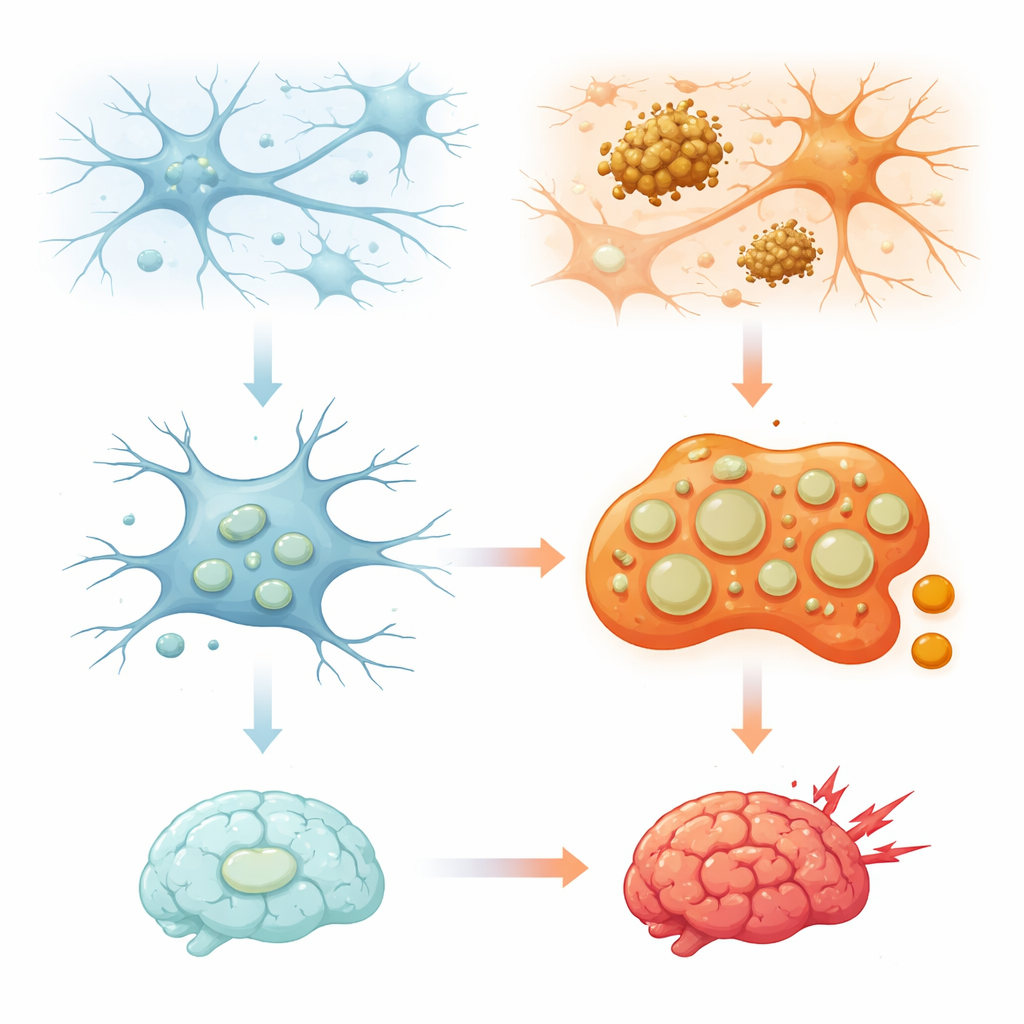
איך שומרי־הסדר של המוח משתמשים במיכלי המיחזור הפנימיים שלהם
ליזוזומים נתפסו זמן רב כדליים פשוטים שמפרקים חלבונים ואברונים שחוקים. העשור האחרון הראה תמונה מורכבת יותר: הליזוזומים גם חשים רמות מזון, עוזרים לשלוט על צריכת אנרגיה, מעצבים תגובות חיסוניות ואפילו משתתפים בהחלטות מוות תאי. במיקרוגליה, שמסיירת ללא הפסקה במוח, מחלקות אלה חשובות במיוחד משום שהן מטפלות בכמויות גדולות של חומר שנבלע — ממיקרובים ועד הצטברויות חלבון וסינפסות שדורשות גיזום. הסקירה מסבירה שליזוזומים מיקרוגליאליים אינם זהים זה לזה; הם יוצרים תת־אוכלוסיות שונות שההרכב שלהן, מיקומן בתוך התא והתנהגותן משתנים בסטרס, בהזדקנות ובמחלה. הבנת האופן שבו בנויה ומתחזקת המגווןיות הזו חיונית כדי להבין מדוע אזורים מוחיים או סוגי תאים מסוימים פגיעים יותר מאחרים.
מתגים שמגבירים או מכבים את פעולת הליזוזומים
ברמה הגנטית, הליזוזומים של המיקרוגליה נשלטים על ידי רשת של מתגים ראשיים, ובפרט משפחה של גורמי שעתוק שכוללת את TFEB. כשהתאים נתונים ללחץ או עמוסים, TFEB נודד לגרעין ומפעיל סט גנים שבונה יותר ליזוזומים ומגבירה את פעילותם. מחקרים בדגי זברה ובמודלים עכבריים מראים שתוכנית מונחית TFEB זו חיונית למיקרוגליה על מנת לנוע כראוי, להחמיץ את הליזוזומים שלה ולקיים תגובת חיסון חזקה כנגד הצטברויות חלבון כגון צורות רעילות של טאו. רגולטורים אחרים פועלים בכיוון ההפוך. למשל, אנזים פעיל יתר המקושר לפרקינסון, LRRK2, שומר על גורמי השעתוק הללו מחוץ לגרעין במיקרוגליה ובמאקרופאגים, מה שמחליש את פירוק הליזוזומים ועשוי להעלות את הסיכון למחלה. יחד, הממצאים הללו מדגישים משיכה־ומתיחה בין מסלולים שמחזקים את תפקוד הליזוזומים תחת לחץ לבין אלה שמגבילים אותו כדי לשמור על שווי משקל יומיומי.
מניקיון מגן לדלקת מזיקה
הליזוזומים המיקרוגליאליים נמצאים בצומת של הסרת פסולת ודלקת. כאשר מיקרוגליה בולעת חומרים שמעוררים את המערכת החיסונית — כגון רכיבים חיידקיים, אמילואיד־בטא או הצטברויות חלבון אחרות — הליזוזומים שלה לא רק מפרקים את החומר אלא גם מסייעים בהפעלת ושחרור אותות דלקתיים. פרוטאזות הנקראות קטפסינים, שלרוב מוגבלות בתוך הליזוזומים, ממלאות תפקידים מרכזיים: הן מסייעות להמיר שליחי חיסון לא פעילים לאקטיביים, מקדמות שחרור מולקולות דלקת, וכאשר הן מדליפות או מופרשות — עלולות אפילו לפגוע בנוירונים סמוכים. חלבון ליזוזומלי נוסף, CD68, משמש באופן נרחב כסמן למיקרוגליה פעילה ופאגוציטית ועולה עם הגיל, מתח חמצוני ופאתולוגיה של אלצהיימר. עם זאת, תפקידו המדויק בסילוק ודלקת נותר לא ברור. חשוב לציין כי תרופות שמשחזרות את חומציות הליזוזומים או נוגדנים שמפעילים נתיבי סילוק מיקרוגליאליים יכולות להרגיע דלקת ולשפר את הסרת החלבונים במודלים חייתיים, רומזות לדרכי טיפול חדשות.
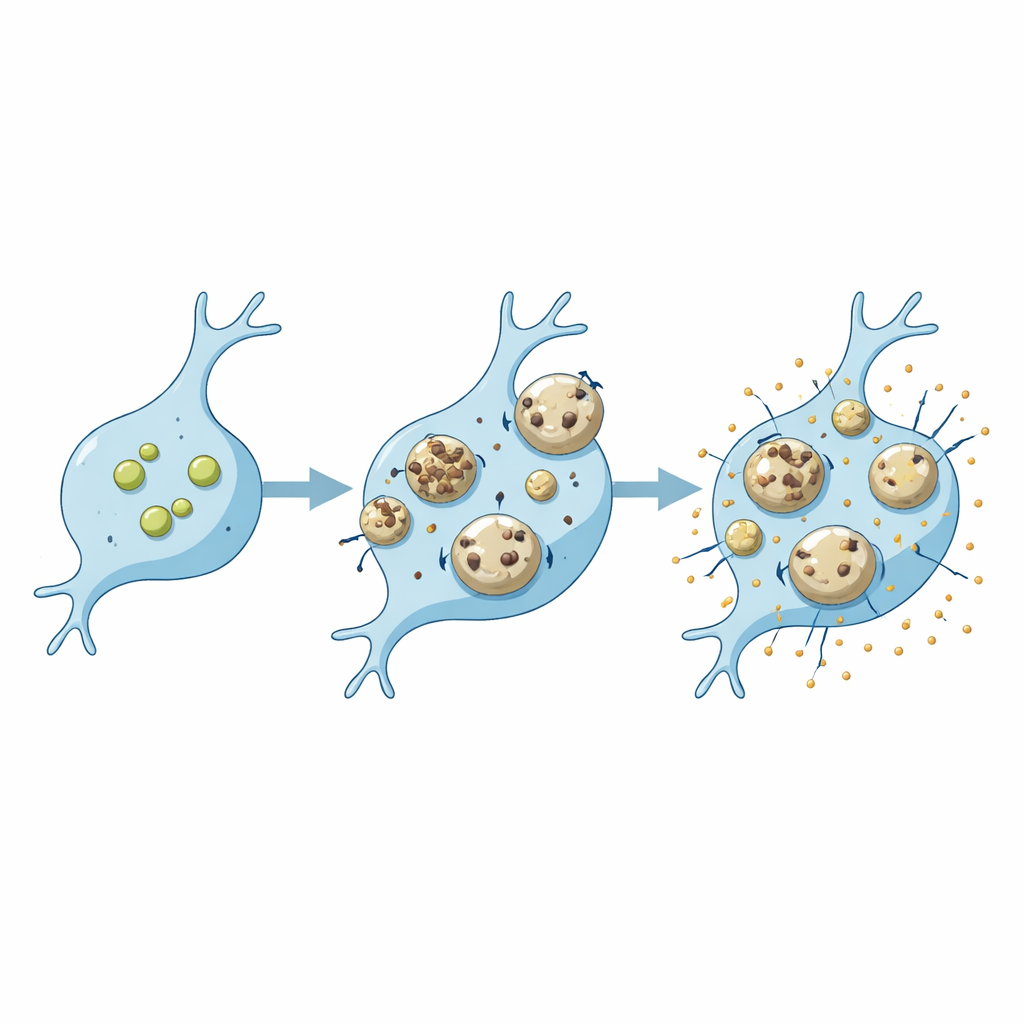
תאים שונים, פגיעויות שונות
הסקירה מדגישה שאותה מוטציה גנטית יכולה להשפיע על ליזוזומים במיקרוגליה ובנוירונים בדרכים שונות. אובדן חלבונים כגון פרוגרנולין, SORLA או C9ORF72, שכולם מקושרים לדמנציה או למחלת נוירון מוטורי, מוביל לתבניות שונות של שינוי ליזוזומלי במיקרוגליה ובנוירונים. במיקרוגליה, שינויים אלו לעתים משפיעים על יעילות פירוק העומס כמו אמילואיד‑בטא או שאריות סינפטיות וכיצד הם מגיבים באיתותי דלקת. הליזוזומים גם נוטים לנזק פיזי כשיוצאי דופן דביקים כמו אמילואיד‑בטא או אלפא‑סינוקלאין ממלאים אותם. במיקרוגליה, נזק כזה יכול לעורר מסלולי תיקון מגן וצורת ניקוי עצמי ממוקדת הנקראת ליזופאגיה; אם אמצעי הזהירות הללו נכשלו, אנזימים מדולפים עלולים להניע מוות תאי ודלקת נוספת. עדויות מצביעות על כך שלמיקרוגליה עשויות להיות אופציות תיקון עמידות יותר מאשר לנוירונים, אך כיצד הדבר משתנה עם הגיל או המחלה עדיין נחקר.
מגוון מוסתר בתוך תאי המיקרוגליה
מעבר להבדלים בין סוגי תאים, המיקרוגליה מציגה שונות בולטת גם ביניהן ואפילו בתוך תא בודד. מחקרים במוחות מזדקנים של עכברים וקופים חשפו שתי קטגוריות רחבות של מיקרוגליה המובחנות לפי כמות חומר האוטופרלואורסצנציה העשיר בליזוזומים שהם צוברים. תת־קבוצה אחת בונה עם הזמן גופיפי אחסון מורכבים ורמות גבוהות של חלבוני ולבעלי־מנגנון ליזוזום, ואז פוחתת במספרה בגילים מאוד מתקדמים. בתוך מיקרוגליה יחיד, ליזוזומים בתהליכים המתמשכים והמשוננים עשויים להיות שונים מאלו שבגוף התא, מה שמעיד על דרישות מקומיות לגיזום סינפסות או לטיפול בשברי מיאלין. המחברים מציינים שאלות פתוחות: כיצד ליזוזומים במנוחה ובמצב מופעל שונים, האם ההפעלה מציתה לידה של ליזוזומים חדשים, איך ליזוזומים החיוביים ל‑CD68 מתמחים, והאם חלק ממאגרי הליזוזום משמשים להפרשה בעוד אחרים מתמקדים בעיכול. מענה על שאלות אלה ידרוש כלים מולקולריים ותמונתיים מתקדמים אך מבטיח להעמיק את הבנתנו את בריאות המוח.
למה מבנים זעירים אלה חשובים לבריאות המוח
בסך הכל, הסקירה מציירת את הליזוזומים המיקרוגליאליים כמרכזים מכוונים היטב שבהם נפגשים ניקיון, מטבוליזם וחיסון. כשמיכלים אלה מתפקדים היטב, הם מסייעים למיקרוגליה לשמור בשקט על מעגלי המוח על ידי סילוק פסולת והגבלת איומים. כשהם עומסים יתר על המידה, פגועים גנטית או נפגעים פיזית על ידי הצטברויות רעילות, הם עלולים להפוך ממרכזי מיחזור מגן למקורות של דלקת כרונית ופגיעה נוירונלית. על ידי מיפוי רשתות הבקרה, תגובות הנזק והמגוון המוסתר של הליזוזומים המיקרוגליאליים, המחברים טוענים שתרופות עתידיות עשויות להגביר באופן סלקטיבי או לאזן מחדש מערכות אלה — לחזק את הסילוק המועיל תוך הגבלת הדלקת המזיקה — כדי להאט או למנוע מחלות נוירו‑דגנרטיביות.
ציטוט: Somodji, E.A., Gowrishankar, S. “Micro-managing” immune activation and protein turnover: microglial lysosomes in the context of health and disease. npj Dement. 2, 35 (2026). https://doi.org/10.1038/s44400-026-00086-8
מילות מפתח: מיקרוגליה, ליזוזומים, דלקת־מוחית, מחלת אלצהיימר, הצטברות חלבונים