Clear Sky Science · de
„Mikro‑Management“ von Immunaktivierung und Proteinumsatz: Mikrogliäre Lysosomen im Kontext von Gesundheit und Krankheit
Die Reinigungsmannschaft des Gehirns beobachten
Tief im Gehirn fungieren winzige Immunzellen, die Mikroglia, als Hausmeister und Ersthelfer. Sie verschlingen Keime, abgestorbene Zellen und Klumpen fehlgefalteter Proteine, die mit dem Alter oder bei Erkrankungen wie Alzheimer zunehmen können. Dieser Übersichtsartikel beleuchtet einen weniger bekannten Teil dieser Geschichte: die Rolle mikrogliärer Lysosomen, der zellulären „Recyclingzentren“. Indem die Autoren nachzeichnen, wie diese Kompartimente gesteuert werden, wie sie sich bei Stress und Alterung verändern und wie sie zwischen Zelltypen variieren, zeigen sie, warum eine genaue Feinabstimmung mikrogliärer Lysosomen der Schlüssel sein könnte, um neurodegenerative Erkrankungen zu verhindern oder zu behandeln.
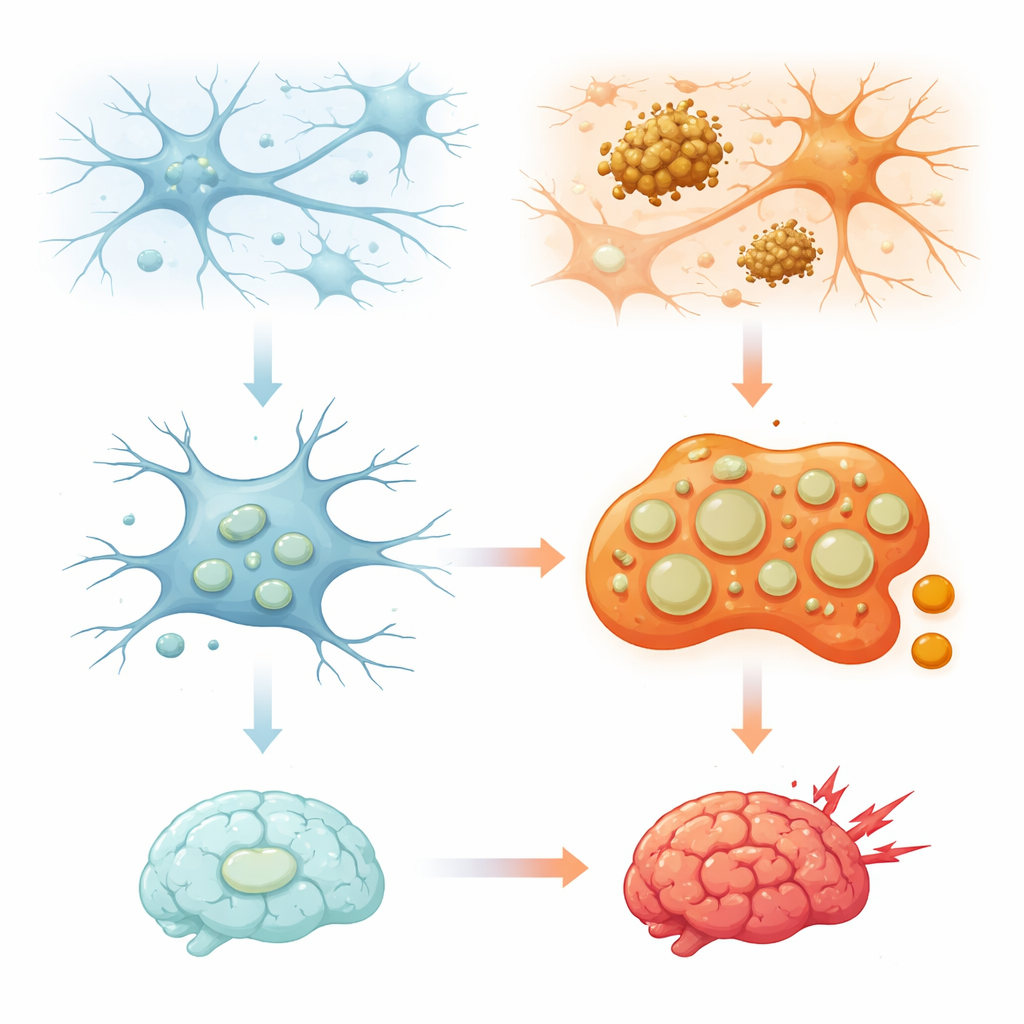
Wie die Brain‑Hausmeister ihre inneren Recyclingbehälter nutzen
Lysosomen galten lange als einfache Mülleimer, die abgenutzte Proteine und Organellen abbauen. Das letzte Jahrzehnt hat ein komplexeres Bild gezeichnet: Lysosomen fühlen auch Nährstoffe, helfen, den Energiehaushalt zu steuern, prägen Immunantworten und sind sogar an Entscheidungen über das Zelltodgeschehen beteiligt. In Mikroglia, die das Gehirn ständig patrouillieren, sind diese Kompartimente besonders wichtig, weil sie große Mengen verschluckten Materials verarbeiten, von Mikroben über Proteinaggregate bis hin zu Synapsen, die beschnitten werden müssen. Die Übersichtsarbeit erklärt, dass mikrogliäre Lysosomen nicht alle gleich sind; sie bilden verschiedene Subpopulationen, deren Zusammensetzung, Position innerhalb der Zelle und Verhalten sich bei Stress, Alterung und Krankheit verschieben. Zu verstehen, wie diese Vielfalt entsteht und erhalten wird, ist wesentlich, um zu begreifen, warum manche Hirnregionen oder Zelltypen anfälliger sind als andere.
Schalter, die Lysosomen hoch- oder herunterregeln
Auf genetischer Ebene werden mikrogliäre Lysosomen von einem Netzwerk von Hauptschaltern kontrolliert, insbesondere einer Familie von Transkriptionsfaktoren, zu der TFEB gehört. Wenn Zellen gestresst oder überlastet sind, wandert TFEB in den Zellkern und schaltet ein Set von Genen an, das mehr Lysosomen aufbaut und deren Aktivität steigert. Studien in Zebrafischen und Mausmodellen zeigen, dass dieses von TFEB gesteuerte Programm entscheidend dafür ist, dass Mikroglia richtig migrieren, ihre Lysosomen ansäuern und eine starke Immunantwort gegen Proteinaggregate wie toxische Tau‑Formen entfalten. Andere Regulatoren wirken entgegengesetzt. Ein überaktives, mit Parkinson assoziiertes Enzym, LRRK2, hält beispielsweise diese Transkriptionsfaktoren in Mikroglia und Makrophagen außerhalb des Zellkerns, schwächt den lysosomalen Abbau und könnte so das Erkrankungsrisiko erhöhen. Zusammen heben diese Befunde ein Tauziehen zwischen Wegen hervor, die die Lysosomenfunktion unter Stress verstärken, und solchen, die sie zurückhalten, um das normale Gleichgewicht zu bewahren.
Von schützendem Aufräumen zu schädlicher Entzündung
Mikrogliäre Lysosomen liegen an der Schnittstelle von Abfallbeseitigung und Entzündung. Wenn Mikroglia immunstimulierende Substanzen – wie bakterielle Bestandteile, Amyloid‑Beta oder andere Proteinaggregate – aufnehmen, bauen ihre Lysosomen dieses Material nicht nur ab, sondern tragen auch zur Aktivierung und Freisetzung entzündlicher Signale bei. Proteasen, sogenannte Kathepsine, die normalerweise innerhalb von Lysosomen eingeschlossen sind, spielen dabei zentrale Rollen: Sie helfen, inaktive Immunbotenstoffe in ihre aktive Form zu überführen, fördern die Freisetzung entzündlicher Moleküle und können bei Leckage oder Sekretion sogar umliegende Neurone schädigen. Ein weiteres lysosomales Protein, CD68, wird breit als Marker für aktive, phagozytierende Mikroglia verwendet und steigt mit Alterung, oxidativem Stress und Alzheimer‑Pathologie an. Seine genaue Funktion bei der Reinigung und Entzündung bleibt jedoch unklar. Wichtig ist, dass Wirkstoffe, die die lysosomale Säure wiederherstellen, oder Antikörper, die mikrogliäre Räumungswege ansprechen, in Tiermodellen Entzündungen dämpfen und Proteinbeseitigung verbessern können, was auf neue therapeutische Wege hindeutet.
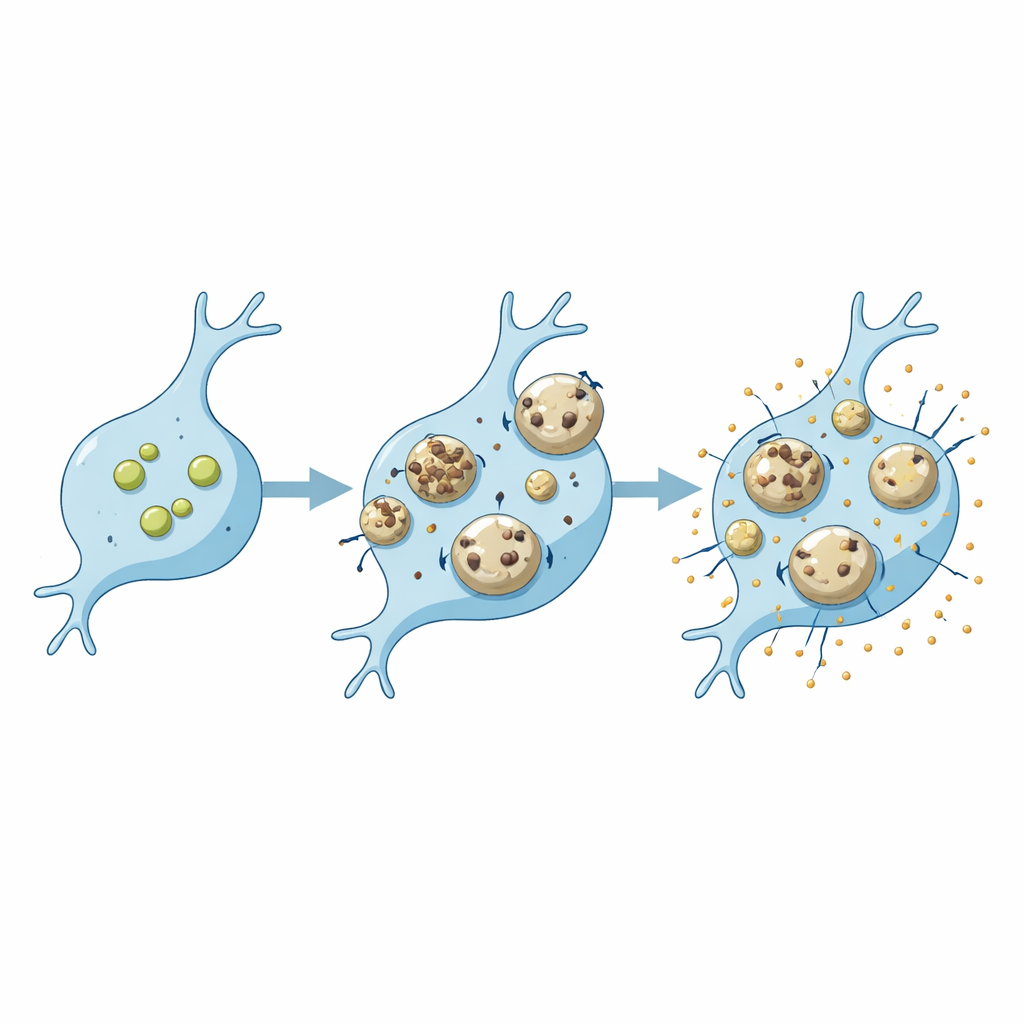
Verschiedene Zellen, verschiedene Verwundbarkeiten
Die Übersichtsarbeit betont, dass derselbe genetische Defekt mikrogliäre und neuronale Lysosomen auf unterschiedliche Weise beeinflussen kann. Der Verlust von Proteinen wie Progranulin, SORLA oder C9ORF72, die alle mit Demenz oder Motoneuronerkrankungen verknüpft sind, führt in Mikroglia zu einem Muster lysosomaler Veränderungen und in Neuronen zu einem anderen. In Mikroglia verändern diese Veränderungen oft, wie gut sie Fracht wie Amyloid‑Beta oder synaptische Trümmer abbauen und wie stark sie mit entzündlichen Signalen reagieren. Lysosomen sind auch physisch anfällig für Schäden, wenn sie mit klebrigen Aggregaten wie Amyloid‑Beta oder α‑Synuclein beladen sind. In Mikroglia kann solche Schädigung protektive Reparaturwege und eine Form gezielter Selbstreinigung namens Lysophagie auslösen; versagen diese Schutzmechanismen, können auslaufende Enzyme Zelltod und weitere Entzündungen antreiben. Hinweise deuten darauf hin, dass Mikroglia möglicherweise robusterer Reparuroptionen als Neurone besitzen, doch wie sich dies mit Alter oder Krankheit ändert, wird noch untersucht.
Verborgene Vielfalt innerhalb mikrogliärer Zellen
Über Unterschiede zwischen Zelltypen hinaus zeigen Mikroglia auffällige Variationen untereinander und sogar innerhalb einer einzelnen Zelle. Arbeiten an alternden Gehirnen von Mäusen und Affen haben zwei breite Klassen von Mikroglia aufgedeckt, die sich durch die Menge an autofluoreszierendem, lysosomenreichem Speicherstoff unterscheiden, die sie akkumulieren. Eine Untergruppe bildet im Laufe der Zeit komplexe Speicherkörper und hohe Mengen lysosomaler Proteine und Enzyme und nimmt in sehr hohem Alter dann in ihrer Zahl ab. Innerhalb einzelner Mikroglia können Lysosomen in langen Verzweigungen anders beschaffen sein als im Zellkörper, was lokale Anforderungen an das Beschneiden von Synapsen oder das Verarbeiten von Myelintrümmern widerspiegelt. Die Autoren skizzieren offene Fragen: wie sich ruhende und aktivierte Lysosomen unterscheiden, ob Aktivierung die Entstehung neuer Lysosomen anstößt, wie CD68‑positive Lysosomen spezialisiert sind und ob einige lysosomale Pools der Sekretion dienen, während andere sich auf Verdauung konzentrieren. Die Beantwortung dieser Fragen erfordert fortgeschrittene Bildgebungs‑ und molekulare Werkzeuge, verspricht aber, unser Verständnis der Gehirngesundheit zu vertiefen.
Warum diese winzigen Kompartimente für die Gehirngesundheit wichtig sind
Insgesamt zeichnen die Autoren das Bild mikrogliärer Lysosomen als fein abgestimmte Schaltzentralen, in denen Reinigung, Stoffwechsel und Immunität zusammenlaufen. Funktionieren diese Kompartimente gut, helfen sie Mikroglia, still und effizient Hirnschaltkreise zu erhalten, indem sie Trümmer beseitigen und Bedrohungen eindämmen. Werden sie überlastet, genetisch beeinträchtigt oder durch toxische Aggregate physisch geschädigt, können sie sich von schützenden Recyclingzentren in Quellen chronischer Entzündung und neuronaler Schädigung verwandeln. Indem die regulatorischen Netzwerke, Schadensantworten und die verborgene Vielfalt mikrogliärer Lysosomen kartiert werden, argumentieren die Autoren, könnten künftige Therapien diese Systeme gezielt stärken oder neu austarieren – indem sie die vorteilhafte Reinigung verbessern und schädliche Entzündungen begrenzen –, um neurodegenerative Erkrankungen zu verlangsamen oder zu verhindern.
Zitation: Somodji, E.A., Gowrishankar, S. “Micro-managing” immune activation and protein turnover: microglial lysosomes in the context of health and disease. npj Dement. 2, 35 (2026). https://doi.org/10.1038/s44400-026-00086-8
Schlüsselwörter: Mikroglia, Lysosomen, Neuroinflammation, Alzheimer‑Krankheit, Proteinaggregation