Clear Sky Science · ja
免疫活性化とタンパク質ターンオーバーを“ミクロに管理する”:健康と疾患の文脈におけるミクログリアのリソソーム
脳の清掃隊を見守る
脳の奥深くで、ミクログリアと呼ばれる小さな免疫細胞は清掃員でありファーストレスポンダーとして働きます。彼らは病原体、死んだ細胞、加齢やアルツハイマー病のような疾患で蓄積する誤って折りたたまれたタンパク質の塊を取り込んで処理します。本レビューはその物語のあまり知られていない側面、つまり細胞内の「リサイクルセンター」であるミクログリアのリソソームの役割を探ります。これらの区画がどのように制御され、ストレスや加齢でどう変化し、細胞種間でどのように異なるかをたどることで、ミクログリアのリソソームの微調整が神経変性疾患の予防や治療の鍵になり得る理由を示しています。
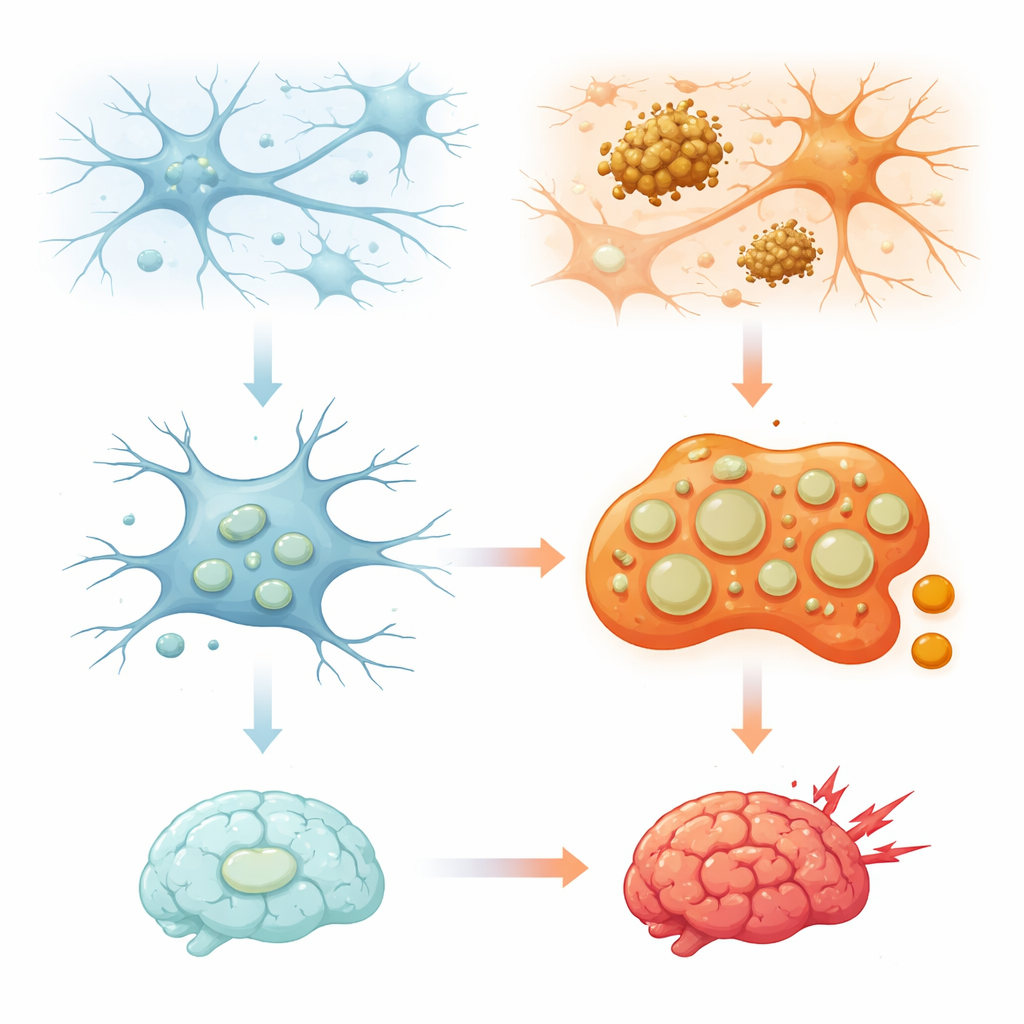
脳の清掃員が内側のリサイクル箱を使う仕組み
リソソームは長く、古くなったタンパク質や細胞小器官を分解する単純なゴミ箱と見なされてきました。しかし過去10年でより複雑な姿が明らかになっています:リソソームは栄養状態を感知し、エネルギー利用を制御し、免疫応答を形作り、さらには細胞死の判断にも関与します。常に脳を見回るミクログリアでは、これらの区画は取り込む物質の量が多いため特に重要です。微生物からタンパク質凝集体、刈り込みが必要なシナプスに至るまで処理します。レビューは、ミクログリアのリソソームが均一ではないことを説明します:組成、細胞内での位置、挙動がストレス、加齢、疾患に応じて変化する異なるサブポピュレーションを形成します。こうした多様性がどのように構築され維持されるかを理解することは、特定の脳領域や細胞種が他より脆弱になる理由を把握するうえで不可欠です。
リソソームの働きを上下させるスイッチ
遺伝子レベルでは、ミクログリアのリソソームはマスタースイッチのネットワーク、特にTFEBを含む転写因子ファミリーによって制御されています。細胞がストレスを受けたり過負荷になると、TFEBは核に移動してリソソームを増やしその活性を高める一連の遺伝子をオンにします。ゼブラフィッシュやマウスモデルの研究は、このTFEB駆動プログラムがミクログリアの適切な移動、リソソームの酸性化、そして有害なタウのようなタンパク質凝集体に対する強い免疫応答を発揮するために重要であることを示しています。他方で、逆方向に働く調節因子もあります。例えば、パーキンソン病に関連する過剰活性の酵素LRRK2は、ミクログリアやマクロファージにおいてこれらの転写因子を核から遠ざけ、リソソーム分解を弱め疾患リスクを高める可能性があります。これらの発見は、ストレス下でリソソーム機能を強化する経路と日常のバランスを保つために抑制する経路との間の綱引きを浮き彫りにします。
保護的な清掃から有害な炎症へ
ミクログリアのリソソームは廃棄物除去と炎症の交差点に位置します。ミクログリアが細菌成分、アミロイドβ、その他のタンパク質凝集体のような免疫刺激物質を貪食するとき、リソソームはこれらを分解するだけでなく炎症シグナルの活性化と放出にも関与します。カテプシンと呼ばれるプロテアーゼは通常リソソーム内部に閉じ込められていますが中心的役割を果たします:不活性な免疫メッセンジャーを活性型に変換し、炎症性分子の放出を促進し、漏れ出したり分泌された場合には近隣のニューロンを損傷することさえあります。別のリソソームタンパク質であるCD68は、活性化され貪食的なミクログリアのマーカーとして広く使われ、加齢、酸化ストレス、アルツハイマー病病理で増加しますが、その除去や炎症における正確な機能は不明のままです。重要なのは、リソソームの酸性度を回復する薬やミクログリアのクリアランス経路に働きかける抗体が、動物モデルで炎症を鎮めタンパク質除去を改善できることが示されており、新たな治療の道を示唆している点です。
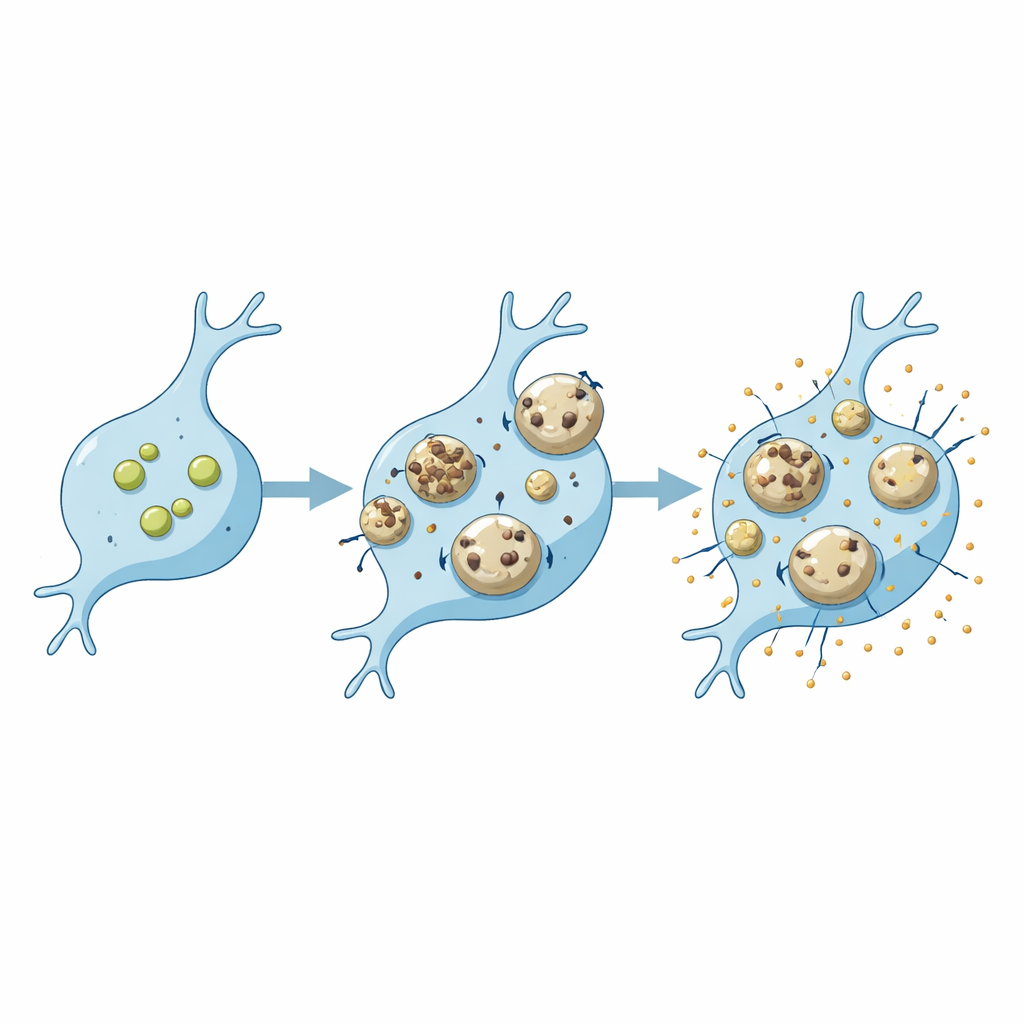
細胞ごとに異なる脆弱性
レビューは同じ遺伝的欠損がミクログリアとニューロンのリソソームに異なる影響を与えることを強調します。プログラニュリン、SORLA、C9ORF72のような認知症や運動ニューロン疾患に関連するタンパク質の欠失は、ミクログリアではあるパターンのリソソーム変化を、ニューロンでは別のパターンを引き起こします。ミクログリアにおいてはこれらの変化がアミロイドβやシナプスの破片などの貨物をどれだけ分解できるか、またどれほど強い炎症応答を示すかをしばしば変えます。リソソームはアミロイドβやα-シヌクレインのような粘着性の凝集体で満たされると物理的損傷を受けやすくなります。ミクログリアでは、こうした損傷が修復経路やリソソームを標的にした自己清掃(リソファジー)と呼ばれる保護機構を引き起こすことがあり、これらの防御が失敗すると漏出した酵素が細胞死とさらなる炎症を促します。証拠はミクログリアがニューロンよりもより頑強な修復手段を持つ可能性を示唆しますが、これが加齢や疾患でどのように変化するかはまだ調査中です。
ミクログリア内部に隠れた多様性
細胞種間の違いを超えて、ミクログリアは互いに、また単一細胞内でも著しい変異を示します。マウスやサルの老化脳での研究は、自己蛍光を示すリソソーム豊富な貯蔵物質の蓄積量によって区別される大きく二つのミクログリアクラスを明らかにしました。一方のサブセットは複雑な貯蔵体と高レベルのリソソームタンパク質・酵素を時間とともに蓄積し、非常に高齢になると数が減少します。個々のミクログリア内では、長い分枝過程のリソソームが細胞体内のものと異なり、局所的なシナプス刈り込みや髄鞘破片の処理という局所需要を反映します。著者らは未解決の問題を列挙します:休止状態のリソソームと活性化されたリソソームはどのように異なるのか、活性化が新しいリソソームの生成を引き起こすのか、CD68陽性リソソームはどのように特殊化しているのか、そして分泌に特化したリソソームプールと消化に専念するプールが存在するのか。これらの問いに答えるには高度なイメージングと分子ツールが必要ですが、脳の健康理解を深めることが期待されます。
これらの小さな区画が脳の健康にとって重要な理由
総じて本レビューは、ミクログリアのリソソームを清掃、代謝、免疫が精密に交差するハブとして描写します。これらの区画が正常に機能すると、ミクログリアは破片を除去し脅威を抑えることで静かに脳回路を維持します。過負荷、遺伝的障害、あるいは有毒な凝集体による物理的損傷が起きると、これらは保護的なリサイクルセンターから慢性的な炎症とニューロン損傷の源に変わり得ます。リソソームの制御ネットワーク、損傷応答、そして隠れた多様性を地図化することにより、将来の治療は有益なクリアランスを強化しつつ有害な炎症を抑えるようにこれらのシステムを選択的に増強または再バランスさせ、神経変性疾患の進行を遅らせるか予防する可能性があると著者らは主張しています。
引用: Somodji, E.A., Gowrishankar, S. “Micro-managing” immune activation and protein turnover: microglial lysosomes in the context of health and disease. npj Dement. 2, 35 (2026). https://doi.org/10.1038/s44400-026-00086-8
キーワード: ミクログリア, リソソーム, 神経炎症, アルツハイマー病, タンパク質凝集