Clear Sky Science · pt
“Microgerenciamento” da ativação imune e do turnover proteico: lisossomos microgliais no contexto da saúde e da doença
Observando a Equipe de Limpeza do Cérebro
Nas profundezas do cérebro, pequenas células imunes chamadas microglia atuam como zeladores e primeiros respondedores. Elas engolfam germes, células mortas e aglomerados de proteínas mal dobradas que podem se acumular com a idade ou em doenças como Alzheimer. Este artigo de revisão explora uma parte menos conhecida dessa história: o papel dos lisossomos microgliais, os “centros de reciclagem” internos da célula. Ao traçar como esses compartimentos são controlados, como mudam sob estresse e envelhecimento e como diferem entre tipos celulares, os autores mostram por que o ajuste fino dos lisossomos microgliais pode ser crucial para prevenir ou tratar doenças neurodegenerativas.
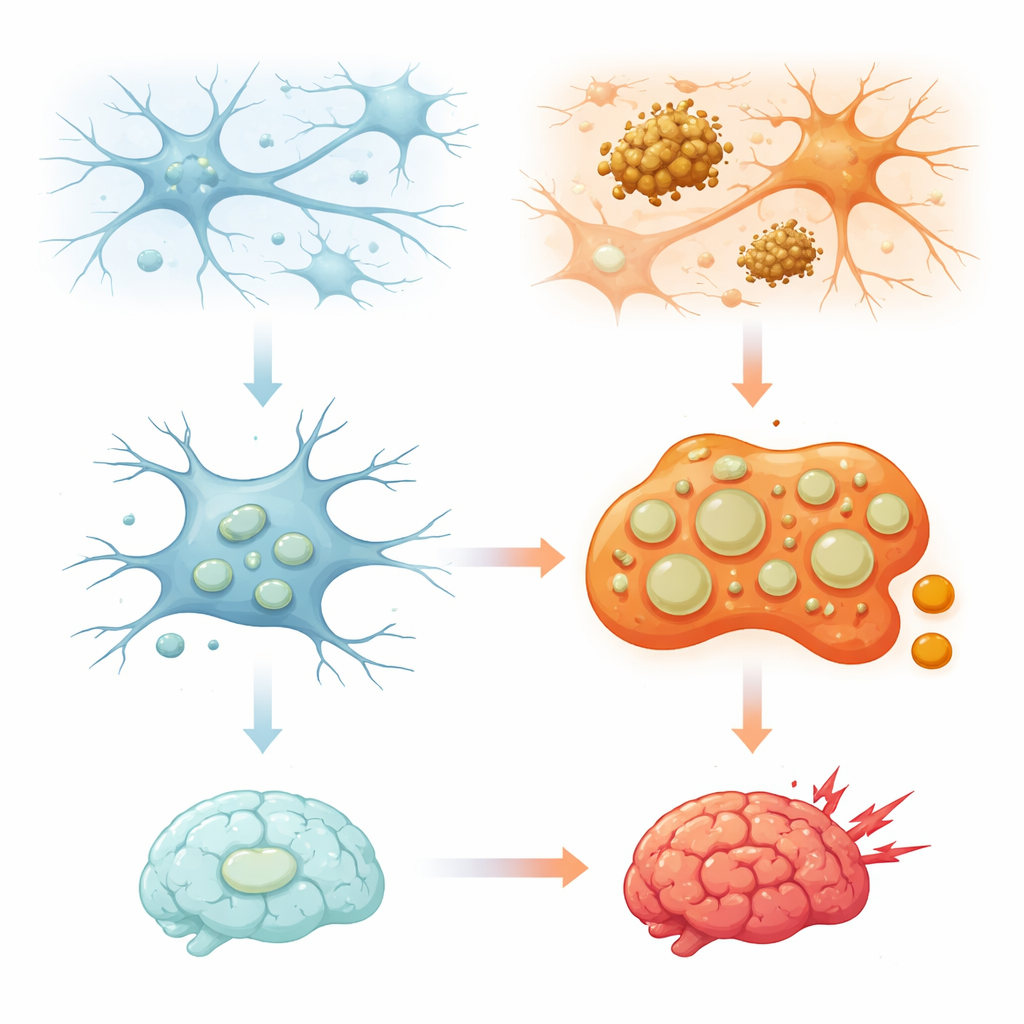
Como os Zeladores Cerebrais Usam Seus Recipientes de Reciclagem Internos
Os lisossomos há muito são vistos como simples lixeiras que degradam proteínas e organelas desgastadas. Na última década surgiu um quadro mais complexo: os lisossomos também detectam nutrientes, ajudam a controlar o uso de energia, moldam respostas imunes e até participam de decisões de morte celular. Nas microglia, que patrulham o cérebro continuamente, esses compartimentos são especialmente importantes porque lidam com grandes quantidades de material engolfado, desde micróbios até agregados proteicos e sinapses que precisam ser podadas. A revisão explica que os lisossomos microgliais não são todos iguais; eles formam subpopulações diferentes cuja composição, posição dentro da célula e comportamento mudam com estresse, envelhecimento e doença. Entender como essa diversidade é construída e mantida é essencial para compreender por que algumas regiões cerebrais ou tipos celulares são mais vulneráveis que outros.
Chaves que Regulam a Atividade dos Lisossomos
No nível genético, os lisossomos microgliais são controlados por uma rede de interruptores mestres, particularmente uma família de fatores de transcrição que inclui o TFEB. Quando as células estão estressadas ou sobrecarregadas, o TFEB se desloca para o núcleo e ativa um conjunto de genes que constroem mais lisossomos e aumentam sua atividade. Estudos em modelos de peixe-zebra e camundongo mostram que esse programa dirigido por TFEB é crucial para que as microglia migrem adequadamente, acidifiquem seus lisossomos e montem uma resposta imune forte contra agregados proteicos, como formas tóxicas da Tau. Outros reguladores atuam no sentido oposto. Por exemplo, uma enzima hiperativa ligada ao Parkinson, LRRK2, impede que esses fatores de transcrição entrem no núcleo em microglia e macrófagos, enfraquecendo a degradação lisossomal e potencialmente aumentando o risco de doença. Em conjunto, essas descobertas destacam uma disputa entre vias que potencializam a função lisossomal sob estresse e aquelas que a freiam para manter o equilíbrio do dia a dia.
Da Limpeza Protetora à Inflamação Nociva
Os lisossomos microgliais estão na encruzilhada entre remoção de resíduos e inflamação. Quando as microglia englobam substâncias que estimulam o sistema imune — como componentes bacterianos, amiloide-β ou outros agregados proteicos — seus lisossomos não apenas degradam esse material, mas também ajudam a ativar e liberar sinais inflamatórios. Proteases chamadas catepsinas, normalmente confinadas aos lisossomos, desempenham papéis centrais: ajudam a converter mensageiros imunes inativos em ativos, promovem a liberação de moléculas inflamatórias e, quando vazadas ou secretadas, podem até danificar neurônios próximos. Outra proteína lisossomal, CD68, é amplamente usada como marcador de microglia ativa e fagocítica e aumenta com o envelhecimento, estresse oxidativo e patologia de Alzheimer. Ainda assim, sua função exata na depuração e na inflamação permanece incerta. Importante, fármacos que restauram a acidez lisossomal ou anticorpos que engajam vias de depuração microglial podem acalmar a inflamação e melhorar a remoção de proteínas em modelos animais, sugerindo novas rotas terapêuticas.
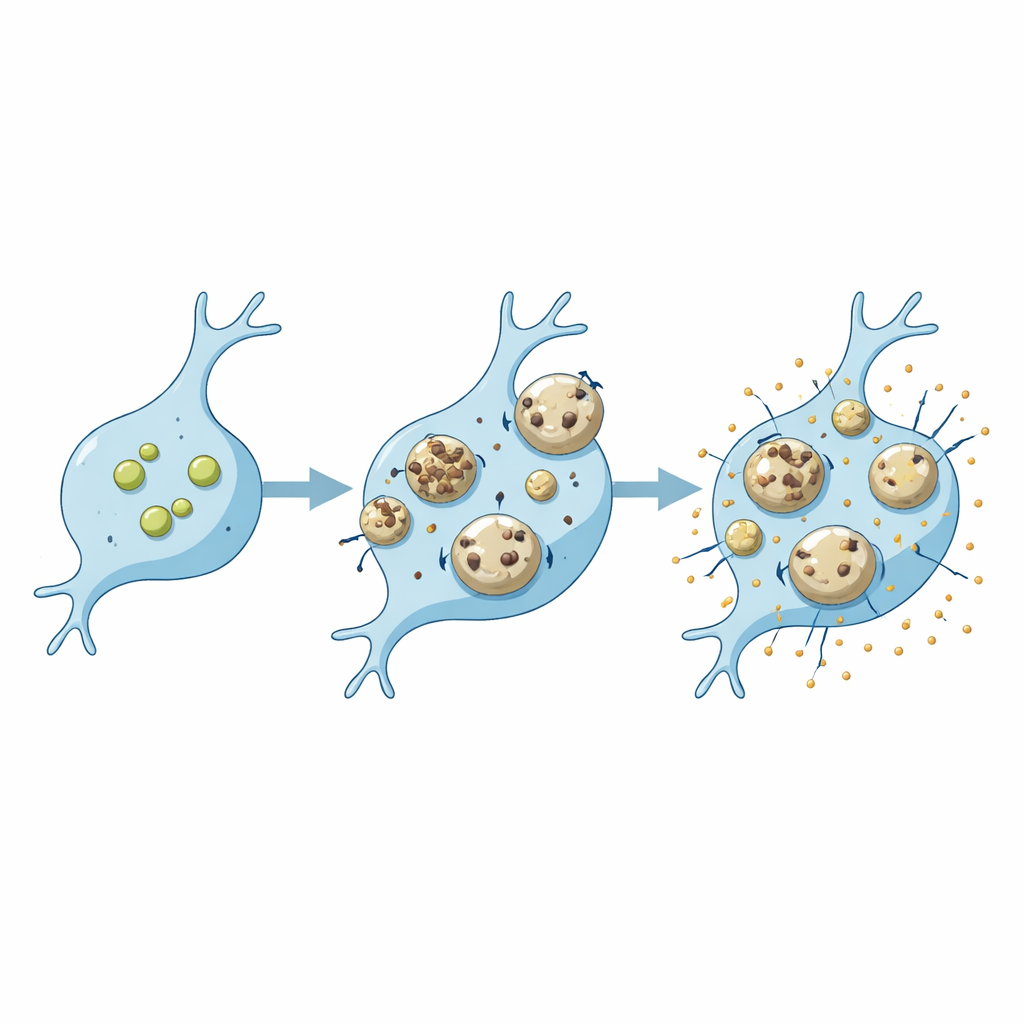
Cellulas Diferentes, Vulnerabilidades Diferentes
A revisão enfatiza que o mesmo defeito genético pode afetar os lisossomos microgliais e neurais de maneiras distintas. A perda de proteínas como progranulina, SORLA ou C9ORF72, todas ligadas à demência ou à doença do neurônio motor, leva a um padrão de alterações lisossomais em microglia e outro em neurônios. Nas microglia, essas alterações frequentemente mudam a eficiência com que degradam cargas como amiloide-β ou detritos sinápticos e a intensidade com que respondem com sinais inflamatórios. Os lisossomos também são suscetíveis a danos físicos quando estão carregados de agregados pegajosos como amiloide-β ou alfa-sinucleína. Nas microglia, tal dano pode desencadear vias protetoras de reparo e uma forma de autolimpeza direcionada chamada lisofagia; se essas salvaguardas falharem, enzimas vazadas podem provocar morte celular e inflamação adicional. Evidências sugerem que as microglia podem dispor de opções de reparo mais robustas do que os neurônios, mas como isso muda com a idade ou a doença ainda está sendo investigado.
Diversidade Oculta Dentro das Células Microgliais
Além das diferenças entre tipos celulares, as microglia mostram variação marcante entre si e até dentro de uma única célula. Estudos em cérebros envelhecidos de camundongos e macacos identificaram duas classes amplas de microglia distinguidas pela quantidade de material de armazenamento autofluorescente e rico em lisossomos que elas acumulam. Um subconjunto acumula corpos de armazenamento complexos e níveis elevados de proteínas e enzimas lisossomais ao longo do tempo, depois declina em número em idades muito avançadas. Dentro de microglia individuais, os lisossomos nos longos processos ramificados podem diferir daqueles no corpo celular, refletindo demandas locais por podar sinapses ou lidar com detritos de mielina. Os autores delineiam questões em aberto: como lisossomos em repouso e ativados diferem, se a ativação desencadeia o nascimento de novos lisossomos, como os lisossomos CD68-positivos são especializados e se alguns reservatórios lisossomais são dedicados à secreção enquanto outros se concentram na digestão. Responder a essas perguntas exigirá ferramentas avançadas de imagem e moleculares, mas promete aprofundar nossa compreensão da saúde cerebral.
Por Que Esses Pequenos Compartimentos Importam para a Saúde Cerebral
Em conjunto, a revisão retrata os lisossomos microgliais como centros finamente ajustados onde limpeza, metabolismo e imunidade se cruzam. Quando esses compartimentos funcionam bem, ajudam as microglia a manter silenciosamente os circuitos cerebrais ao remover detritos e conter ameaças. Quando estão sobrecarregados, geneticamente comprometidos ou fisicamente danificados por agregados tóxicos, podem se transformar de centros de reciclagem protetores em fontes de inflamação crônica e lesão neuronal. Ao mapear as redes regulatórias, respostas a danos e a diversidade oculta dos lisossomos microgliais, os autores argumentam que futuras terapias poderiam aumentar seletivamente ou reequilibrar esses sistemas — potencializando a depuração benéfica enquanto limitam a inflamação nociva — para retardar ou prevenir doenças neurodegenerativas.
Citação: Somodji, E.A., Gowrishankar, S. “Micro-managing” immune activation and protein turnover: microglial lysosomes in the context of health and disease. npj Dement. 2, 35 (2026). https://doi.org/10.1038/s44400-026-00086-8
Palavras-chave: microglia, lisossomos, neuroinflamação, doença de Alzheimer, agregação de proteínas