Clear Sky Science · pl
„Mikro‑zarządzanie” aktywacji odpornościowej i obrotu białek: lizosomy mikrogleju w kontekście zdrowia i choroby
Obserwowanie ekipy sprzątającej mózg
Głęboko w mózgu małe komórki odpornościowe zwane mikroglejem pełnią rolę sprzątaczy i pierwszych ratowników. Pożerają zarazki, martwe komórki i skupiska źle sfałdowanych białek, które mogą gromadzić się wraz z wiekiem lub w chorobach takich jak choroba Alzheimera. Ten artykuł przeglądowy bada mniej znany aspekt tej historii: rolę lizosomów mikrogleju, wewnętrznych „centrów recyklingu” komórki. Śledząc, jak te przedziały są regulowane, jak zmieniają się pod wpływem stresu i starzenia oraz jak różnią się między typami komórek, autorzy pokazują, dlaczego precyzyjne dostrajanie lizosomów mikrogleju może być kluczem do zapobiegania lub leczenia chorób neurodegeneracyjnych.
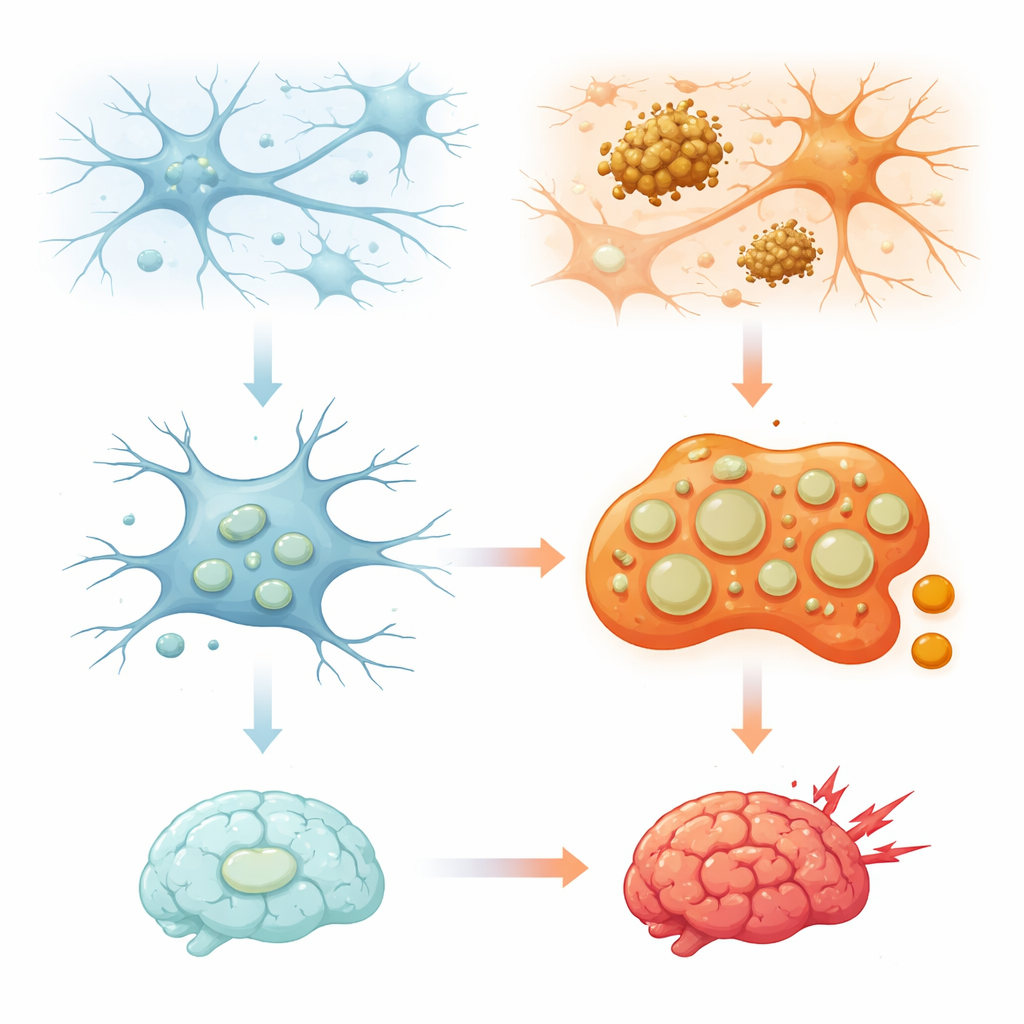
Jak mózgowi sprzątacze używają wewnętrznych pojemników na recykling
Lizosomy długo postrzegano jako proste kosze na śmieci, rozkładające zużyte białka i organelle. Ostatnia dekada odsłoniła bardziej złożony obraz: lizosomy także wyczuwają składniki odżywcze, pomagają kontrolować zużycie energii, kształtują odpowiedzi immunologiczne, a nawet uczestniczą w decyzjach o śmierci komórki. W mikrogleju, który nieustannie patroluje mózg, te przedziały są szczególnie ważne, ponieważ radzą sobie z dużą ilością pochłoniętego materiału — od drobnoustrojów po agregaty białek i synapsy wymagające przycinania. Przegląd wyjaśnia, że lizosomy mikrogleju nie są jednakowe; tworzą różne podpopulacje, których skład, położenie w komórce i zachowanie zmieniają się pod wpływem stresu, starzenia i choroby. Zrozumienie, jak powstaje i jest utrzymywana ta różnorodność, jest niezbędne, by pojąć, dlaczego niektóre obszary mózgu lub typy komórek są bardziej podatne niż inne.
Przełączniki zwiększające lub zmniejszające aktywność lizosomów
Na poziomie genetycznym lizosomy mikrogleju są kontrolowane przez sieć nadrzędnych przełączników, w szczególności rodzinę czynników transkrypcyjnych obejmującą TFEB. Gdy komórki są zestresowane lub przeciążone, TFEB przemieszcza się do jądra i włącza zestaw genów, które budują więcej lizosomów i zwiększają ich aktywność. Badania na modelach ryb Danio i myszach pokazują, że program prowadzony przez TFEB jest kluczowy, aby mikroglej mógł prawidłowo migrować, zakwaszać lizosomy i uruchamiać silną odpowiedź immunologiczną przeciw agregatom białek, takim jak toksyczne formy Tau. Inni regulatorzy działają w przeciwną stronę. Na przykład nadaktywna, sprzężona z chorobą Parkinsona kinaza LRRK2 zatrzymuje te czynniki transkrypcyjne poza jądrem w mikrogleju i makrofagach, osłabiając lizosomalny rozkład i potencjalnie zwiększając ryzyko choroby. Razem te odkrycia podkreślają przeciąganie liny między szlakami wzmacniającymi funkcję lizosomów w warunkach stresu a tymi, które ją tłumią, by utrzymać codzienną równowagę.
Od ochronnego sprzątania do szkodliwego zapalenia
Lizosomy mikrogleju leżą na skrzyżowaniu usuwania odpadów i zapalenia. Kiedy mikroglej pochłania substancje pobudzające układ odpornościowy — takie jak składniki bakteryjne, amyloid‑beta czy inne agregaty białek — jego lizosomy nie tylko degradują ten materiał, lecz także pomagają aktywować i uwalniać sygnały zapalne. Proteazy zwane katepsynami, zwykle ograniczone do lizosomów, odgrywają tu centralną rolę: pomagają przekształcać nieaktywne przekaźniki odpornościowe w formy aktywne, sprzyjają uwalnianiu cząsteczek zapalnych i gdy wyciekają lub są sekreowane, mogą uszkadzać pobliskie neurony. Inne białko lizosomalne, CD68, jest szeroko stosowane jako marker aktywnych, fagocytujących mikroglejów i nasila się wraz z wiekiem, stresem oksydacyjnym oraz patologią Alzheimera. Jego dokładna rola w oczyszczaniu i zapaleniu pozostaje jednak niejasna. Co istotne, leki przywracające kwasowość lizosomów lub przeciwciała angażujące szlaki oczyszczania mikrogleju potrafią uspokoić stan zapalny i poprawić usuwanie białek w modelach zwierzęcych, sugerując nowe kierunki terapeutyczne.
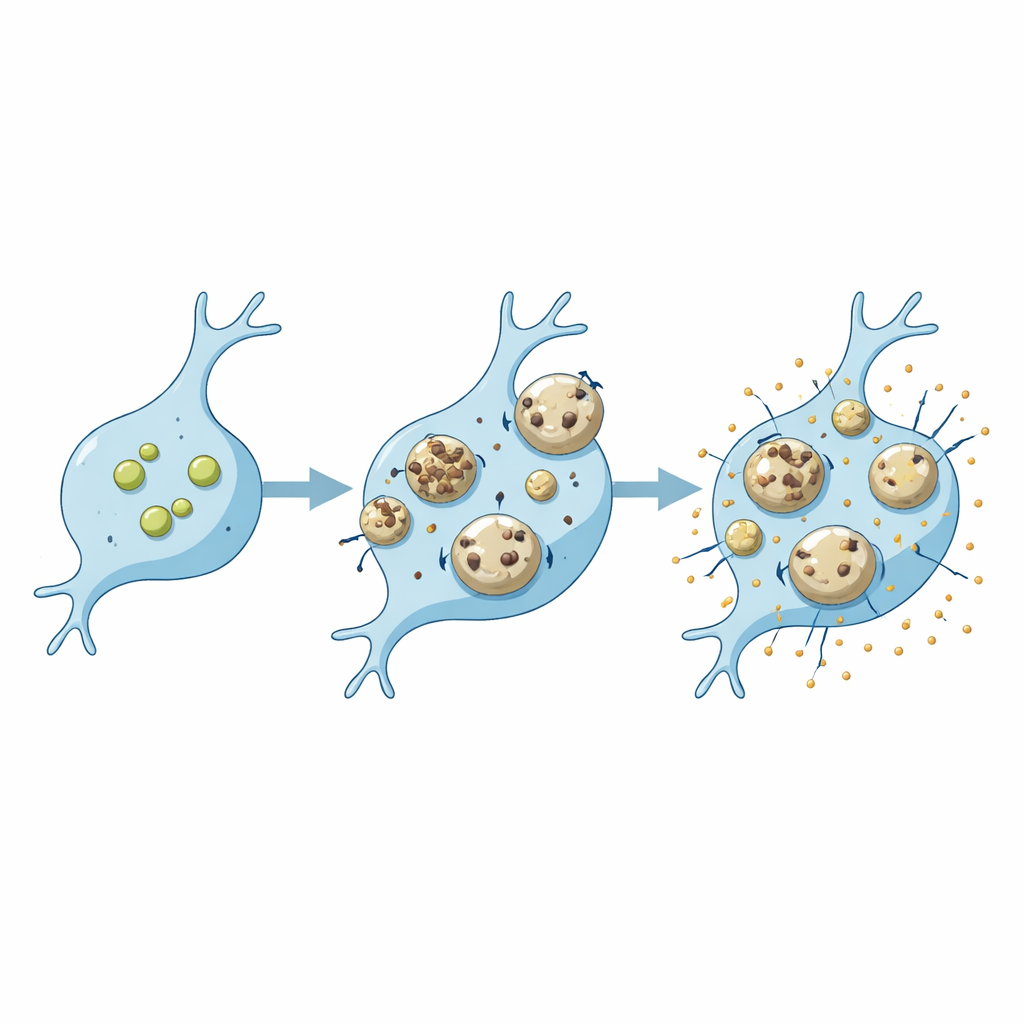
Różne komórki, różne podatności
Przegląd podkreśla, że ten sam defekt genetyczny może wpływać na lizosomy mikrogleju i neuronów w odmienny sposób. Utrata białek takich jak progranulina, SORLA czy C9ORF72, związanych z demencją lub chorobą neuronu ruchowego, prowadzi do jednego wzorca zmian lizosomalnych w mikrogleju i innego w neuronach. W mikrogleju te zmiany często zmieniają efektywność degradacji ładunku, takiego jak amyloid‑beta czy szczątki synaptyczne, oraz siłę odpowiedzi zapalnej. Lizosomy są też podatne na uszkodzenia fizyczne, gdy są zapchane lepkimi agregatami, takimi jak amyloid‑beta czy alfa‑synukleina. W mikrogleju takie uszkodzenia mogą uruchamiać ochronne szlaki naprawcze i formę ukierunkowanego samozmywania się zwaną lizofagią; jeśli te mechanizmy zawodzą, wyciekłe enzymy mogą wywołać śmierć komórek i dalsze zapalenie. Dane sugerują, że mikroglej może dysponować bardziej odpornymi opcjami naprawczymi niż neurony, lecz jak to się zmienia z wiekiem lub w chorobie, pozostaje wciąż badane.
Ukryta różnorodność wewnątrz komórek mikrogleju
Ponad różnicami między typami komórek, mikroglej wykazuje uderzającą zmienność między poszczególnymi komórkami, a nawet wewnątrz pojedynczej komórki. Badania w starzejących się mózgach myszy i małp odkryły dwie szerokie klasy mikrogleju, rozróżniane przez ilość autofluorescencyjnego, bogatego w lizosomy materiału magazynowego, który się w nich gromadzi. Jedna podgrupa buduje złożone ciała magazynowe i wysokie poziomy białek oraz enzymów lizosomalnych z czasem, a następnie maleje liczebnie w bardzo podeszłym wieku. W obrębie pojedynczych mikroglejów lizosomy w długich rozgałęzionych wypustkach mogą różnić się od tych w ciele komórkowym, odzwierciedlając lokalne potrzeby związane z przycinaniem synaps lub usuwaniem resztek osłonki mielinowej. Autorzy wyliczają otwarte pytania: jak różnią się lizosomy w stanie spoczynku i aktywacji, czy aktywacja inicjuje powstawanie nowych lizosomów, jak wyspecjalizowane są lizosomy pozytywne względem CD68 i czy niektóre pule lizosomalne są przeznaczone do sekrecji, podczas gdy inne koncentrują się na trawieniu. Odpowiedzi na te pytania będą wymagać zaawansowanych narzędzi obrazowania i molekularnych, ale obiecują pogłębienie naszej wiedzy o zdrowiu mózgu.
Dlaczego te maleńkie przedziały mają znaczenie dla zdrowia mózgu
W sumie przegląd przedstawia lizosomy mikrogleju jako precyzyjnie dostrojone węzły, gdzie przecinają się sprzątanie, metabolizm i odporność. Gdy te przedziały funkcjonują prawidłowo, pomagają mikroglejowi cicho utrzymywać obwody mózgowe poprzez usuwanie odpadów i ograniczanie zagrożeń. Gdy są przeciążone, genetycznie upośledzone lub fizycznie uszkodzone przez toksyczne agregaty, mogą przełączyć się z ochronnych centrów recyklingu w źródła przewlekłego zapalenia i uszkodzeń neuronów. Mapując sieci regulacyjne, reakcje na uszkodzenia i ukrytą różnorodność lizosomów mikrogleju, autorzy argumentują, że przyszłe terapie mogłyby selektywnie wzmacniać lub przywracać równowagę tych systemów — zwiększając korzystne oczyszczanie przy jednoczesnym ograniczeniu szkodliwego zapalenia — aby spowolnić lub zapobiec chorobom neurodegeneracyjnym.
Cytowanie: Somodji, E.A., Gowrishankar, S. “Micro-managing” immune activation and protein turnover: microglial lysosomes in the context of health and disease. npj Dement. 2, 35 (2026). https://doi.org/10.1038/s44400-026-00086-8
Słowa kluczowe: mikroglej, lizosomy, neurozapalanie, choroba Alzheimera, agregacja białek