Clear Sky Science · es
“Microgestión” de la activación inmune y el recambio proteico: los lisosomas microgliales en el contexto de la salud y la enfermedad
Vigilando el equipo de limpieza del cerebro
En lo profundo del cerebro, pequeñas células inmunitarias llamadas microglía actúan como conserjes y primeros intervinientes. Ingeran gérmenes, células muertas y conglomerados de proteínas mal plegadas que pueden acumularse con la edad o en enfermedades como el Alzheimer. Este artículo de revisión explora una parte menos conocida de esa historia: el papel de los lisosomas microgliales, los “centros de reciclaje” internos de la célula. Al rastrear cómo se controlan estos compartimentos, cómo cambian con el estrés y el envejecimiento, y cómo difieren entre tipos celulares, los autores muestran por qué afinar los lisosomas microgliales podría ser clave para prevenir o tratar las enfermedades neurodegenerativas.
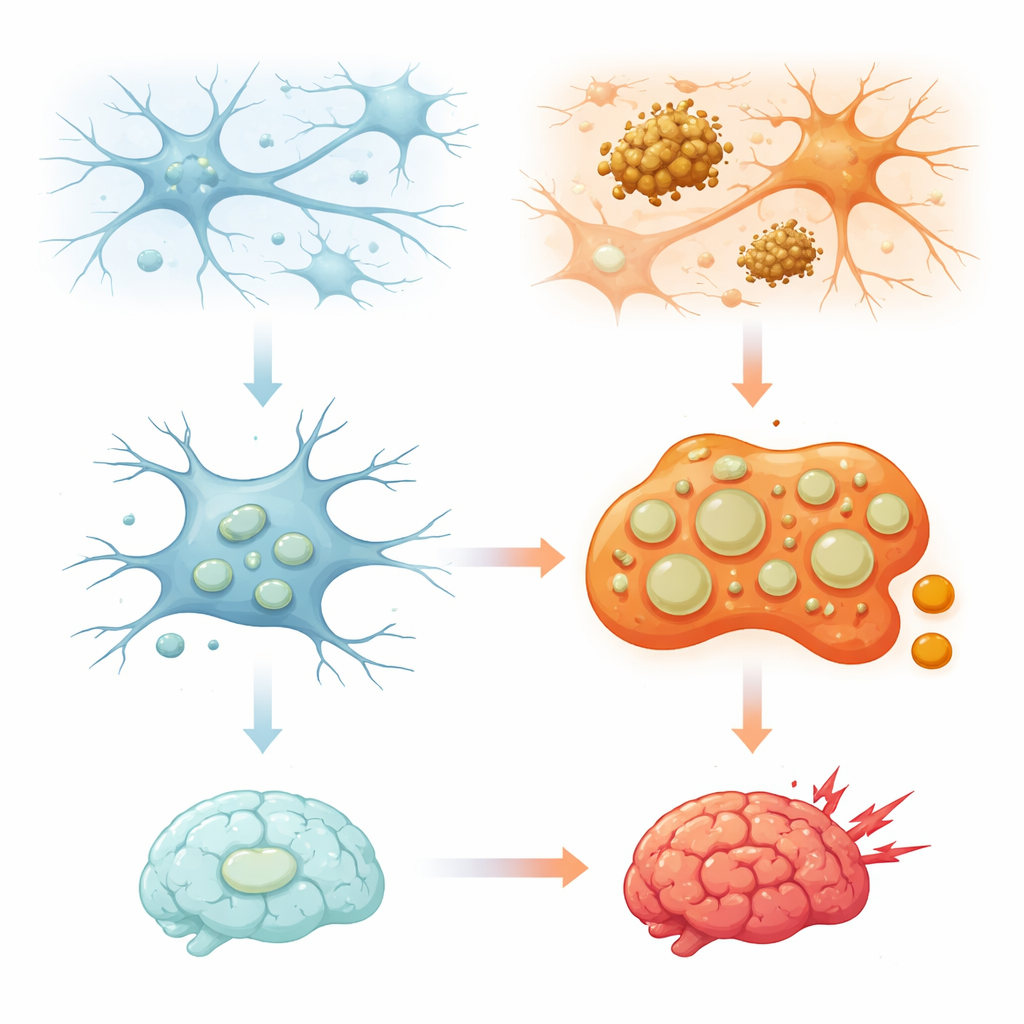
Cómo usan los conserjes cerebrales sus contenedores de reciclaje internos
Durante mucho tiempo se consideró a los lisosomas como simples botes de basura que degradan proteínas y orgánulos desgastados. La última década ha mostrado un panorama más complejo: los lisosomas también detectan nutrientes, ayudan a controlar el uso de energía, moldean respuestas inmunitarias e incluso participan en decisiones de muerte celular. En las microglías, que patrullan constantemente el cerebro, estos compartimentos son especialmente importantes porque manejan grandes cantidades de material ingerido, desde microbios hasta agregados proteicos y sinapsis que necesitan poda. La revisión explica que los lisosomas microgliales no son todos iguales; forman subpoblaciones distintas cuya composición, posición dentro de la célula y comportamiento cambian con el estrés, el envejecimiento y la enfermedad. Comprender cómo se construye y mantiene esa diversidad es esencial para entender por qué algunas regiones cerebrales o tipos celulares son más vulnerables que otras.
Interruptores que aumentan o reducen la actividad lisosomal
A nivel genético, los lisosomas microgliales están controlados por una red de interruptores maestros, en particular una familia de factores de transcripción que incluye a TFEB. Cuando las células están estresadas o sobrecargadas, TFEB se traslada al núcleo y activa un conjunto de genes que generan más lisosomas y aumentan su actividad. Estudios en modelos de pez cebra y ratón muestran que este programa impulsado por TFEB es crucial para que las microglías migren adecuadamente, acidifiquen sus lisosomas y monten una respuesta inmune fuerte contra agregados proteicos como las formas tóxicas de la proteína Tau. Otros reguladores actúan en sentido opuesto. Por ejemplo, una enzima hiperactiva vinculada al Parkinson, LRRK2, mantiene a estos factores de transcripción fuera del núcleo en microglías y macrófagos, debilitando la degradación lisosomal y potencialmente aumentando el riesgo de enfermedad. En conjunto, estos hallazgos resaltan una pugna entre vías que potencian la función lisosomal bajo estrés y otras que la restringen para mantener el equilibrio cotidiano.
De la limpieza protectora a la inflamación dañina
Los lisosomas microgliales se sitúan en la intersección entre la eliminación de desechos y la inflamación. Cuando las microglías engullen sustancias estimulantes del sistema inmune —como componentes bacterianos, beta-amiloide u otros agregados proteicos—, sus lisosomas no solo degradan ese material sino que también ayudan a activar y liberar señales inflamatorias. Proteasas llamadas catepsinas, normalmente confinadas dentro de los lisosomas, desempeñan papeles centrales: ayudan a convertir mensajeros inmunes inactivos en activos, promueven la liberación de moléculas inflamatorias y, cuando se filtran o secretan, pueden incluso dañar neuronas cercanas. Otra proteína lisosomal, CD68, se usa ampliamente como marcador de microglía activa y fagocítica y aumenta con la edad, el estrés oxidativo y la patología del Alzheimer. Sin embargo, su función exacta en la limpieza y la inflamación sigue sin aclararse. Es importante destacar que fármacos que restauran la acidez lisosomal o anticuerpos que activan vías de eliminación microglial pueden calmar la inflamación y mejorar la remoción de proteínas en modelos animales, lo que apunta a nuevas vías terapéuticas.
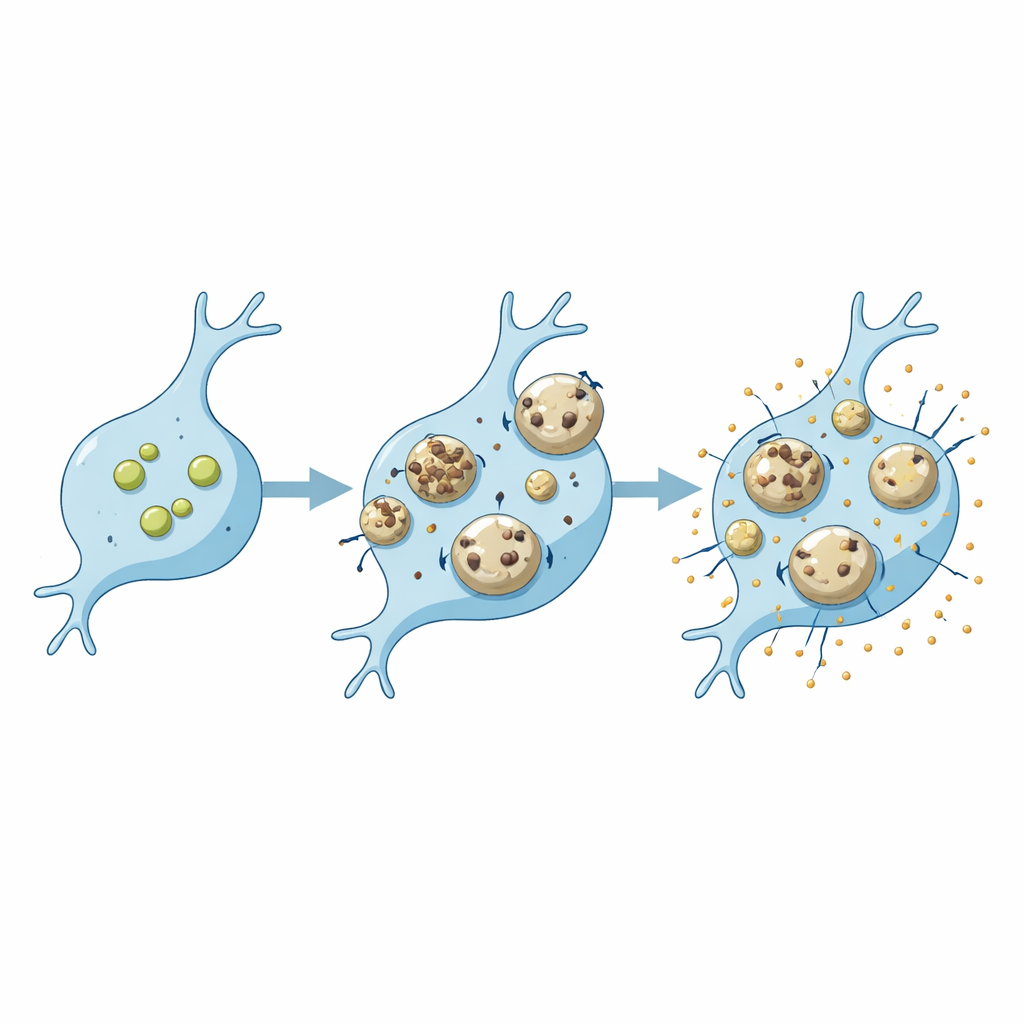
Diferentes células, diferentes vulnerabilidades
La revisión enfatiza que el mismo defecto genético puede afectar a los lisosomas microgliales y neuronales de formas distintas. La pérdida de proteínas como progranulina, SORLA o C9ORF72, todas vinculadas con demencia o enfermedades de la motoneurona, conduce a un patrón de cambios lisosomales en microglías y otro en neuronas. En microglías, estos cambios a menudo alteran la eficacia para degradar cargas como beta-amiloide o restos sinápticos y la intensidad de la respuesta inflamatoria. Los lisosomas también son proclives a sufrir daño físico cuando se llenan de agregados pegajosos como beta-amiloide o alfa-sinucleína. En microglías, dicho daño puede desencadenar vías de reparación protectoras y una forma de limpieza selectiva llamada lisofagia; si estas salvaguardas fallan, enzimas filtradas pueden inducir muerte celular y agravar la inflamación. La evidencia sugiere que las microglías pueden disponer de opciones de reparación más robustas que las neuronas, pero cómo cambia esto con la edad o la enfermedad sigue siendo objeto de investigación.
Diversidad oculta dentro de las células microgliales
Más allá de las diferencias entre tipos celulares, las microglías muestran una variación sorprendente entre ellas e incluso dentro de una sola célula. Trabajos en cerebros envejecidos de ratones y monos han descubierto dos clases amplias de microglías distinguibles por la cantidad de material autofluorescente rico en lisosomas que acumulan. Un subconjunto acumula cuerpos de almacenamiento complejos y altos niveles de proteínas y enzimas lisosomales con el tiempo, para luego disminuir en número en edades muy avanzadas. Dentro de microglías individuales, los lisosomas en los largos procesos ramificados pueden diferir de los del soma, reflejando demandas locales para podar sinapsis o manejar restos de mielina. Los autores plantean preguntas abiertas: cómo difieren los lisosomas en reposo y activados, si la activación dispara el nacimiento de nuevos lisosomas, cómo se especializan los lisosomas CD68-positivos y si algunos reservorios lisosomales están dedicados a la secreción mientras otros se centran en la digestión. Responder estas preguntas requerirá herramientas moleculares e imágenes avanzadas, pero promete profundizar nuestro entendimiento de la salud cerebral.
Por qué estos pequeños compartimentos importan para la salud del cerebro
En conjunto, la revisión presenta a los lisosomas microgliales como centros finamente afinados donde convergen limpieza, metabolismo e inmunidad. Cuando estos compartimentos funcionan bien, ayudan a las microglías a mantener discretamente los circuitos cerebrales al eliminar desechos y contener amenazas. Cuando están sobrecargados, genéticamente dañados o físicamente lesionados por agregados tóxicos, pueden pasar de centros de reciclaje protectores a fuentes de inflamación crónica y daño neuronal. Al cartografiar las redes regulatorias, las respuestas al daño y la diversidad oculta de los lisosomas microgliales, los autores sostienen que futuras terapias podrían potenciar o reequilibrar selectivamente estos sistemas —mejorando la eliminación beneficiosa mientras limitan la inflamación perjudicial— para ralentizar o prevenir las enfermedades neurodegenerativas.
Cita: Somodji, E.A., Gowrishankar, S. “Micro-managing” immune activation and protein turnover: microglial lysosomes in the context of health and disease. npj Dement. 2, 35 (2026). https://doi.org/10.1038/s44400-026-00086-8
Palabras clave: microglía, lisosomas, neuroinflamación, enfermedad de Alzheimer, agregación de proteínas