Clear Sky Science · tr
Ölümsüzleştirilmiş dorsal kök ganglionu nöron hücre hattı F11'de voltaj kapılı kalsiyum kanallarının nöronal farklılaşmanın temel düzenleyicileri olarak rolü
Sinir sağlığı için küçük kalsiyum kapılarının önemi
Beynimiz ve sinirlerimiz, elektrik sinyalleri ile kimyasal haberciler arasındaki hassas bir dengeye dayanır. En önemlilerinden biri, hücre zarındaki küçük geçitlerin kalsiyum iyonlarının içeri akmasına izin vermesidir. Bu çalışma, voltaj kapılı kalsiyum kanalları olarak adlandırılan bu geçit ailesinin olgunlaşmamış sinir benzeri hücrelerin daha olgun, nöron benzeri hücrelere dönüşmesine nasıl yardımcı olduğunu ve bu kanallar aracılığıyla aşırı aktivitenin hücrelere zarar vererek işlevlerini bozabileceğini inceliyor. Bu dengenin anlaşılması, sinir hücrelerinin sıklıkla stres altında olduğu veya öldüğü kronik ağrı ve nörodejeneratif hastalıkların tedavisi için yeni yollar açabilir.
Basit hücrelerden dallanan sinir benzeri ağlara
Araştırmacılar, omurilik duyusal nöronlarının özellikleriyle bir kanser hücre hattının özelliklerini karıştıran yaygın bir laboratuvar modeli olan F11 hücreleri ile çalıştı. Normal koşullarda F11 hücreleri bölünür ve oldukça basit görünür. cAMP adlı bir haberciyi artıran bir kokteyle maruz kaldıklarında bölünmeyi durdurur ve gerçek duyusal nöronlara daha çok benzeyen davranışlar göstermeye başlar; uzun uzantılar olan nöritler büyür. Ekip, bu geçiş sırasında hücrelerin potasyum ile kısa süreli depolarize edildiklerinde daha güçlü kalsiyum dalgalanmaları gösterdiğini ve daha fazla spontan elektriksel çıkış ürettiğini doğruladı. Başka bir ifadeyle, hücreler olgunlaştıkça elektriksel ve kalsiyum sinyalleşme makineleri daha aktif hale geldi; bu, gerçek sinir hücrelerinin gelişiminde görülenlerle paraleldir.
Büyümeyi yöneten kalsiyum kanalları
Hangi kalsiyum kanallarının sorumlu olduğunu belirlemek için bilim insanları farklı kanal alt tiplerini kodlayan genlerin aktivitesini ölçtü. F11 hücreleri farklılaştıkça sekiz kanal tipinin daha bol bulunduğunu ve özellikle CaV1.3 olarak bilinen belirli bir L-tipi kanal geninde çarpıcı bir artış olduğunu keşfettiler. L-tipi kanalları seçici olarak bloke eden ilaçları kullanarak, bu kanalları 72 saatlik farklılaşma süresi boyunca kapatmanın potasyumla indüklenen kalsiyum sinyallerini keskin şekilde azalttığını ve nöritleri kısalttığını, ancak hücreleri öldürmediğini gösterdiler. Sinaptik iletimde rol oynayan çeşitli yüksek voltajlı kanallara veya T-tipi kanallara yönelik diğer kanal engelleyicilerinin ise küçük etkileri oldu. Görüntüleme, iki L-tipi kanalın — CaV1.2 ve özellikle CaV1.3 — farklılaşmış hücrelerin yüzeyinde daha bol olduğunu doğrulayarak bu kanalların nöron benzeri özelliklerin inşasına yardımcı kalsiyum sinyallerinin ana iticileri olduğu fikrini destekledi.
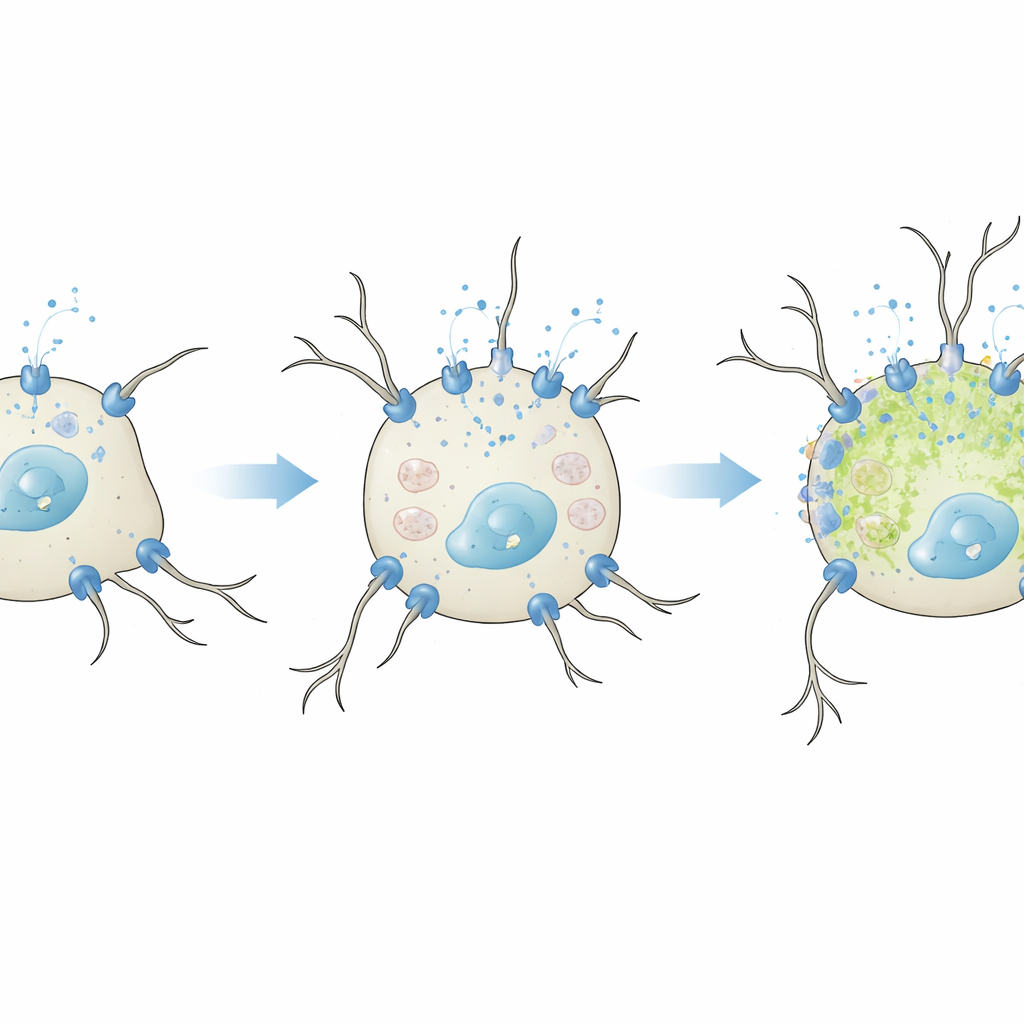
Yararlı kalsiyumun zararlıya dönüştüğü an
Ardından ekip, bu L-tipi kanalların yapay olarak artırılması durumunda ne olduğunu sordu. Azalmış serum ile hafif, farklılaştırmayan koşullar altında ek CaV1.2 veya CaV1.3 eklemek, hücrelerin potasyuma daha güçlü yanıt vererek daha büyük kalsiyum dalgalanmaları göstermesine yol açtı. Ancak yalnızca CaV1.3, nörit büyümesini artırdı; bu, önceki çalışmalarda bu alt tipin nöronlarda büyüme ile ilişkili yolakları özellikle iyi etkinleştirdiğini öne süren bulgularla tutarlı. Önemli olarak, bu aşamada oksidatif stres belirteçlerinde artış görülmedi; bu da orta düzeyde kalsiyum girişinin nöronal özellikleri güvenle teşvik edebileceğini gösteriyor. Tam farklılaşma koşulları altında tablo değişti. Hücreler zaten olgunlaşmaya zorlanırken CaV1.2 veya CaV1.3 fazla üretildiğinde, nöritler kısaldı ve hücrelerde reaksiyon veren oksijen türleri birikti — bu oksidatif hasarın bir göstergesi. Etki en güçlü şekilde, daha düşük voltajlarda aktive olan ve uzun süreli kalsiyum girişini destekleyebilen CaV1.3 için gözlendi.
Büyüme ile zarar arasındaki ince çizgi
Birlikte değerlendirildiğinde, sonuçlar bu duyusal nöron benzeri modelde L-tipi kalsiyum kanallarının iki uçlu bir rolünü ortaya koyuyor. CaV1.2 ve CaV1.3'ün normal düzeyde yükselmesi, F11 hücrelerinin önemli nöronal özellikler kazanması için gerekli gibi görünüyor: daha uzun nöritler, daha güçlü kalsiyum yanıtları ve daha aktif elektriksel sinyalleşme. Yine de bu kanalları, özellikle zaten kalsiyumla dolu bir ortamda CaV1.3'ü aşırı derecede zorlamak, dengeyi oksidatif strese ve olgunlaşmanın durmasına doğru kaydırıyor. Destekleyici ile zararlı kalsiyum sinyalleşmesi arasındaki bu denge, kanal aktivitesi ve oksidatif stresin sıklıkla bozulduğu nöropatik ağrı ve nörodejeneratif hastalıklar gibi durumlarla yakından ilişkilidir. F11 hücreleri, ağrı algılayan nöronların birçok özelliğini taklit ettiği ve otomatik görüntüleme ile kalsiyum ölçümleriyle incelenebildiği için, bu çalışma kalsiyum girişini ince ayar yapmayı ve savunmasız sinirleri korumayı hedefleyen gelecekteki ilaçlar için pratik bir test ortamı olarak değerlerini güçlendiriyor.
Atıf: López, D., Brea, J., Barro, M. et al. Voltage-gated calcium channels as key regulators of neuronal differentiation in the immortalized dorsal root ganglion neuronal cell line F11. Sci Rep 16, 14621 (2026). https://doi.org/10.1038/s41598-026-44595-1
Anahtar kelimeler: kalsiyum sinyalleşmesi, nöronal farklılaşma, voltaj kapılı kalsiyum kanalları, nöropatik ağrı, oksidatif stres