Clear Sky Science · sv
Spänningsstyrda kalciumkanaler som nyckelregulatorer av neuronal differentiering i den odödliga dorsalrotsganglion-neuronala cellinjen F11
Varför små kalciumportar spelar roll för nervhälsa
Våra hjärnor och nerver är beroende av en känslig balans mellan elektriska signaler och kemiska budbärare. Bland de viktigaste är små portar i cellmembranet som släpper in kalciumjoner. Denna studie undersöker hur en familj av dessa portar, kallade spänningsstyrda kalciumkanaler, hjälper omogna nervliknande celler att utvecklas till mer mogna, neuronlika celler — och hur överdriven aktivitet genom dessa kanaler kan slå tillbaka och skada cellerna. Att förstå denna balans kan öppna nya vägar för behandling av kronisk smärta och neurodegenerativa sjukdomar, där nervceller ofta är utsatta för stress eller dör.
Från enkla celler till förgrenade nervliknande nätverk
Forskarna arbetade med F11-celler, en i laboratorier ofta använd modell som kombinerar egenskaper från ryggmärgens sensoriska neuroner med en cancercellinje. Under normala förhållanden delar sig F11-celler och ser ganska enkla ut. När de exponeras för en cocktail som höjer budbärarmolekylen cAMP slutar de dela sig och börjar bete sig mer som verkliga sensoriska neuroner, genom att växa långa utskott kallade neuriter. Teamet bekräftade att cellerna under denna övergång uppvisade starkare kalciumpikar när de kortvarigt depolariserades med kalium, och att de fyrade fler spontana elektriska spikar. Med andra ord, i takt med att cellerna mognade blev deras elektriska och kalciumsignaliserande maskineri mer aktivt, vilket speglar vad som händer under utvecklingen av riktiga nervceller.
Kalciumkanaler som tillväxtomkopplare
För att ta reda på vilka kalciumkanaler som var ansvariga mätte forskarna aktiviteten hos gener som kodar för olika kanalundergrupper. De upptäckte att åtta typer av kanaler blev mer förekommande när F11-celler differentierades, med en markant ökning av genen för en särskild L-typkanal känd som CaV1.3. Med hjälp av läkemedel som selektivt blockerar L-typkanaler visade de att blockering av dessa kanaler under den 72 timmar långa differentieringsperioden kraftigt minskade kalciumsignalerna som utlösts av kalium och förkortade neuriterna, utan att döda cellerna. Andra kanalblockerare, inriktade på T-typ eller olika högspänningskanaler involverade i synaptisk transmission, hade liten effekt. Avbildning bekräftade att två L-typkanaler, CaV1.2 och särskilt CaV1.3, var mer rikligt förekommande på ytan av differentierade celler, vilket stöder idén att dessa kanaler är nyckeldrivkrafter för de kalciumsignaler som hjälper till att bygga neuronlika egenskaper.
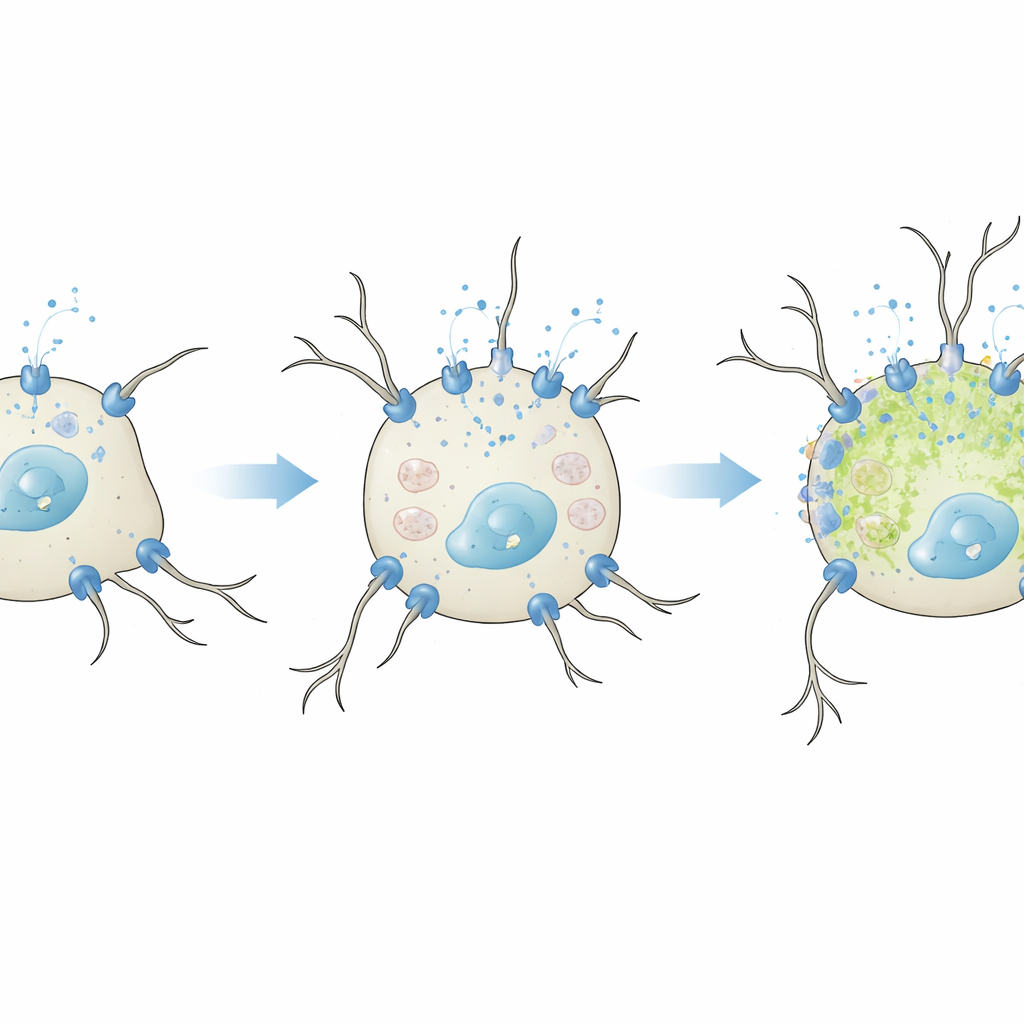
När hjälpsamt kalcium blir skadligt
Teamet frågade sedan vad som händer om dessa L-typkanaler förstärks artificiellt. Under milda, icke-differentierande förhållanden med reducerat serum gjorde extra CaV1.2 eller CaV1.3 att cellerna svarade starkare på kalium med större kalciumpikar. Endast CaV1.3 förbättrade dock neuritutväxten, i linje med tidigare arbete som antyder att denna undergrupp är särskilt bra på att aktivera tillväxtrelaterade signalvägar i neuroner. Viktigt är att det i detta skede inte fanns någon ökning av markörer för oxidativ stress, vilket visar att en måttlig ökning av kalciuminflöde kan främja neuronala egenskaper på ett säkert sätt. Bilden förändrades under fulla differentieringsförhållanden. När CaV1.2 eller CaV1.3 överproducerades medan cellerna redan trycktes mot mognad, blev neuriterna kortare och cellerna ackumulerade fler reaktiva syreradikaler — ett tecken på oxidativ skada. Effekten var starkast för CaV1.3, som aktiveras vid lägre spänningar och kan stödja förlängt kalciuminflöde.
En tunn linje mellan tillväxt och skada
Sammantaget visar resultaten en dubbelriktad roll för L-typkalciumkanaler i denna modell av sensoriska neuronlika celler. Normal uppreglering av CaV1.2 och CaV1.3 verkar nödvändig för att F11-celler ska skaffa sig viktiga neuronala egenskaper: längre neuriter, starkare kalciumsvar och mer aktiv elektrisk signalering. Ändå leder en överdriven stimulering av dessa kanaler, särskilt CaV1.3 i en redan kalciumfylld miljö, till oxidativ stress och hämmad mognad. Denna balans mellan stödjande och skadlig kalciumsignalering är högt relevant för tillstånd som neuropatisk smärta och neurodegenerativ sjukdom, där både kanalaktivitet och oxidativ stress ofta är störda. Eftersom F11-celler efterliknar många egenskaper hos smärtkänsliga neuroner och kan undersökas med automatiserad avbildning och kalciummätningar, stärker detta arbete deras värde som ett praktiskt testunderlag för framtida läkemedel som syftar till att finjustera kalciuminflöde och skydda sårbara nerver.
Citering: López, D., Brea, J., Barro, M. et al. Voltage-gated calcium channels as key regulators of neuronal differentiation in the immortalized dorsal root ganglion neuronal cell line F11. Sci Rep 16, 14621 (2026). https://doi.org/10.1038/s41598-026-44595-1
Nyckelord: kalciumsignalering, neuronal differentiering, spänningsstyrda kalciumkanaler, neuropatisk smärta, oxidativ stress