Clear Sky Science · he
ערוצי סידן שמופעלים במתח כמתאמים מרכזיים של התماיינות נוירונית בקו התאים הנוירוני הבלתי-מתכלה F11 של גנגליון השורש הגבי
למה שערי סידן זעירים חשובים לבריאות העצבים
המוחות והעצבים שלנו נשענים על מאזן עדין של אותות חשמליים ומוליכים כימיים. בין החשובים שבהם נמצאים שערים זעירים בממברנת התא שמאפשרים ליוני סידן לשטוף פנימה. מחקר זה בוחן כיצד משפחה אחת של שערים אלה, שנקראת ערוצי סידן שמופעלים במתח, מסייעת לתאים לא בשלים בדמויית עצב להתפתח לתאים דמויי-נוירונים בשלים יותר — וכיצד פעילות מופרזת בערוצים אלה עלולה לחזור כבומרנג ולפגוע בתאים. הבנת האיזון הזה עשויה לפתוח דרכים חדשות לטיפול בכאב כרוני ובמחלות ניווניות עצביות, שבהן תאי עצב נמצאים לעתים קרובות במצוקה או מתים.
מתאים פשוטים לרשתות ענפיות בדמות עצב
החוקרים עבדו עם תאי F11, מודל מעבדה נפוץ שמשלב תכונות של נוירונים תחושתיים ספינליים וקו תאי סרטן. בתנאים רגילים תאי F11 מתחלקים ונראים די פשוטים. כאשר הם חשופים לתמהיל שמעלה את מולקולת המשדר cAMP, הם מפסיקים להתחלק ומתחילים להתנהג יותר כמו נוירונים תחושתיים אמיתיים, וגדלים תיצאולים ארוכים הידועים כנויריטים. הצוות אישר שבמהלך המעבר הזה התאים הציגו גליצות סידן חזקות יותר כאשר הודפו בקצרה עם אשלגן, וירו יותר צפיצות חשמליות ספונטניות. במילים אחרות, ככל שהתאים הבשילו, המכונות החשמליות והסיגנליות של הסידן הפכו פעיליות יותר, מה שמשקף את מה שמתרחש במהלך התפתחות תאי עצב אמיתיים.
ערוצי סידן כמתגי גדילה
כדי לגלות אילו ערוצי סידן אחראים, המדענים מדדו את פעילות הגנים המקודדים תתי-סוגים שונים של ערוצים. הם מצאו שמונה סוגי ערוצים הפכו לשכיחים יותר ככל שתאי F11 התמיינו, עם עלייה בולטת בגן של ערוץ מסוג L ידוע כ-CaV1.3. באמצעות תרופות החוסמות באופן סלקטיבי ערוצי L-type, הם הראו שכיבוי ערוצים אלה במהלך תקופת ההתמיינות של 72 שעות הקטין בצורה חדה את אותות הסידן המעוררים על-ידי אשלגן וקיצר את הנויריטים, מבלי להרוג את התאים. חוסמי ערוצים אחרים, שפנו לערוצי T-type או לערוצים שונים המופעלים במתח גבוה המעורבים בהעברה סינפטית, לא גרמו להשפעה משמעותית. הדמיה אישרה ששני ערוצי L-type, CaV1.2 ובייחוד CaV1.3, היו שופעים יותר על פני שטח התאים המותמיינים, ותומכת ברעיון שאלה ערוצים מרכזיים ליצירת אותות הסידן המסייעים לבניית התכונות הדמויות-נוירון.
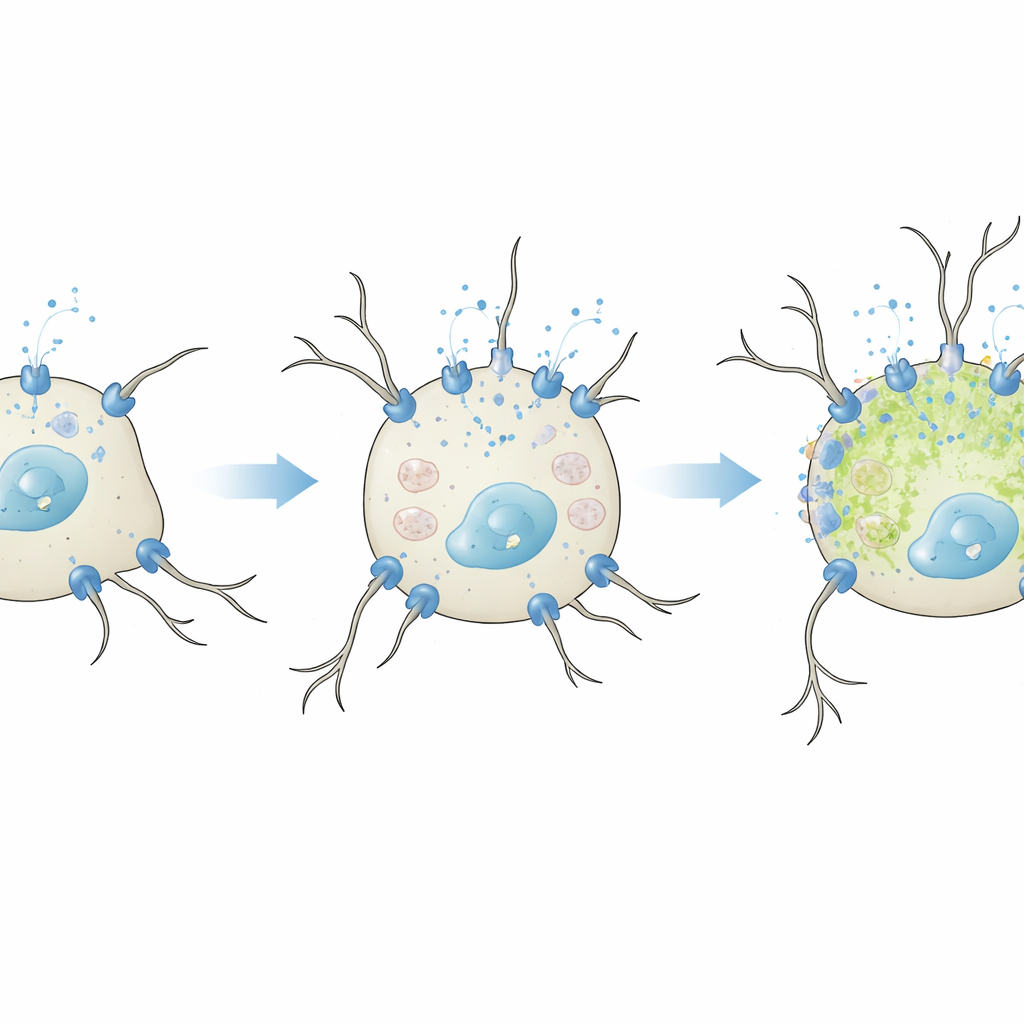
מתי סידן מועיל הופך למזיק
הצוות בדק לאחר מכן מה קורה אם מחזקים באופן מלאכותי את ערוצי ה-L-type הללו. בתנאים מתונים, שאינם גורמים להתמיינות, עם סרום מופחת, הוספת CaV1.2 או CaV1.3 נוסף גרמה לכך שהתאים הגיבו חזק יותר לאשלגן עם גליצות סידן גדולות יותר. רק CaV1.3, עם זאת, שיפרה את הצמיחה של הנויריטים, בהתאמה לעבודה קודמת שמציעה שתת-סוג זה טוב במיוחד בהפעלה של מסלולי גדילה בנוירונים. חשוב לציין שבשלב זה לא נראה עלייה בסמנים של לחץ חמצוני, מה שמראה שהתוספת הממוצעת בכניסת סידן יכולה לעודד תכונות נוירוניות בצורה בטוחה. התמונה השתנתה בתנאי התמיינות מלאים. כאשר CaV1.2 או CaV1.3 יוצרו בכמות מוגזמת בזמן שהתאים כבר נדחפו לבשילה, הנויריטים התקצרו והתאים צברו יותר סוגים של חמצן תגובתי — סימן לנזק חמצוני. ההשפעה הייתה החזקה ביותר עבור CaV1.3, שמופעלת במתחים נמוכים יותר ויכולה לתמוך בכניסת סידן ממושכת.
קו דק בין גדילה ונזק
לסיכום, התוצאות מגלות תפקיד דו-קצווי לערוצי סידן מסוג L במודל הזה של תאים דמויי-נוירון תחושתי. עלייה נורמלית של CaV1.2 ו-CaV1.3 נראית הכרחית כדי שתאי F11 ירכשו תכונות נוירוניות מרכזיות: נויריטים ארוכים יותר, תגובות סידן חזקות יותר ואותות חשמליים פעילים יותר. יחד עם זאת, דחיפה מוגזמת של ערוצים אלה, ובמיוחד CaV1.3 בסביבה שכבר עמוסת סידן, מפּנה את האיזון לעבר לחץ חמצוני ועיכוב בהבשלה. האיזון הזה בין אותות סידן תומכים ומזיקים רלוונטי במיוחד למצבים כמו כאב נוירופתי ומחלות ניווניות עצביות, שבהם פעילות הערוצים והלחץ החמצוני משובשים לעתים קרובות. מכיוון שתאי F11 חיקו תכונות רבות של נוירונים חשים וניתנים לחקירה באמצעות הדמיה אוטומטית ומדידות סידן, עבודה זו מחזקת את ערכם כמשטח בדיקה מעשי לתרופות עתידיות שמטרתן לכוונן בעדינות את כניסת הסידן ולהגן על עצבים פגיעים.
ציטוט: López, D., Brea, J., Barro, M. et al. Voltage-gated calcium channels as key regulators of neuronal differentiation in the immortalized dorsal root ganglion neuronal cell line F11. Sci Rep 16, 14621 (2026). https://doi.org/10.1038/s41598-026-44595-1
מילות מפתח: אותות סידן, התמיינות נוירונית, ערוצי סידן שמופעלים במתח, כאב נוירופתי, לחץ חמצוני