Clear Sky Science · es
Canales de calcio dependientes de voltaje como reguladores clave de la diferenciación neuronal en la línea celular neuronal inmortalizada del ganglio de la raíz dorsal F11
Por qué importan las pequeñas compuertas de calcio para la salud nerviosa
Nuestros cerebros y nervios dependen de un delicado equilibrio de señales eléctricas y mensajeros químicos. Entre los más importantes están unas pequeñas puertas en la membrana celular que permiten la entrada de iones calcio. Este estudio analiza cómo una familia de estas puertas, llamadas canales de calcio dependientes de voltaje, ayuda a que células inmaduras semejantes a neuronas se conviertan en células más maduras con rasgos neuronales —y cómo una actividad excesiva a través de estos canales puede revertirse y dañar las células. Comprender este equilibrio podría abrir nuevas vías para tratar el dolor crónico y las enfermedades neurodegenerativas, en las que las células nerviosas a menudo están estresadas o mueren.
De células simples a redes ramificadas semejantes a nervios
Los investigadores trabajaron con células F11, un modelo de laboratorio muy usado que combina propiedades de neuronas sensoriales espinales con una línea celular cancerosa. En condiciones normales, las células F11 se dividen y tienen un aspecto bastante simple. Al exponerse a un cóctel que eleva una molécula mensajera llamada AMPc, dejan de dividirse y empiezan a comportarse más como neuronas sensoriales reales, desarrollando largas extensiones conocidas como neuritas. El equipo confirmó que durante este cambio las células mostraron oleadas de calcio más intensas cuando se despolarizaban brevemente con potasio, y dispararon más picos eléctricos espontáneos. En otras palabras, a medida que las células maduraban, su maquinaria eléctrica y de señalización por calcio se activó más, reflejando lo que sucede durante el desarrollo de neuronas verdaderas.
Canales de calcio como interruptores de crecimiento
Para averiguar qué canales de calcio eran responsables, los científicos midieron la actividad de los genes que codifican diferentes subtipos de canales. Descubrieron que ocho tipos de canales aumentaron su abundancia conforme las células F11 se diferenciaban, con un notable incremento en el gen de un canal tipo L conocido como CaV1.3. Usando fármacos que bloquean selectivamente los canales tipo L, mostraron que inhibir estos canales durante el período de diferenciación de 72 horas redujo drásticamente las señales de calcio evocadas por potasio y acortó las neuritas, sin matar a las células. Otros bloqueadores de canales, dirigidos a los de tipo T o a diversos canales de alto voltaje implicados en la transmisión sináptica, tuvieron poco efecto. La microscopía confirmó que dos canales tipo L, CaV1.2 y especialmente CaV1.3, eran más abundantes en la superficie de las células diferenciadas, lo que respalda la idea de que estos canales son impulsores claves de las señales de calcio que ayudan a construir características neuronales.
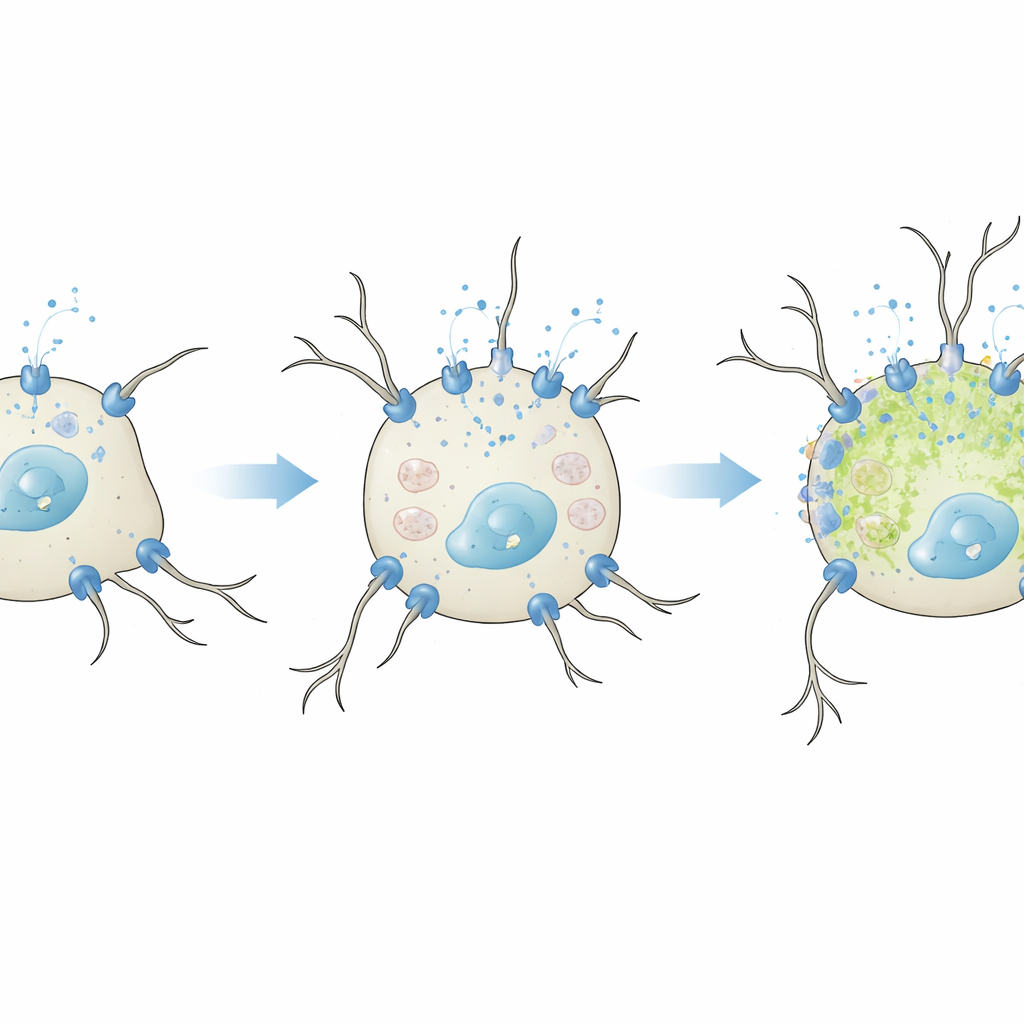
Cuando el calcio útil se vuelve perjudicial
El equipo se preguntó entonces qué ocurre si se incrementa artificialmente la actividad de estos canales tipo L. En condiciones leves, no diferenciantes, con suero reducido, la adición extra de CaV1.2 o CaV1.3 hizo que las células respondieran con oleadas de calcio mayores ante potasio. Sin embargo, solo CaV1.3 potenció el crecimiento de neuritas, coherente con trabajos previos que sugieren que este subtipo es particularmente eficaz en activar vías relacionadas con el crecimiento en neuronas. Es importante destacar que en esta etapa no hubo aumento de marcadores de estrés oxidativo, lo que muestra que un incremento moderado en la entrada de calcio puede promover rasgos neuronales de forma segura. El panorama cambió bajo condiciones de diferenciación completas. Cuando CaV1.2 o CaV1.3 se sobreexpresaron mientras las células ya estaban siendo empujadas a madurar, las neuritas se acortaron y las células acumularon más especies reactivas de oxígeno —una señal de daño oxidativo. El efecto fue más intenso para CaV1.3, que se activa a voltajes más bajos y puede sostener una entrada prolongada de calcio.
Una línea fina entre crecimiento y daño
En conjunto, los resultados revelan un papel de doble filo para los canales de calcio tipo L en este modelo semejante a neuronas sensoriales. La regulación al alza normal de CaV1.2 y CaV1.3 parece necesaria para que las células F11 adquieran propiedades neuronales clave: neuritas más largas, respuestas de calcio más fuertes y señalización eléctrica más activa. Sin embargo, llevar estos canales demasiado lejos, en particular CaV1.3 en un entorno ya cargado de calcio, inclina la balanza hacia el estrés oxidativo y la maduración detenida. Este equilibrio entre señalización de calcio de apoyo y perjudicial es muy relevante para condiciones como el dolor neuropático y las enfermedades neurodegenerativas, donde tanto la actividad de los canales como el estrés oxidativo suelen estar alterados. Dado que las células F11 imitan muchas características de las neuronas sensoras del dolor y pueden ser evaluadas con imágenes automatizadas y mediciones de calcio, este trabajo refuerza su valor como banco de pruebas práctico para futuros fármacos que busquen afinar la entrada de calcio y proteger nervios vulnerables.
Cita: López, D., Brea, J., Barro, M. et al. Voltage-gated calcium channels as key regulators of neuronal differentiation in the immortalized dorsal root ganglion neuronal cell line F11. Sci Rep 16, 14621 (2026). https://doi.org/10.1038/s41598-026-44595-1
Palabras clave: señalización por calcio, diferenciación neuronal, canales de calcio dependientes de voltaje, dolor neuropático, estrés oxidativo