Clear Sky Science · it
I canali del calcio voltaggio-dipendenti come regolatori chiave della differenziazione neuronale nella linea cellulare neuronale immortalizzata del ganglio dorsale F11
Perché i piccoli cancelli del calcio sono importanti per la salute dei nervi
I nostri cervelli e nervi dipendono da un delicato equilibrio di segnali elettrici e messaggeri chimici. Tra i più importanti ci sono piccole porte nella membrana cellulare che permettono agli ioni calcio di entrare rapidamente. Questo studio esamina come una famiglia di queste porte, chiamata canali del calcio voltaggio-dipendenti, aiuti cellule immature simili a neuroni a maturare in cellule più neuronali—e come un’attività eccessiva attraverso questi canali possa avere l’effetto opposto, danneggiando le cellule. Comprendere questo equilibrio potrebbe aprire nuove strade per trattare il dolore cronico e le malattie neurodegenerative, in cui le cellule nervose sono spesso sotto stress o muoiono.
Da cellule semplici a reti ramificate simili a neuroni
I ricercatori hanno lavorato con cellule F11, un modello di laboratorio ampiamente utilizzato che combina proprietà dei neuroni sensoriali spinali con una linea cellulare tumorale. In condizioni normali, le cellule F11 si dividono e hanno un aspetto piuttosto semplice. Quando vengono esposte a un cocktail che aumenta una molecola messaggera chiamata cAMP, smettono di dividersi e cominciano a comportarsi più come veri neuroni sensoriali, crescendo lunghi prolungamenti noti come neuriti. Il gruppo ha confermato che durante questo passaggio le cellule mostrano intensi aumenti di calcio quando vengono brevemente depolarizzate con potassio e generano più scariche elettriche spontanee. In altre parole, man mano che le cellule maturano, la loro macchina di segnalazione elettrica e del calcio diventa più attiva, rispecchiando quanto avviene durante lo sviluppo dei veri neuroni.
I canali del calcio come interruttori della crescita
Per capire quali canali del calcio fossero responsabili, gli scienziati hanno misurato l’attività dei geni che codificano i diversi sottotipi di canale. Hanno scoperto che otto tipi di canali diventavano più abbondanti durante la differenziazione delle F11, con un marcato aumento del gene per un canale di tipo L noto come CaV1.3. Usando farmaci che bloccano selettivamente i canali di tipo L, hanno mostrato che spegnere questi canali durante le 72 ore di differenziazione riduceva nettamente i segnali di calcio indotti dal potassio e accorciava i neuriti, senza uccidere le cellule. Altri bloccanti, diretti ai canali di tipo T o a vari canali ad alto voltaggio coinvolti nella trasmissione sinaptica, hanno avuto poco effetto. Le immagini hanno confermato che due canali di tipo L, CaV1.2 e soprattutto CaV1.3, erano più abbondanti sulla superficie delle cellule differenziate, sostenendo l’idea che questi canali siano i principali motori dei segnali di calcio che favoriscono la formazione di caratteristiche neuronali.
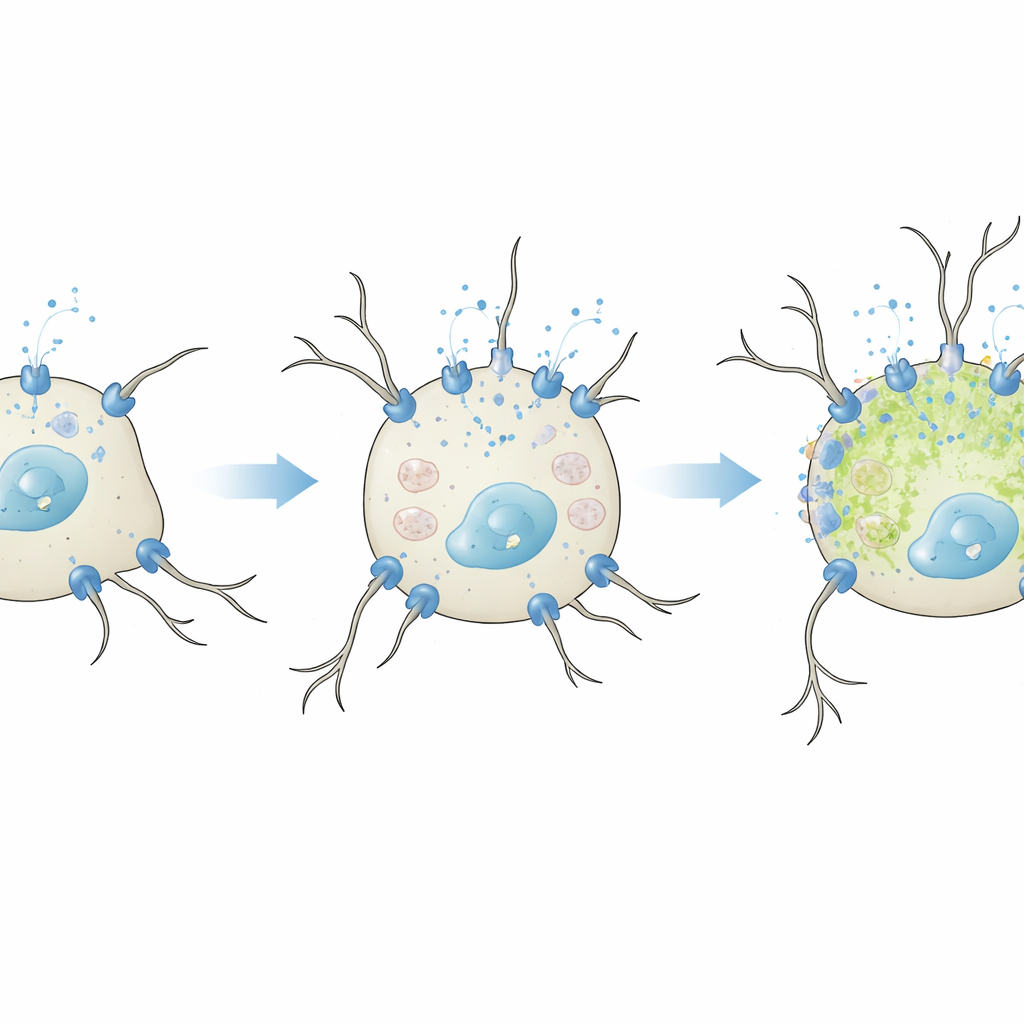
Quando il calcio utile diventa dannoso
Il team ha poi chiesto cosa succede se questi canali di tipo L vengono potenziati artificialmente. In condizioni lievi, non differenzianti, con siero ridotto, l’aggiunta di CaV1.2 o CaV1.3 aumentava la risposta delle cellule al potassio con surges di calcio più grandi. Tuttavia, solo CaV1.3 migliorava la crescita dei neuriti, coerente con lavori precedenti che suggeriscono che questo sottotipo è particolarmente efficace nell’attivare vie legate alla crescita nei neuroni. È importante notare che a questo stadio non si osservava un aumento nei marcatori di stress ossidativo, indicando che un moderato incremento dell’entrata di calcio può promuovere in sicurezza tratti neuronali. Il quadro cambiava in condizioni di differenziazione completa. Quando CaV1.2 o CaV1.3 venivano sovraespresse mentre le cellule erano già spinte a maturare, i neuriti diventavano più corti e le cellule accumulavano più specie reattive dell’ossigeno—un segno di danno ossidativo. L’effetto era più marcato per CaV1.3, che si attiva a voltaggi più bassi e può sostenere un’entrata prolungata di calcio.
Una linea sottile tra crescita e danno
Nel complesso, i risultati rivelano un ruolo a doppio taglio per i canali del calcio di tipo L in questo modello simile ai neuroni sensoriali. L’aumento normale di CaV1.2 e CaV1.3 sembra necessario affinché le cellule F11 acquisiscano proprietà neuronali chiave: neuriti più lunghi, risposte al calcio più intense e segnali elettrici più attivi. Tuttavia spingere troppo questi canali, in particolare CaV1.3 in un ambiente già carico di calcio, fa pendere l’equilibrio verso lo stress ossidativo e l’arresto della maturazione. Questo equilibrio tra segnalazione del calcio di supporto e dannosa è altamente rilevante per condizioni come il dolore neuropatico e le malattie neurodegenerative, dove sia l’attività dei canali sia lo stress ossidativo sono spesso alterati. Poiché le cellule F11 imitano molte caratteristiche dei neuroni che percepiscono il dolore e possono essere analizzate con imaging automatizzato e misure del calcio, questo lavoro ne rafforza il valore come banco di prova pratico per futuri farmaci volti a regolare finemente l’entrata di calcio e proteggere i nervi vulnerabili.
Citazione: López, D., Brea, J., Barro, M. et al. Voltage-gated calcium channels as key regulators of neuronal differentiation in the immortalized dorsal root ganglion neuronal cell line F11. Sci Rep 16, 14621 (2026). https://doi.org/10.1038/s41598-026-44595-1
Parole chiave: segnalazione del calcio, differenziazione neuronale, canali del calcio voltaggio-dipendenti, dolore neuropatico, stress ossidativo