Clear Sky Science · pl
Kanały wapniowe zależne od potencjału jako kluczowi regulatorzy różnicowania neuronalnego w immortalizowanej linii komórkowej zwoju rdzeniowego F11
Dlaczego małe bramki wapniowe mają znaczenie dla zdrowia nerwów
Nasz mózg i nerwy opierają się na delikatnej równowadze między sygnałami elektrycznymi a przekaźnikami chemicznymi. Wśród najważniejszych elementów są drobne kanały w błonie komórkowej, które pozwalają jonom wapnia napływać do wnętrza. W badaniu tym przyjrzano się, jak jedna rodzina tych bramek, zwana kanałami wapniowymi zależnymi od potencjału, pomaga niedojrzałym komórkom o cechach nerwowych przekształcać się w bardziej dojrzałe, neuronopodobne komórki — oraz jak nadmierna aktywność przez te kanały może mieć efekt odwrotny, uszkadzając komórki. Zrozumienie tej równowagi może otworzyć nowe drogi leczenia przewlekłego bólu i chorób neurodegeneracyjnych, w których komórki nerwowe często są zestresowane lub giną.
Od prostych komórek do rozgałęziających się sieci neuronopodobnych
Naukowcy pracowali na komórkach F11, szeroko stosowanym modelu laboratoryjnym łączącym cechy neuronów czuciowych rdzenia z linią komórkową nowotworu. W warunkach normalnych komórki F11 dzielą się i wyglądają stosunkowo prosto. Po ekspozycji na koktajl podnoszący poziom przekaźnika cAMP przestają się dzielić i zaczynają zachowywać bardziej jak prawdziwe neurony czuciowe, wyrastając długie wypustki zwane neurytami. Zespół potwierdził, że podczas tej przemiany komórki wykazywały silniejsze skoki wapniowe przy krótkiej depolaryzacji potasem i częstsze spontaniczne wyładowania elektryczne. Innymi słowy, w miarę dojrzewania komórek wzrastała aktywność ich układów do sygnalizacji elektrycznej i wapniowej, co odpowiada temu, co dzieje się podczas rozwoju rzeczywistych komórek nerwowych.
Kanały wapniowe jako przełączniki wzrostu
Aby ustalić, które kanały wapniowe były odpowiedzialne, badacze zmierzyli aktywność genów kodujących różne podtypy kanałów. Odkryli, że osiem typów kanałów staje się bardziej obfitych w miarę różnicowania F11, z wyraźnym wzrostem ekspresji genu dla specyficznego kanału typu L, znanego jako CaV1.3. Używając leków selektywnie blokujących kanały typu L, pokazali, że wyłączenie tych kanałów podczas 72-godzinnego okresu różnicowania znacząco zmniejsza sygnały wapniowe wywołane potasem i skraca neurity, bez zabijania komórek. Inne blokery kanałów, celujące w typ T lub różne kanały wysokiego napięcia zaangażowane w transmisję synaptyczną, miały niewielki efekt. Obrazowanie potwierdziło, że dwa kanały typu L, CaV1.2 i w szczególności CaV1.3, były bardziej obecne na powierzchni komórek zróżnicowanych, co wspiera tezę, że te kanały są kluczowymi napędami sygnałów wapniowych pomagających budować cechy neuronopodobne.
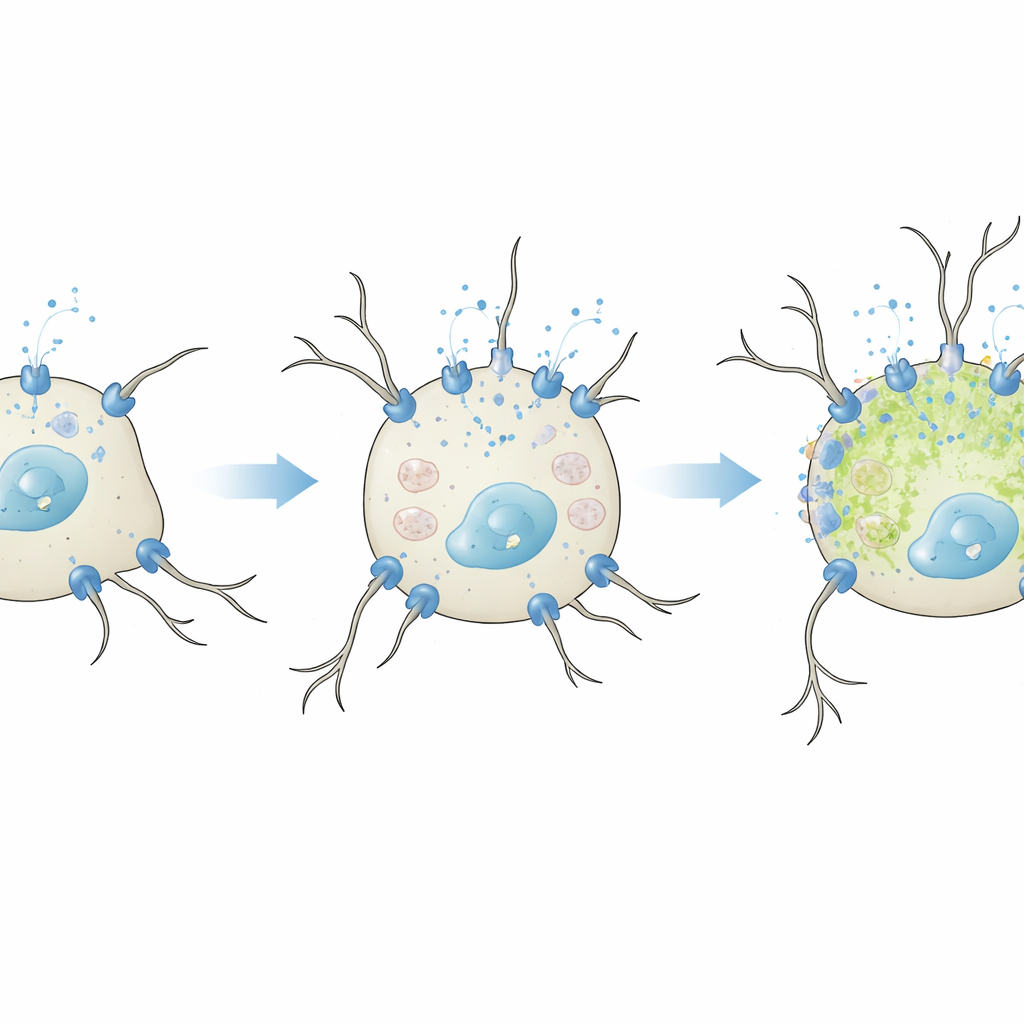
Kiedy pomocny wapń staje się szkodliwy
Zespół zapytał następnie, co się stanie, gdy te kanały typu L zostaną sztucznie wzmocnione. W łagodnych warunkach, które nie sprzyjały różnicowaniu i przy obniżonym stężeniu surowicy, dodanie większej ilości CaV1.2 lub CaV1.3 sprawiło, że komórki silniej reagowały na potas większymi skokami wapniowymi. Jednak tylko CaV1.3 zwiększał wydłużanie neurytów, zgodnie z wcześniejszymi pracami sugerującymi, że ten podtyp szczególnie skutecznie uruchamia szlaki związane ze wzrostem w neuronach. Co ważne, na tym etapie nie obserwowano wzrostu markerów stresu oksydacyjnego, co pokazuje, że umiarkowany wzrost napływu wapnia może bezpiecznie promować cechy neuronalne. Obraz uległ zmianie w pełnych warunkach różnicowania. Gdy CaV1.2 lub CaV1.3 były nadmiernie produkowane w czasie, gdy komórki były już popychane do dojrzewania, neurity ulegały skróceniu, a komórki akumulowały więcej reaktywnych form tlenu — oznakę uszkodzeń oksydacyjnych. Efekt był najsilniejszy dla CaV1.3, który aktywuje się przy niższych napięciach i może wspierać wydłużony napływ wapnia.
Wąska granica między wzrostem a uszkodzeniem
Podsumowując, wyniki ujawniają obosieczną rolę kanałów wapniowych typu L w tym modelu przypominającym neurony czuciowe. Normalna regulacja w górę CaV1.2 i CaV1.3 wydaje się niezbędna, aby komórki F11 nabyły kluczowe właściwości neuronalne: dłuższe neurity, silniejsze odpowiedzi wapniowe i bardziej aktywne sygnalizowanie elektryczne. Jednocześnie nadmierne pobudzenie tych kanałów, szczególnie CaV1.3 w już obciążonym wapniem środowisku, przechyla równowagę w stronę stresu oksydacyjnego i zahamowanego dojrzewania. Ta równowaga między wspierającą a szkodliwą sygnalizacją wapniową ma duże znaczenie dla stanów takich jak ból neuropatyczny i choroby neurodegeneracyjne, w których zarówno aktywność kanałów, jak i stres oksydacyjny są często zaburzone. Ponieważ komórki F11 naśladują wiele cech neuronów czucia bólu i można je badać za pomocą zautomatyzowanego obrazowania oraz pomiarów wapniowych, praca ta wzmacnia ich wartość jako praktycznego poligonu testowego dla przyszłych leków mających na celu precyzyjne dostrojenie napływu wapnia i ochronę podatnych nerwów.
Cytowanie: López, D., Brea, J., Barro, M. et al. Voltage-gated calcium channels as key regulators of neuronal differentiation in the immortalized dorsal root ganglion neuronal cell line F11. Sci Rep 16, 14621 (2026). https://doi.org/10.1038/s41598-026-44595-1
Słowa kluczowe: sygnalizacja wapniowa, różnicowanie neuronalne, kanały wapniowe zależne od potencjału, ból neuropatyczny, stres oksydacyjny