Clear Sky Science · pt
Canais de cálcio dependentes de voltagem como reguladores-chave da diferenciação neuronal na linhagem celular neuronal imortalizada do gânglio da raiz dorsal F11
Por que pequenos portões de cálcio importam para a saúde dos nervos
Nossos cérebros e nervos dependem de um equilíbrio delicado entre sinais elétricos e mensageiros químicos. Entre os mais importantes estão pequenos portais na membrana celular que permitem a entrada de íons de cálcio. Este estudo investiga como uma família desses portais, chamada canais de cálcio dependentes de voltagem, ajuda células imaturas semelhantes a neurônios a se transformarem em células mais maduras — e como atividade excessiva nesses canais pode sair pela culatra, danificando as células. Compreender esse equilíbrio pode abrir novos caminhos para tratar dor crônica e doenças neurodegenerativas, nas quais as células nervosas frequentemente estão estressadas ou morrendo.
De células simples a redes ramificadas semelhantes a nervos
Os pesquisadores trabalharam com células F11, um modelo de laboratório amplamente usado que mistura propriedades de neurônios sensoriais espinhais com uma linhagem celular cancerosa. Em condições normais, as células F11 se dividem e têm aparência relativamente simples. Quando expostas a um coquetel que eleva uma molécula mensageira chamada AMP cíclico (cAMP), elas param de se dividir e começam a se comportar mais como neurônios sensoriais verdadeiros, crescendo extensões longas conhecidas como neuritos. A equipe confirmou que, durante essa mudança, as células mostraram surtos de cálcio mais fortes quando despolarizadas brevemente com potássio, e dispararam mais picos elétricos espontâneos. Em outras palavras, à medida que as células amadureciam, sua maquinaria elétrica e de sinalização do cálcio tornou-se mais ativa, espelhando o que acontece durante o desenvolvimento de neurônios reais.
Canais de cálcio como interruptores de crescimento
Para identificar quais canais de cálcio eram responsáveis, os cientistas mediram a atividade dos genes que codificam diferentes subtipos de canais. Descobriram que oito tipos de canais se tornaram mais abundantes à medida que as células F11 diferenciavam, com um aumento notável no gene de um canal do tipo L conhecido como CaV1.3. Usando fármacos que bloqueiam seletivamente os canais do tipo L, eles mostraram que bloquear esses canais durante o período de diferenciação de 72 horas reduziu drasticamente os sinais de cálcio evocados por potássio e encurtou os neuritos, sem matar as células. Outros bloqueadores, direcionados ao tipo T ou a vários canais de alto limiar envolvidos na transmissão sináptica, tiveram pouco efeito. Imagens confirmaram que dois canais do tipo L, CaV1.2 e especialmente CaV1.3, eram mais abundantes na superfície das células diferenciadas, corroborando a ideia de que esses canais são motores-chave dos sinais de cálcio que ajudam a construir características semelhantes a neurônios.
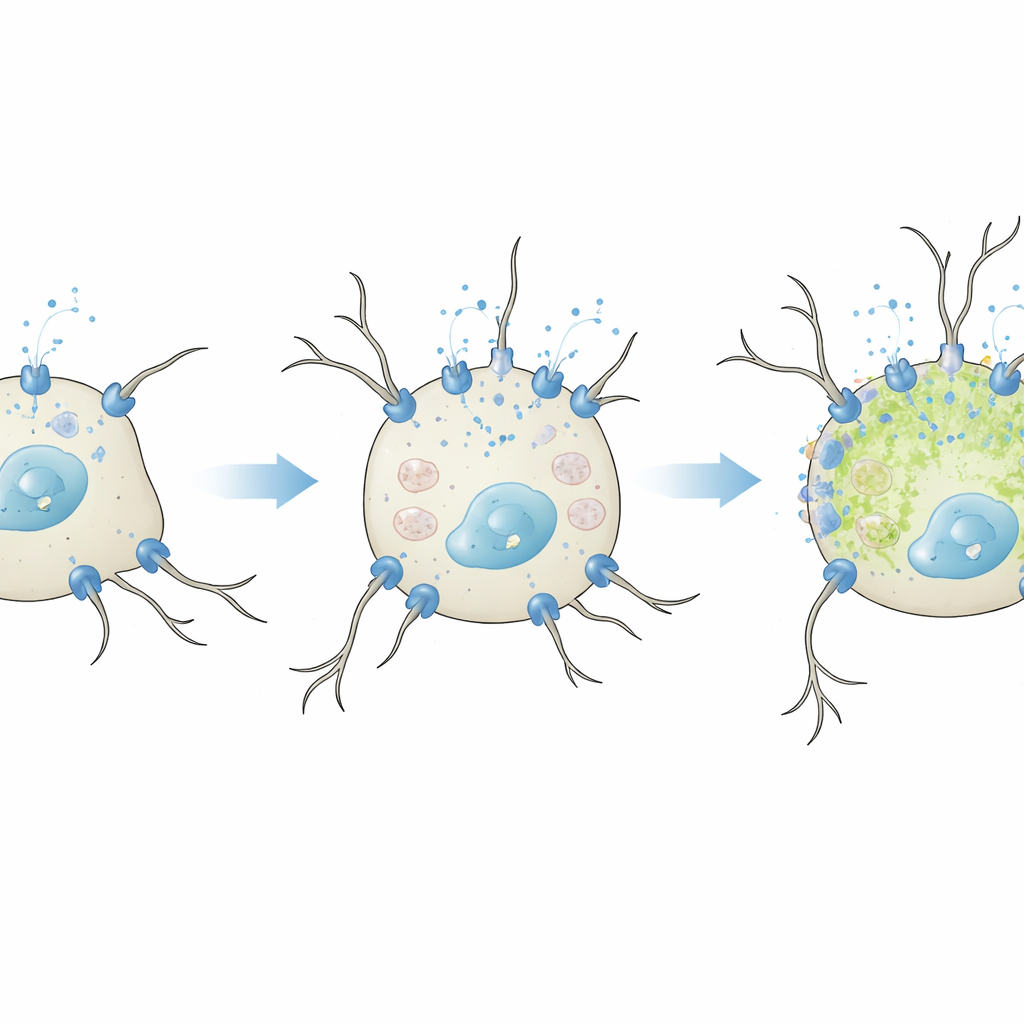
Quando o cálcio útil se torna nocivo
A equipe então investigou o que acontece se esses canais do tipo L são artificialmente aumentados. Em condições brandas, não diferenciadoras, com soro reduzido, a adição extra de CaV1.2 ou CaV1.3 fez com que as células respondessem mais fortemente ao potássio, com surtos de cálcio maiores. No entanto, apenas o CaV1.3 aumentou o crescimento de neuritos, consistente com trabalhos anteriores que sugerem que esse subtipo é particularmente eficaz em ativar vias relacionadas ao crescimento em neurônios. Importante: nessa fase não houve aumento de marcadores de estresse oxidativo, mostrando que um aumento moderado da entrada de cálcio pode promover traços neuronais com segurança. O quadro mudou sob condições de diferenciação completa. Quando CaV1.2 ou CaV1.3 foram superexpressos enquanto as células já eram induzidas a amadurecer, os neuritos ficaram mais curtos e as células acumularam mais espécies reativas de oxigênio — um sinal de dano oxidativo. O efeito foi mais forte para CaV1.3, que ativa em voltagens mais baixas e pode suportar entrada prolongada de cálcio.
Uma linha tênue entre crescimento e dano
Em conjunto, os resultados revelam um papel de dois gumes para os canais de cálcio do tipo L neste modelo semelhante a neurônio sensorial. A regulação positiva normal de CaV1.2 e CaV1.3 parece necessária para que as células F11 adquiram propriedades neuronais chave: neuritos mais longos, respostas de cálcio mais fortes e sinalização elétrica mais ativa. Ainda assim, levar esses canais longe demais, particularmente CaV1.3 em um ambiente já carregado de cálcio, inclina a balança para o estresse oxidativo e a maturação interrompida. Esse equilíbrio entre sinalização de cálcio favorável e nociva é altamente relevante para condições como dor neuropática e doenças neurodegenerativas, nas quais tanto a atividade dos canais quanto o estresse oxidativo frequentemente estão alterados. Como as células F11 imitam muitas características de neurônios sensoriais de detecção de dor e podem ser examinadas com imageamento automatizado e medições de cálcio, este trabalho reforça seu valor como um campo de testes prático para futuros fármacos que visem ajustar a entrada de cálcio e proteger nervos vulneráveis.
Citação: López, D., Brea, J., Barro, M. et al. Voltage-gated calcium channels as key regulators of neuronal differentiation in the immortalized dorsal root ganglion neuronal cell line F11. Sci Rep 16, 14621 (2026). https://doi.org/10.1038/s41598-026-44595-1
Palavras-chave: sinalização por cálcio, diferenciação neuronal, canais de cálcio dependentes de voltagem, dor neuropática, estresse oxidativo