Clear Sky Science · fr
Les canaux calciques voltage‑dépendants, régulateurs clés de la différenciation neuronale dans la lignée cellulaire immortalisée du ganglion rachidien dorsal F11
Pourquoi de minuscules portes au calcium comptent pour la santé nerveuse
Nos cerveaux et nos nerfs reposent sur un équilibre délicat de signaux électriques et de messagers chimiques. Parmi les plus importants se trouvent de minuscules portes dans la membrane cellulaire qui laissent entrer des ions calcium. Cette étude examine comment une famille de ces portes, appelées canaux calciques voltage‑dépendants, aide des cellules immatures de type nerveux à mûrir en cellules plus proches des neurones — et comment une activité excessive via ces canaux peut se retourner contre les cellules et les endommager. Comprendre cet équilibre pourrait ouvrir de nouvelles voies pour traiter la douleur chronique et les maladies neurodégénératives, où les neurones sont souvent stressés ou en train de mourir.
De cellules simples à des réseaux ramifiés de type nerveux
Les chercheurs ont travaillé avec des cellules F11, un modèle de laboratoire largement utilisé qui combine des caractéristiques des neurones sensoriels spinaux et d’une lignée de cellules cancéreuses. Dans des conditions normales, les cellules F11 se divisent et présentent un aspect relativement simple. Lorsqu’elles sont exposées à un mélange qui augmente une molécule messagère appelée AMPc, elles arrêtent de se diviser et commencent à se comporter davantage comme de vrais neurones sensoriels, en développant de longues extensions appelées neurites. L’équipe a confirmé que pendant cette transition, les cellules présentaient des poussées calciques plus intenses lorsqu’elles étaient brièvement dépolarisées au potassium, et qu’elles déclenchaient davantage de pointes électriques spontanées. Autrement dit, à mesure que les cellules mûrissaient, leur machinerie de signalisation électrique et calcique devenait plus active, reflétant ce qui se passe lors du développement de neurones véritables.
Les canaux calciques comme interrupteurs de croissance
Pour identifier quels canaux calciques étaient responsables, les scientifiques ont mesuré l’activité des gènes codant différentes sous‑types de canaux. Ils ont découvert que huit types de canaux devenaient plus abondants lors de la différenciation des cellules F11, avec une augmentation marquée du gène d’un canal de type L particulier connu sous le nom de CaV1.3. En utilisant des médicaments qui bloquent sélectivement les canaux de type L, ils ont montré que l’inhibition de ces canaux pendant la période de différenciation de 72 heures réduisait fortement les signaux calciques induits par le potassium et raccourcissait les neurites, sans tuer les cellules. D’autres bloqueurs, ciblant les canaux de type T ou divers canaux à haut voltage impliqués dans la transmission synaptique, avaient peu d’effet. L’imagerie a confirmé que deux canaux de type L, CaV1.2 et surtout CaV1.3, étaient plus abondants à la surface des cellules différenciées, soutenant l’idée que ces canaux sont des moteurs clés des signaux calciques qui favorisent la formation de traits de type neuronal.
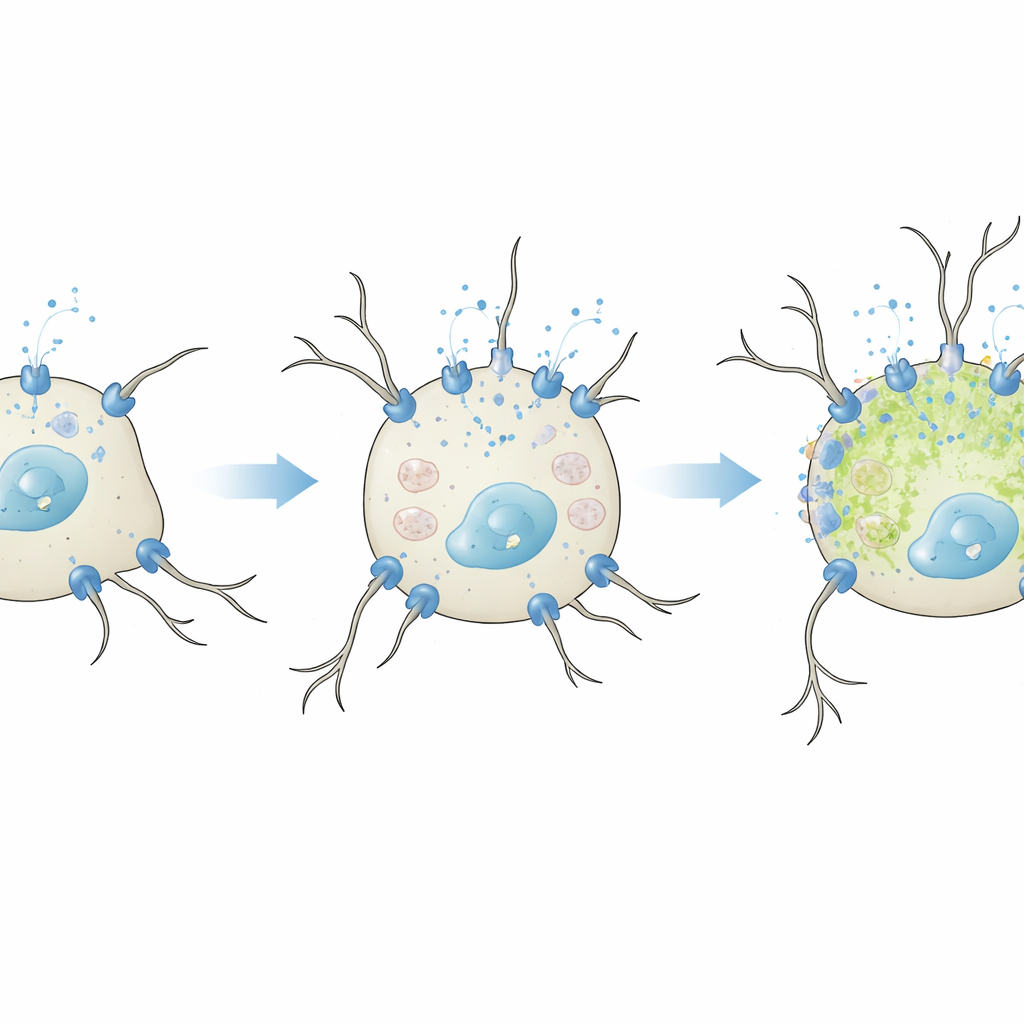
Quand un calcium utile devient nocif
L’équipe s’est ensuite demandé ce qui se passe si ces canaux de type L sont stimulés artificiellement. Dans des conditions douces, non différenciantes et avec un sérum réduit, l’ajout de CaV1.2 ou CaV1.3 a rendu les cellules plus réactives au potassium, avec des poussées calciques plus importantes. Seul CaV1.3, cependant, a favorisé l’allongement des neurites, conformément à des travaux antérieurs suggérant que ce sous‑type est particulièrement efficace pour activer les voies de croissance neuronale. Il est important de noter qu’à ce stade il n’y avait pas d’augmentation des marqueurs de stress oxydatif, montrant qu’une augmentation modérée de l’entrée calcique pouvait promouvoir en toute sécurité des traits neuronaux. Le tableau a changé en conditions de différenciation complète. Lorsque CaV1.2 ou CaV1.3 étaient surproduits alors que les cellules étaient déjà poussées à maturer, les neurites devenaient plus courts et les cellules accumulaient davantage d’espèces réactives de l’oxygène — un signe de dommage oxydatif. L’effet était le plus marqué pour CaV1.3, qui s’active à des potentiels plus négatifs et peut soutenir une entrée calcique prolongée.
Une ligne fine entre croissance et dommage
Pris ensemble, les résultats révèlent un rôle à double tranchant des canaux calciques de type L dans ce modèle proche des neurones sensoriels. Une régulation à la hausse normale de CaV1.2 et CaV1.3 semble nécessaire pour que les cellules F11 acquièrent des propriétés neuronales clés : neurites plus longs, réponses calciques plus fortes et signalisation électrique plus active. Pourtant, pousser ces canaux trop loin, en particulier CaV1.3 dans un environnement déjà chargé en calcium, fait pencher la balance vers le stress oxydatif et un blocage de la maturation. Cet équilibre entre une signalisation calcique favorable et nuisible est très pertinent pour des affections comme la douleur neuropathique et les maladies neurodégénératives, où l’activité des canaux et le stress oxydatif sont souvent perturbés. Parce que les cellules F11 imitent de nombreuses caractéristiques des neurones détecteurs de la douleur et peuvent être étudiées par imagerie automatisée et mesures calciques, ce travail renforce leur valeur comme banc d’essai pratique pour des futurs médicaments visant à ajuster l’entrée calcique et protéger les nerfs vulnérables.
Citation: López, D., Brea, J., Barro, M. et al. Voltage-gated calcium channels as key regulators of neuronal differentiation in the immortalized dorsal root ganglion neuronal cell line F11. Sci Rep 16, 14621 (2026). https://doi.org/10.1038/s41598-026-44595-1
Mots-clés: signalisation calcique, différenciation neuronale, canaux calciques voltage‑dépendants, douleur neuropathique, stress oxydatif