Clear Sky Science · tr
Kapsamlı makine öğrenmesi, gastrik kanserde tedavi direncini ve sağkalımı öngören anoikiz imzalarını tanımlıyor
Bu araştırma hastalar için neden önemli
Mide kanseri, birçok tümörün kemoterapi ve yeni immünoterapilere yanıt vermeyi bırakması nedeniyle dünyada en ölümcül kanserlerden biri olmaya devam ediyor. Bu çalışma basit ama kritik bir soruyu soruyor: tümör hücrelerinin ve çevresinin moleküler “hayatta kalma numaralarını” okuyarak hangi hastaların tedaviye direnç göstereceğini ve kimlerin fayda göreceğini tahmin edebilir miyiz? Modern makine öğrenmesiyle binlerce geni tarayarak araştırmacılar, doktorların mide kanseri hastaları için daha etkili, kişiselleştirilmiş tedaviler seçmesine yardımcı olabilecek güçlü bir skor geliştirdiler.
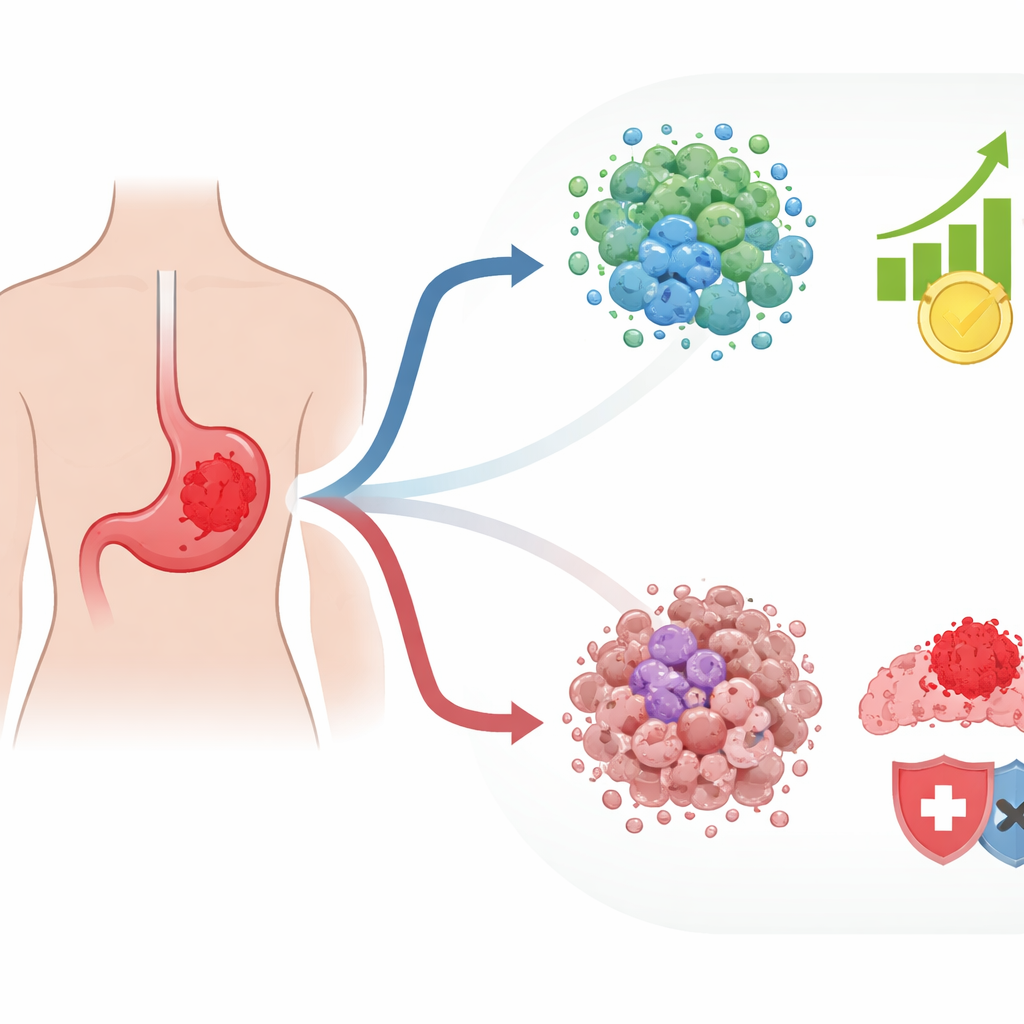
Tümör hücreleri doğal güvenlik kontrollerinden nasıl kaçıyor
Normal hücreler, doku içindeki doğru yerlerini kaybettiklerinde devreye giren bir kendini yok etme programıyla donatılmıştır; bu süreç detachment-induced cell death (yerinden kopma kaynaklı hücre ölümü) olarak adlandırılır. Kanser hücreleri genellikle bu kaderden kaçmayı öğrenir, bu da onların yayılmasına ve yeni tümör tohumları oluşturmasına izin verir. Yazarlar, bu kopma yanıtıyla bağlantılı genlere ve bunların tümörlerin ilaçlara verdiği yanıtlarla nasıl ilişkili olduğuna odaklandı. 10 büyük halka açık mide kanseri veri tabanını kullanarak hücre ölümü, kemoterapiye duyarlılık veya direnç ve immünoterapiye yanıtla ilişkili gen setlerini çapraz referansladılar. Bu karmaşık örtüşmeden, hem hücrelerin detachment-induced death’den ne kadar kolay kaçtığını hem de tedavi altındaki davranışlarını yansıtan 125 anahtar geni ayırdılar; bunlara ilaçla “doğallaştırılmış” anoikiz genleri anlamında drug-naturalized anoikis genes (DNAGs) adını verdiler.
Midenin iki gizli tümör türü
Ekibin DNAG etkinliğine göre 800’den fazla mide tümörünü gruplayınca iki ana desen ortaya çıktı. Bir grup tümörde çok sayıda genetik mutasyon ve kromozom yapısında değişiklik vardı; bu ilk bakışta kötü bir haber gibi görünse de, aslında kanseri bağışıklık sistemi tarafından daha görünür kılabilir. Bu tümörler aktif bağışıklık saldırısına dair daha fazla işaret taşıyor ve kanseri tanıyıp savaşa katılabilen bağışıklık hücrelerini içeriyordu. İkinci grup ise çok farklıydı: daha genç hastalarda ve agresif olduğu bilinen belirli moleküler bir alt tipte daha sık görülüyordu. Bu tümörler, kanseri bağışıklık saldırısından koruma eğiliminde olan yapısal destek hücreleri ve diğer bileşenlerin baskın olduğu, güçlü şekilde baskılanmış bir çevrede yer alıyordu. Bu ikinci desene sahip hastaların genel gidişatları daha kötüydü.
Tümör davranışını okuyan tedavi skoru
Bu desenlerin üzerine inşa ederek, araştırmacılar 101 makine öğrenmesi yaklaşımının kombinasyonlarını kullanıp daha küçük bir 11 genlik sete indirgediler ve buna “tedavi odaklı prognostik imza” (TOPS) adını verdiler. Bu skor hastaları yüksek ve düşük risk gruplarına ayırıyor. Bağımsız hasta koleksiyonlarının birden fazlasında, yüksek TOPS skorlu olanların tutarlı şekilde daha kısa sağkalıma, daha ileri hastalığa ve invaziv davranışıyla bilinen tümör tiplerine sahip olduğu görüldü. Aynı zamanda yüksek TOPS’lu tümörler hem kemoterapiye hem de immün kontrol noktası ilaçlarına daha az yanıt verme eğilimindeydi; düşük TOPS’lu tümörler ise immünoterapi sonrası daha iyi yanıtlar ve daha uzun sağkalım gösteriyordu. Skor, yaş, cinsiyet ve evre gibi geleneksel klinik özelliklerden daha iyi bir sonuç öngörücü performans sergiledi.
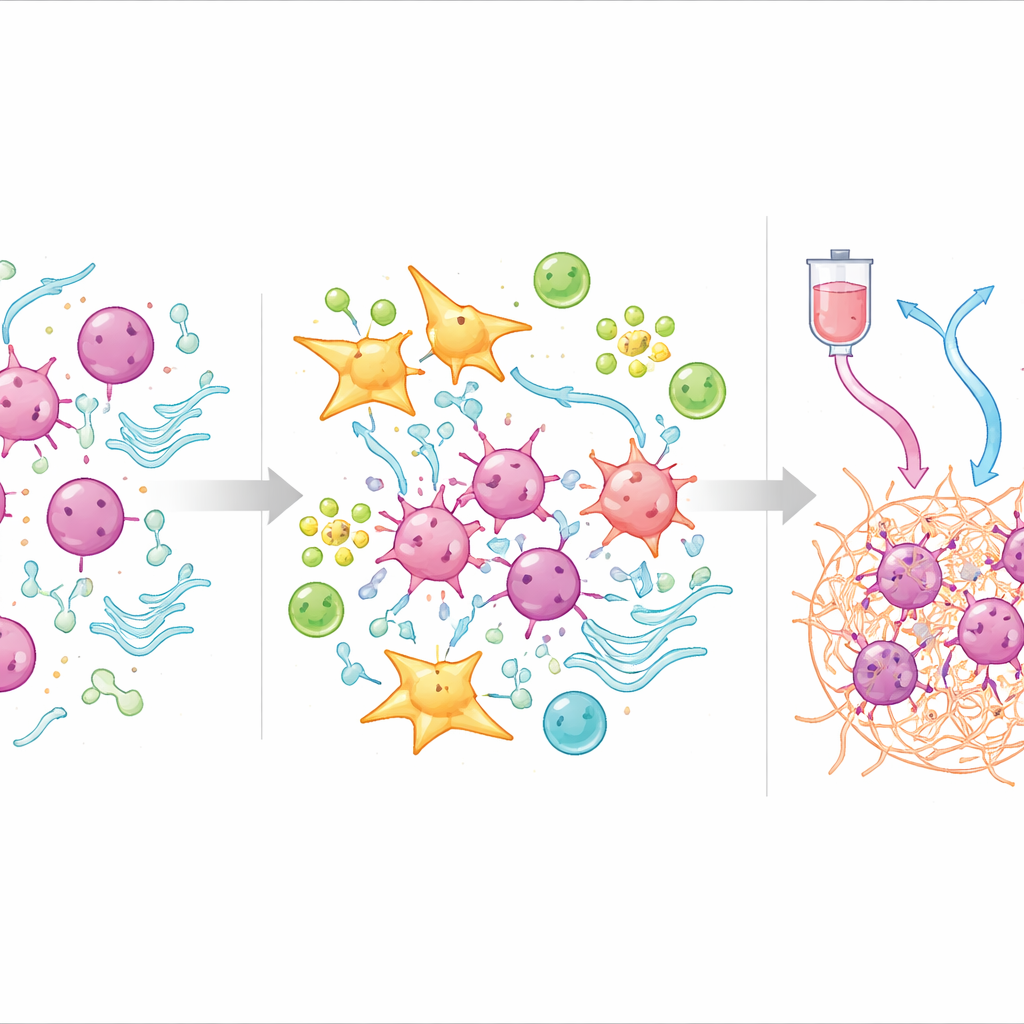
Direnç hakkında tümör ekosisteminin açığa çıkardıkları
Skorun neden işe yaradığını anlamak için ekip, tümör içindeki bireysel hücreleri inceleyen tek hücre dizilemesine yöneldi. Yüksek TOPS’lu tümörlerin fibroblastlarla—doku iskeletini oluşturmaya yardımcı hücrelerle—ve belirli damar hücreleriyle dolu olduğunu buldular; bu hücreler kanser hücrelerinin etrafında yoğun, koruyucu bir kabuk oluşturuyordu. Bu kabuk içinde fibroblastlar, tümör hücreleriyle güçlü iletişim kuran ve yeni damar oluşumu, değişmiş metabolizma ve immün baskılanmayla ilişkili yolları aktive eden bir alt tipe doğru gelişimsel bir yol izlediler. Buna karşılık, düşük TOPS’lu tümörler daha fazla T hücresi, B hücresi ve plazma hücresi içeriyor; bunlar etkili bir immün saldırı başlatabilir ve invaziyondan ziyade normal metabolizma ve doku bakımını destekleyen gen aktivite desenleri gösteriyordu.
Gelecekteki tedavi için olası anlamı
Hastalar için çalışmanın temel mesajı şudur: mikroskop altında benzer görünen tüm mide kanserleri aynı değildir. Hücrelerin yerinden kopma ile nasıl başa çıktıkları ve çevre dokunun nasıl davrandığı ile ilişkili 11 genlik bir imzayı okuyarak doktorlar bir gün standart kemoterapi veya immünoterapiden kimlerin fayda göreceğini, kimlerin destekleyici hücreleri ve tümör komşuluğundaki sinyalleri de hedefleyen alternatif veya kombinasyon stratejilerine ihtiyaç duyacağını daha iyi tahmin edebilirler. Modelin ileriye dönük klinik deneylerde test edilmesi gerekiyor olsa da, mide kanseri tedavisini daha gerçekten kişiselleştirilmiş hale getirme ve bu zorlu hastalıkla karşı karşıya kalan hastalar için şansları iyileştirme yönünde umut verici bir yol haritası sunuyor.
Atıf: Liu, F., Zhou, Y., Xie, Y. et al. Comprehensive machine learning identifies anoikis signatures predicting therapeutic resistance and survival in gastric cancer. Sci Rep 16, 11571 (2026). https://doi.org/10.1038/s41598-026-38996-5
Anahtar kelimeler: mide kanseri, tedavi direnci, tümör mikroçevresi, immünoterapi yanıtı, makine öğrenmesi biyoişaretçileri