Clear Sky Science · nl
Omvattende machine learning identificeert anoikissignaturen die therapeutische resistentie en overleving bij maagkanker voorspellen
Waarom dit onderzoek belangrijk is voor patiënten
Maagkanker blijft een van de dodelijkste kankers wereldwijd, grotendeels omdat veel tumoren ophouden te reageren op chemotherapie en nieuwe immunotherapieën. Deze studie stelt een eenvoudige maar cruciale vraag: kunnen we de moleculaire “overlevingstrucs” van kankercellen en hun omgeving aflezen om te voorspellen welke patiënten resistent zullen zijn tegen behandeling en welke ervan zullen profiteren? Door duizenden genen te doorzoeken met moderne machine learning, bouwen de onderzoekers een krachtige score die artsen mogelijk kan helpen bij het kiezen van effectievere, gepersonaliseerde therapieën voor mensen met maagkanker.
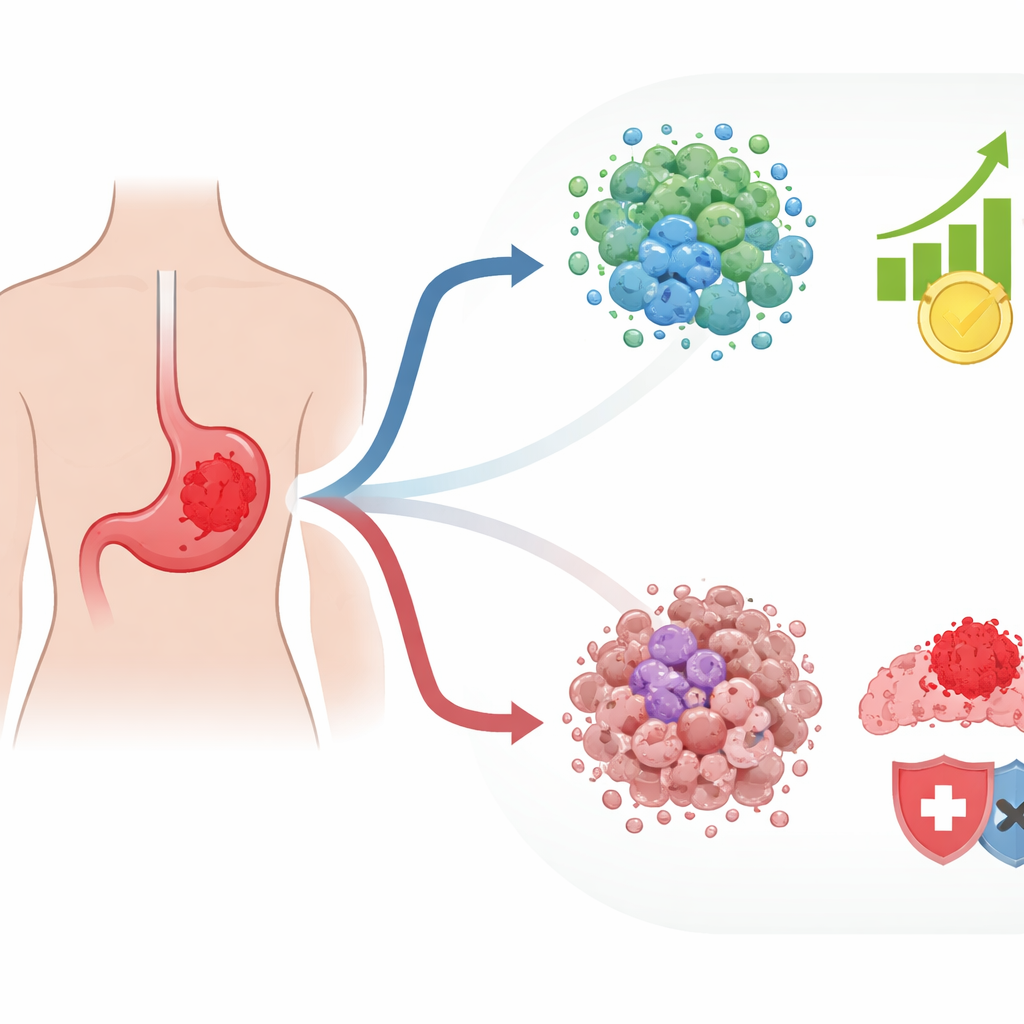
Hoe kankercellen hun natuurlijke veiligheidsschakelaars omzeilen
Normale cellen beschikken over een zelfvernietigingsprogramma dat wordt geactiveerd wanneer ze hun juiste plaats in het weefsel verliezen, een proces dat detachment-induced cell death wordt genoemd. Kankercellen leren deze afloop vaak te vermijden, waardoor ze zich kunnen verspreiden en nieuwe tumoren kunnen vormen. De auteurs concentreerden zich op genen die verbonden zijn met deze loslatingsreactie en op hoe die genen zich verhouden tot de reacties van tumoren op geneesmiddelen. Met behulp van 10 grote publieke databanken voor maagkanker kruisverwijzigden ze genensets die samenhangen met celdood, gevoeligheid of resistentie voor chemotherapie, en respons op immunotherapie. Uit deze complexe overlap distilleerden ze 125 sleutelgenen die zowel weerspiegelen hoe gemakkelijk cellen ontkomen aan loslatingsgeïnduceerde dood als hoe ze zich gedragen onder behandeling; ze noemen deze drug-naturalized anoikis-genen, of DNAGs.
Twee verborgen types maagtumoren
Toen het team meer dan 800 maagtumoren groepeerde op basis van DNAG-activiteit, kwamen twee grote patronen naar voren. De ene groep tumoren droeg veel genetische mutaties en veranderingen in chromosoomstructuur, wat misschien bedreigend klinkt maar de kanker juist zichtbaarder voor het immuunsysteem kan maken. Deze tumoren vertoonden meer tekenen van actieve immuunaanval en bevatten immuuncellen die kanker kunnen herkennen en bestrijden. De tweede groep zag er heel anders uit: deze kwam vaker voor bij jongere patiënten en bij een bepaald moleculair subtype dat bekendstaat als agressief. Deze tumoren bevonden zich in een sterk onderdrukte omgeving, gedomineerd door structurele ondersteuningscellen en andere componenten die de kanker doorgaans afschermen tegen immuunaanvallen. Patiënten met dit tweede patroon hadden over het algemeen een slechtere prognose.
De behandelingsscore die tumorgedrag afleest
Voortbouwend op deze patronen gebruikten de onderzoekers combinaties van 101 machine learning-benaderingen om een kleinere set van 11 genen te destilleren tot een "treatment-oriented prognostic signature", of TOPS. Deze score deelt patiënten in hoge- en lage-risicogroepen in. In meerdere onafhankelijke patiëntverzamelingen hadden patiënten met hoge TOPS-scores consequent kortere overleving, meer gevorderde ziekte en tumortypes die bekendstaan om invasief gedrag. Tegelijkertijd waren tumoren met hoge TOPS minder geneigd te reageren op zowel chemotherapie als immuuncheckpointremmers, terwijl lage-TOPS-tumoren betere reacties en langere overleving na immunotherapie lieten zien. De score presteerde beter dan traditionele klinische kenmerken zoals leeftijd, geslacht en stadium bij het voorspellen van de uitkomst.
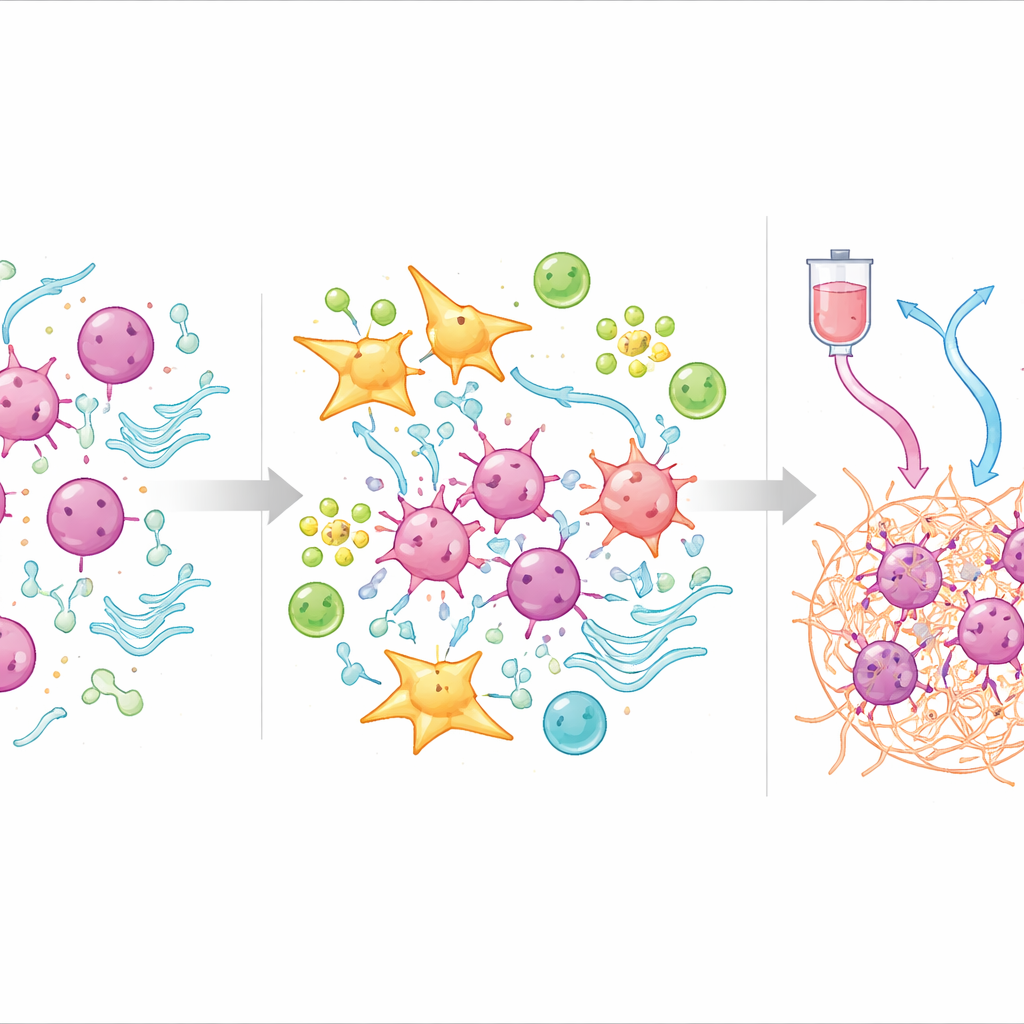
Wat het tumorecosysteem onthult over resistentie
Om te begrijpen waarom de score werkt, wendde het team zich tot single-cell sequencing, waarmee individuele cellen binnen tumoren worden onderzocht. Ze vonden dat hoge-TOPS-tumoren vol zaten met fibroblasten—cellen die helpen bij het bouwen van weefselscaffolding—en bepaalde bloedvatcellen, die een dicht, beschermend omhulsel rond kankercellen vormden. Binnen dit omhulsel volgden fibroblasten een ontwikkelingspad naar een subtype dat sterk communiceert met tumorcellen en routes activeert die verband houden met nieuwe bloedvatvorming, veranderde stofwisseling en immuunsuppressie. Daarentegen bevatten lage-TOPS-tumoren meer T-cellen, B-cellen en plasmacellen die een effectieve immuunrespons kunnen opbouwen en lieten genactiviteitspatronen zien die normale stofwisseling en weefselonderhoud bevorderden in plaats van invasie.
Wat dit kan betekenen voor toekomstige behandelingen
Voor patiënten is de kernboodschap van de studie dat niet alle maagkankers hetzelfde zijn, zelfs niet wanneer ze onder de microscoop vergelijkbaar lijken. Door een 11-genensignatuur af te lezen die verband houdt met hoe cellen omgaan met loslating en hoe het omringende weefsel zich gedraagt, kunnen artsen mogelijk beter voorspellen wie zal profiteren van standaard chemotherapie of immunotherapie, en wie alternatieve of gecombineerde strategieën nodig heeft die ook de ondersteunende cellen en signalen in de tumoromgeving aanpakken. Hoewel het model nog getest moet worden in prospectieve klinische trials, biedt het een veelbelovend stappenplan om de behandeling van maagkanker echt persoonlijker te maken en de kansen voor patiënten met deze ernstige ziekte te verbeteren.
Bronvermelding: Liu, F., Zhou, Y., Xie, Y. et al. Comprehensive machine learning identifies anoikis signatures predicting therapeutic resistance and survival in gastric cancer. Sci Rep 16, 11571 (2026). https://doi.org/10.1038/s41598-026-38996-5
Trefwoorden: maagkanker, behandelingsresistentie, tumor-micro-omgeving, immunotherapie-respons, machine learning-biomarkers