Clear Sky Science · sv
Omfattande maskininlärning identifierar anoikis-signaturer som förutsäger terapeutisk resistens och överlevnad vid magsäckscancer
Varför denna forskning är viktig för patienter
Magsäckscancer är fortfarande en av de dödligaste cancerformerna globalt, framför allt eftersom många tumörer slutar svara på cytostatika och nya immunoterapier. Denna studie ställer en enkel men avgörande fråga: kan vi avläsa tumörcellernas och deras omgivnings molekylära ”överlevnadstrick” för att förutsäga vilka patienter som kommer att vara resistenta mot behandling och vilka som får nytta av den? Genom att gräva i tusentals gener med moderna maskininlärningsmetoder bygger forskarna en kraftfull poäng som kan hjälpa läkare att välja mer effektiva, individualiserade behandlingar för personer med magsäckscancer.
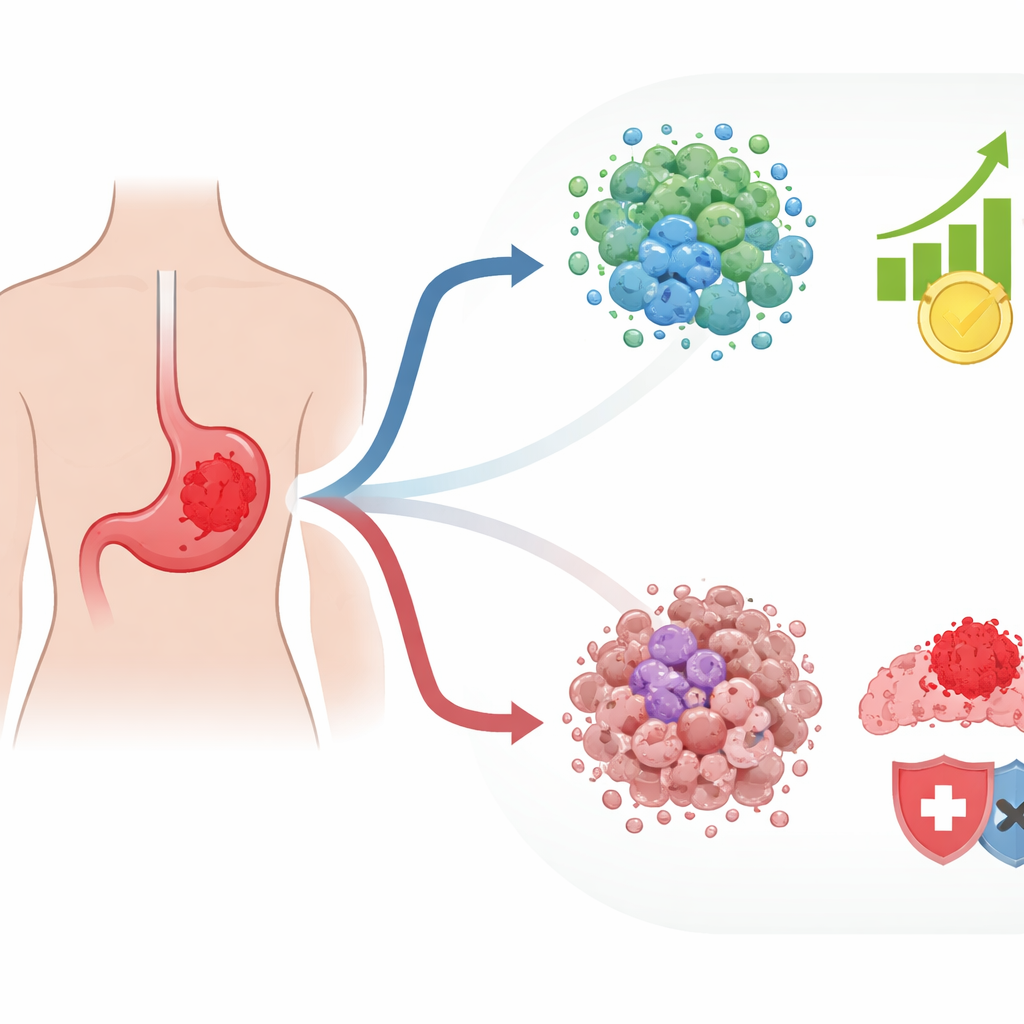
Hur tumörceller undviker sina naturliga säkerhetskontroller
Normala celler är utrustade med ett självförstörande program som aktiveras när de förlorar sin rätta plats i vävnaden, en process som kallas detachment‑induced cell death. Cancerceller lär sig ofta att undvika detta öde, vilket gör att de kan sprida sig och ge upphov till nya tumörer. Författarna fokuserade på gener kopplade till denna detacheringsrespons och på hur de relaterar till tumörers känslighet för läkemedel. Genom att använda tio stora offentliga databaser för magsäckscancer korsrefererade de genset som hör till celldöd, känslighet eller resistens mot kemoterapi och svar på immunterapi. Ur detta komplexa överlapp destillerade de fram 125 nyckelgener som både speglar hur lätt celler undviker detachment‑induced death och hur de beter sig under behandling; de kallar dessa drug‑naturalized anoikis genes, eller DNAGs.
Två dolda typer av magsäckstumörer
När teamet grupperade mer än 800 magsklyftstumörer baserat på DNAG‑aktivitet framträdde två huvudsakliga mönster. En grupp tumörer bar på många genetiska mutationer och förändringar i kromosomstruktur, vilket kan låta allvarligt men som faktiskt kan göra cancern mer synlig för immunsystemet. Dessa tumörer visade fler tecken på aktiv immunattack och inkluderade immunceller som kan känna igen och bekämpa cancer. Den andra gruppen såg mycket annorlunda ut: den förekom oftare hos yngre patienter och i en särskild molekylär subtyp som är känd för att vara aggressiv. Dessa tumörer låg i en starkt undertryckt miljö dominerad av stödjeceller och andra komponenter som tenderar att skydda cancern från immunsvar. Patienter med detta andra mönster hade sämre prognos totalt sett.
Behandlingspoängen som läser tumörbeteende
Med utgångspunkt i dessa mönster använde forskarna kombinationer av 101 maskininlärningsmetoder för att destillera en mindre uppsättning på 11 gener till en ”behandlingsorienterad prognostisk signatur”, eller TOPS. Denna poäng delar in patienter i hög‑ respektive lågriskgrupper. I flera oberoende patientserier hade de med höga TOPS‑poäng konsekvent kortare överlevnad, mer avancerad sjukdom och tumörtyper kända för invasivt beteende. Samtidigt var tumörer med hög TOPS mindre benägna att svara på både kemoterapi och immuncheckpoint‑läkemedel, medan låg‑TOPS‑tumörer visade bättre svar och längre överlevnad efter immunterapi. Poängen överträffade traditionella kliniska variabler såsom ålder, kön och stadium när det gällde att förutsäga utfall.
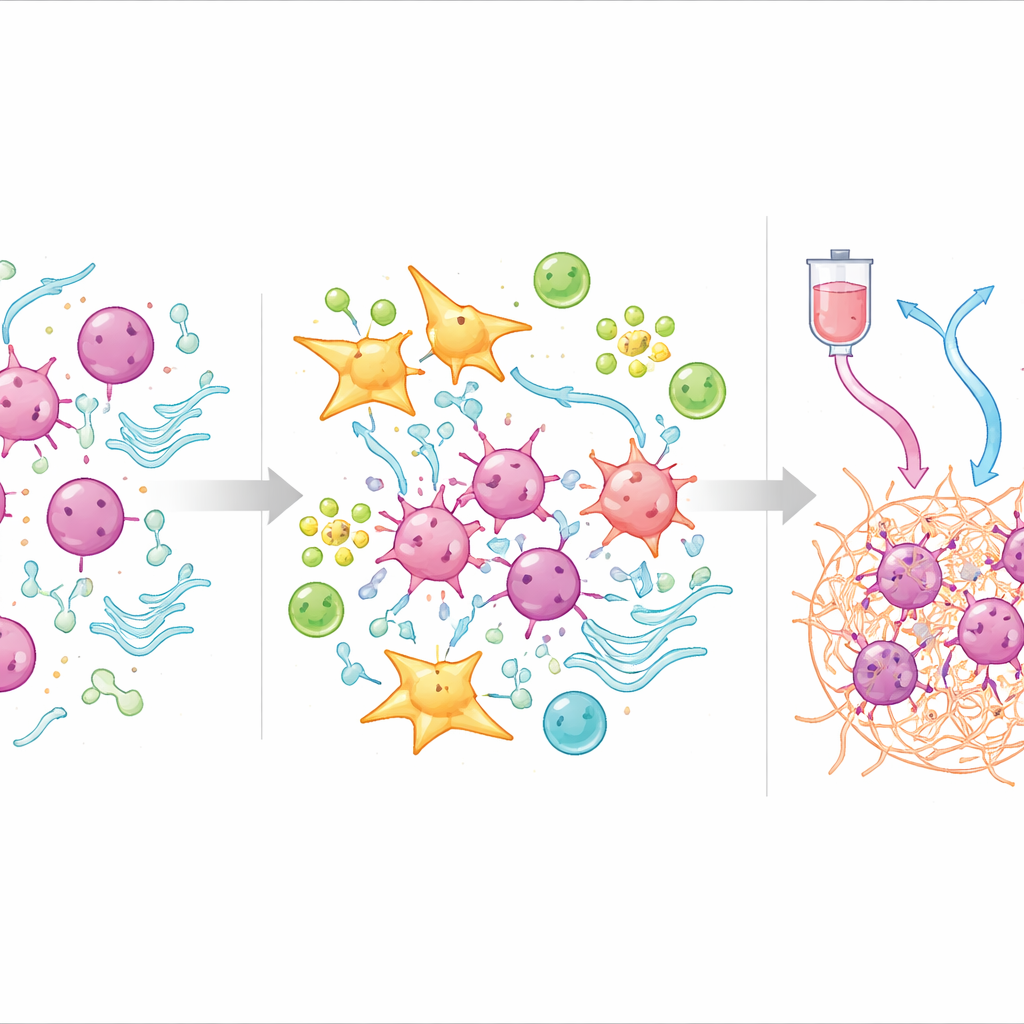
Vad tumörekosystemet avslöjar om resistens
För att förstå varför poängen fungerar vände teamet sig till enkelcellssekvensering, som undersöker enskilda celler inom tumörer. De fann att hög‑TOPS‑tumörer var fyllda av fibroblaster — celler som bygger vävnadens stomme — och vissa blodkärlsceller, vilket bildar ett tätt, skyddande skal runt cancercellerna. Inom detta skal följde fibroblasterna en utvecklingsbana mot en subtyp som kommunicerar starkt med tumörceller och aktiverar vägar kopplade till ny blodkärlsbildning, förändrad metabolism och immunsuppression. I kontrast innehöll låg‑TOPS‑tumörer fler T‑celler, B‑celler och plasmaceller som kan genomföra en effektiv immunattack och visade genaktivitetsmönster som gynnade normal metabolism och vävnadsunderhåll snarare än invasion.
Vad detta kan innebära för framtida behandling
För patienter är studiens huvudbudskap att inte alla magsäckstumörer är likadana, även när de ser lika ut i mikroskopet. Genom att avläsa en 11‑geners signatur relaterad till hur celler hanterar detachment och hur omgivande vävnad beter sig kan läkare en dag bättre förutsäga vilka som får nytta av standardkemoterapi eller immunterapi, och vilka som kan behöva alternativa eller kombinerade strategier som också riktar sig mot stödjecellerna och signalerna i tumörens närområde. Även om modellen fortfarande behöver prövas i prospektiva kliniska prövningar erbjuder den en lovande färdplan för att göra magsäckscancerbehandling mer verkligt personaliserad och förbättra utsikterna för patienter som står inför denna svåra sjukdom.
Citering: Liu, F., Zhou, Y., Xie, Y. et al. Comprehensive machine learning identifies anoikis signatures predicting therapeutic resistance and survival in gastric cancer. Sci Rep 16, 11571 (2026). https://doi.org/10.1038/s41598-026-38996-5
Nyckelord: magsäckscancer, behandlingsresistens, tumörmikromiljö, immunoterapisvar, biomarkörer från maskininlärning