Clear Sky Science · fr
Apprentissage automatique complet identifie des signatures d'anoïkose prédisant la résistance thérapeutique et la survie dans le cancer gastrique
Pourquoi cette recherche compte pour les patients
Le cancer de l’estomac reste l’un des cancers les plus meurtriers dans le monde, en grande partie parce que de nombreuses tumeurs cessent de répondre à la chimiothérapie et aux nouvelles immunothérapies. Cette étude pose une question simple mais cruciale : peut‑on lire les « astuces de survie » moléculaires des cellules tumorales et de leur environnement pour prédire quels patients résisteront au traitement et lesquels en bénéficieront ? En exploitant des milliers de gènes avec des méthodes modernes d’apprentissage automatique, les chercheurs élaborent un score puissant qui pourrait aider les médecins à choisir des thérapies plus efficaces et personnalisées pour les personnes atteintes de cancer gastrique.
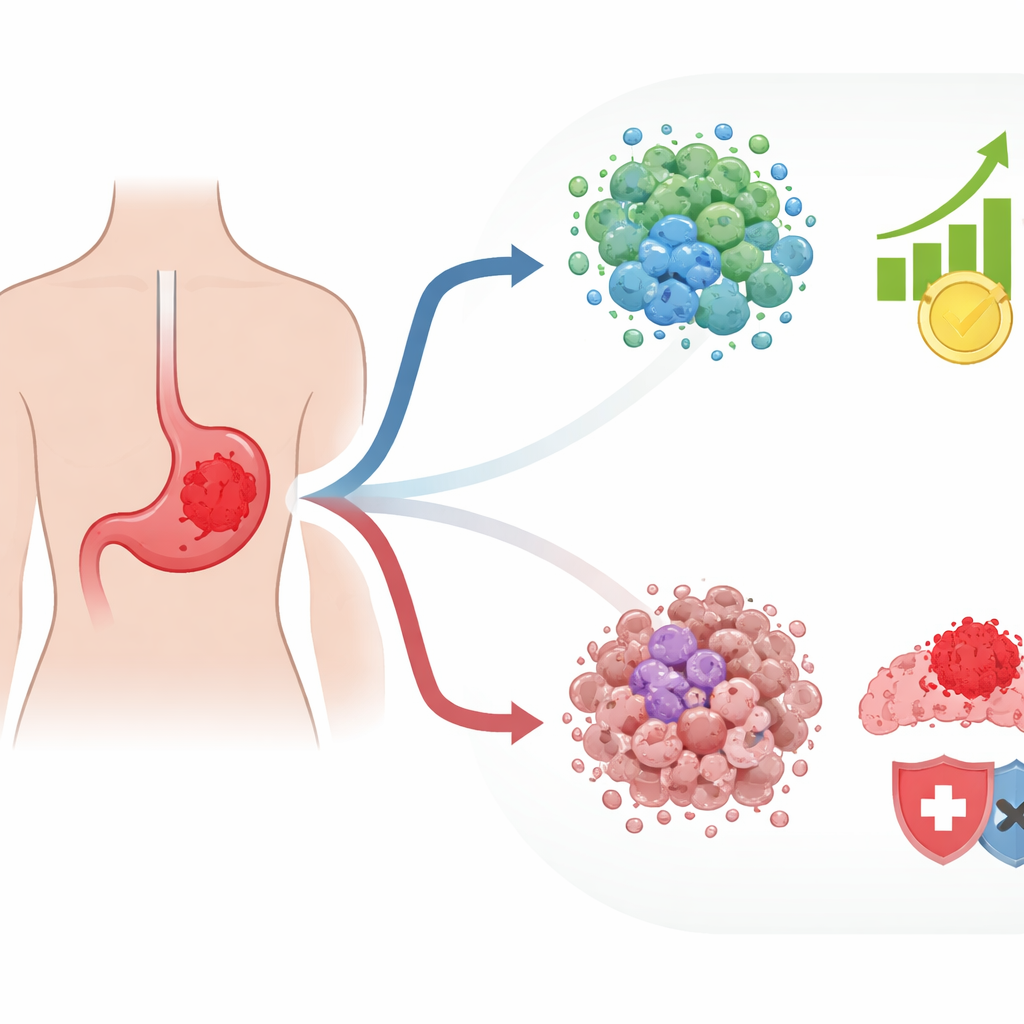
Comment les cellules tumorales échappent à leurs contrôles naturels
Les cellules normales possèdent un programme d’autodestruction qui s’active lorsqu’elles perdent leur ancrage tissulaire, un processus appelé mort cellulaire induite par le détachement. Les cellules cancéreuses apprennent souvent à éviter ce destin, ce qui leur permet de se disséminer et d’ensemencer de nouvelles tumeurs. Les auteurs se sont concentrés sur les gènes liés à cette réponse au détachement et sur leur relation avec la manière dont les tumeurs réagissent aux médicaments. En utilisant dix grandes bases de données publiques sur le cancer gastrique, ils ont recoupé des ensembles de gènes associés à la mort cellulaire, à la sensibilité ou à la résistance à la chimiothérapie, et à la réponse à l’immunothérapie. À partir de ce chevauchement complexe, ils ont isolé 125 gènes clés qui reflètent à la fois la facilité avec laquelle les cellules échappent à la mort par détachement et leur comportement sous traitement ; ils appellent ces gènes « gènes d’anoïkose naturalisés par les médicaments », ou DNAGs.
Deux types cachés de tumeurs gastriques
Lorsque l’équipe a regroupé plus de 800 tumeurs gastriques selon l’activité des DNAGs, deux schémas majeurs sont apparus. Un groupe de tumeurs présentait de nombreuses mutations génétiques et des altérations de la structure chromosomique, ce qui peut sembler inquiétant mais peut rendre le cancer plus visible au système immunitaire. Ces tumeurs montraient davantage de signes d’attaque immunitaire active et incluaient des cellules immunitaires capables de reconnaître et de combattre le cancer. Le second groupe était très différent : il survenait plus souvent chez des patients plus jeunes et appartenait à un sous‑type moléculaire connu pour son agressivité. Ces tumeurs évoluaient dans un environnement fortement immunosupprimé dominé par des cellules de soutien structurel et d’autres composants qui ont tendance à protéger la tumeur de l’attaque immunitaire. Les patients présentant ce second profil avaient un pronostic global plus mauvais.
Le score thérapeutique qui lit le comportement tumoral
À partir de ces schémas, les chercheurs ont combiné 101 approches d’apprentissage automatique pour réduire à un ensemble plus petit de 11 gènes une « signature pronostique orientée traitement », ou TOPS. Ce score divise les patients en groupes à risque élevé ou faible. Dans plusieurs cohortes indépendantes, les patients avec un score TOPS élevé présentaient de façon consistante une survie plus courte, une maladie plus avancée et des types tumoraux connus pour leur comportement invasif. Parallèlement, les tumeurs à score TOPS élevé répondaient moins aux chimiothérapies et aux inhibiteurs de points de contrôle immunitaire, tandis que les tumeurs à faible TOPS montraient de meilleures réponses et une survie prolongée après immunothérapie. Le score surpassait les caractéristiques cliniques traditionnelles telles que l’âge, le sexe et le stade pour prédire le résultat.
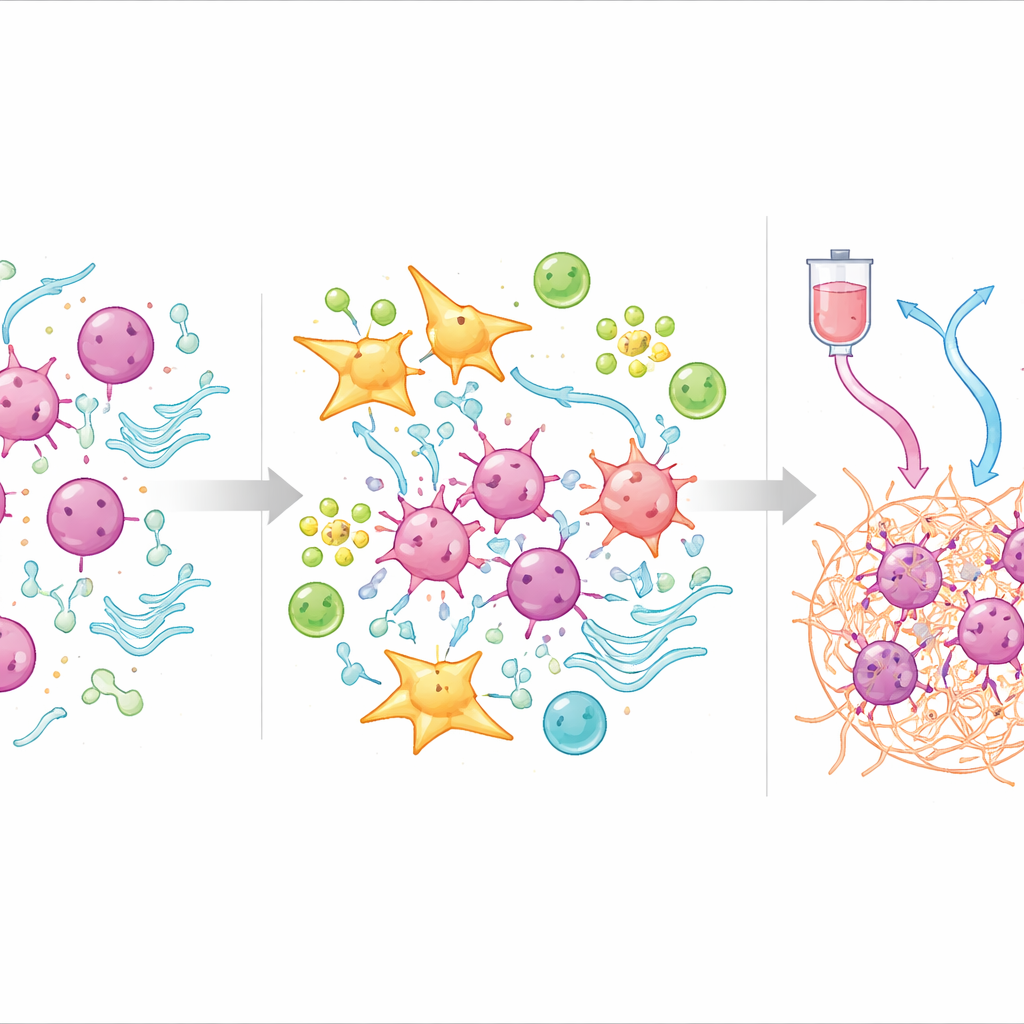
Ce que l’écosystème tumoral révèle sur la résistance
Pour comprendre pourquoi le score fonctionne, l’équipe s’est tournée vers le séquençage unicellulaire, qui analyse les cellules individuelles au sein des tumeurs. Ils ont constaté que les tumeurs à TOPS élevé étaient remplies de fibroblastes — des cellules qui construisent l’ossature tissulaire — et de certains types de cellules vasculaires, formant une couche dense et protectrice autour des cellules cancéreuses. Au sein de cette coque, les fibroblastes suivaient une trajectoire de développement vers un sous‑type qui communique fortement avec les cellules tumorales et active des voies liées à l’angiogenèse, au métabolisme altéré et à l’immunosuppression. En revanche, les tumeurs à faible TOPS contenaient davantage de cellules T, de cellules B et de plasmocytes capables de monter une réponse immunitaire efficace et montraient des profils d’expression génique favorisant un métabolisme normal et le maintien tissulaire plutôt que l’invasion.
Ce que cela pourrait signifier pour les traitements futurs
Pour les patients, le message principal de l’étude est que tous les cancers de l’estomac ne se valent pas, même lorsqu’ils se ressemblent au microscope. En lisant une signature de 11 gènes liée à la façon dont les cellules gèrent le détachement et au comportement du tissu environnant, les médecins pourraient un jour mieux prédire qui bénéficiera de la chimiothérapie ou de l’immunothérapie standard, et qui nécessitera des stratégies alternatives ou combinées ciblant également les cellules de soutien et les signaux du microenvironnement tumoral. Bien que le modèle doive encore être testé dans des essais cliniques prospectifs, il offre une feuille de route prometteuse pour personnaliser davantage le traitement du cancer gastrique et améliorer les chances des patients confrontés à cette maladie difficile.
Citation: Liu, F., Zhou, Y., Xie, Y. et al. Comprehensive machine learning identifies anoikis signatures predicting therapeutic resistance and survival in gastric cancer. Sci Rep 16, 11571 (2026). https://doi.org/10.1038/s41598-026-38996-5
Mots-clés: cancer gastrique, résistance au traitement, microenvironnement tumoral, réponse à l’immunothérapie, biomarqueurs apprentissage automatique