Clear Sky Science · pl
Wszechstronne uczenie maszynowe identyfikuje sygnatury anoikis przewidujące oporność na leczenie i przeżycie w raku żołądka
Dlaczego te badania są ważne dla pacjentów
Rak żołądka pozostaje jednym z najgroźniejszych nowotworów na świecie, w dużej mierze dlatego, że wiele guzów przestaje reagować na chemioterapię i nowe immunoterapie. Badanie stawia proste, lecz istotne pytanie: czy możemy odczytać molekularne „sztuczki przetrwania” komórek nowotworowych i ich otoczenia, aby przewidzieć, którzy pacjenci będą odporni na leczenie, a którzy odniosą korzyść? Przeszukując tysiące genów przy użyciu nowoczesnych metod uczenia maszynowego, autorzy skonstruowali silny wskaźnik, który może pomóc lekarzom w doborze skuteczniejszych, spersonalizowanych terapii dla osób z rakiem żołądka.
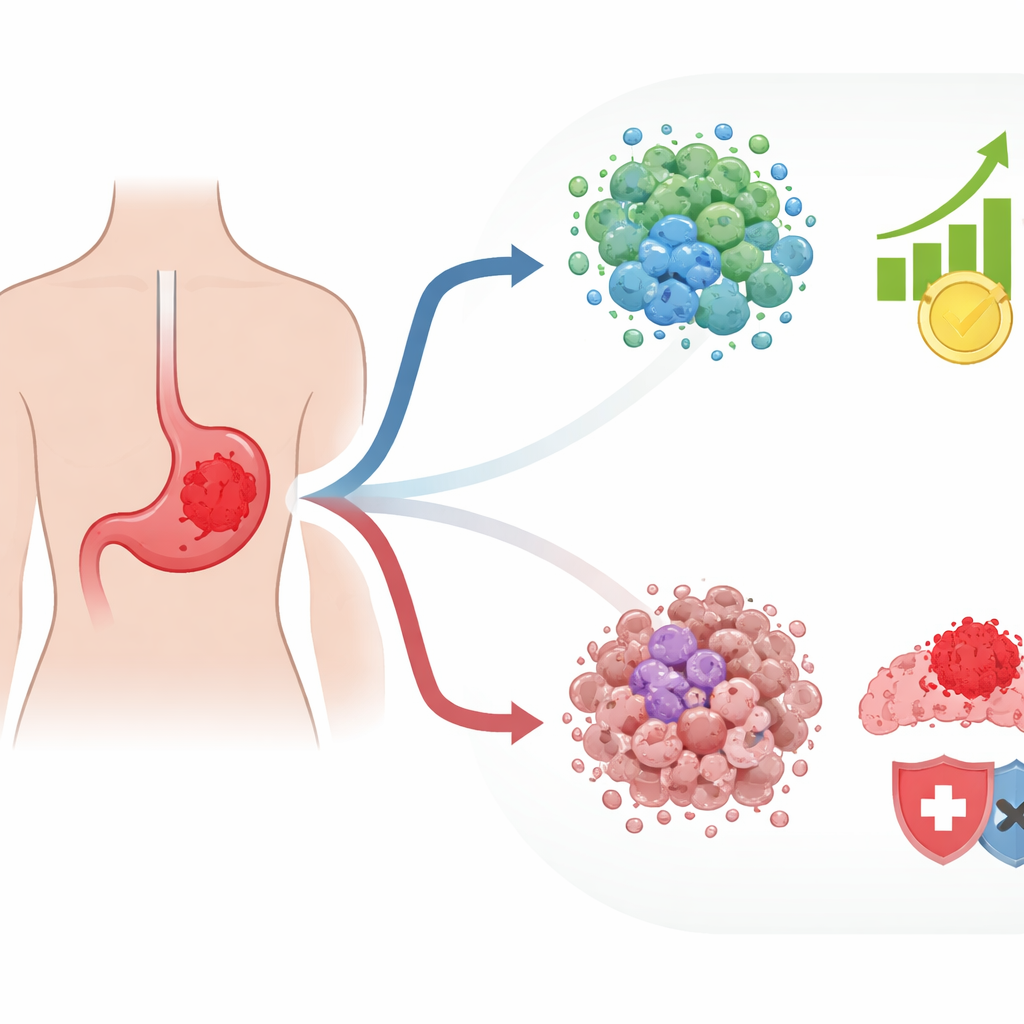
Jak komórki nowotworowe unikają naturalnych mechanizmów bezpieczeństwa
Normalne komórki posiadają program samobójczy, który uruchamia się, gdy tracą swoje prawidłowe zakotwiczenie w tkance — proces zwany śmiercią komórkową indukowaną odłączeniem. Komórki nowotworowe często uczą się omijać ten los, co pozwala im na rozprzestrzenianie się i tworzenie odległych przerzutów. Autorzy skupili się na genach związanych z tą odpowiedzią na odłączenie oraz na tym, jak korelują one z wrażliwością lub opornością na leki. Korzystając z 10 dużych publicznych baz danych dotyczących raka żołądka, skrosowali zestawy genów powiązane ze śmiercią komórek, wrażliwością lub opornością na chemioterapię oraz odpowiedzią na immunoterapię. Z tego złożonego nakładania wyodrębnili 125 kluczowych genów, które zarówno odzwierciedlają zdolność komórek do unikania śmierci indukowanej odłączeniem, jak i ich zachowanie pod wpływem leczenia; nazwali je zneutralizowanymi przez leki genami anoikis, czyli DNAGs.
Dwa ukryte typy guzów żołądka
Gdy zespół pogrupował ponad 800 guzów żołądka na podstawie aktywności DNAG, wyłoniły się dwa główne wzorce. Jedna grupa guzów miała wiele mutacji genetycznych i zmian w strukturze chromosomów, co może brzmieć groźnie, ale w praktyce może sprawić, że nowotwór staje się bardziej widoczny dla układu odpornościowego. Te guzy wykazywały więcej oznak aktywnego ataku odpornościowego i zawierały komórki immunologiczne zdolne rozpoznawać i zwalczać nowotwór. Druga grupa wyglądała bardzo inaczej: występowała częściej u młodszych pacjentów i wiązała się z określonym molekularnym podtypem znanym z agresywnego przebiegu. Te guzy znajdowały się w silnie stłumionym środowisku zdominowanym przez komórki podporowe i inne składniki, które zwykle chronią nowotwór przed atakiem immunologicznym. Pacjenci z tym drugim profilem mieli gorsze wyniki ogólne.
Wskaźnik terapeutyczny odczytujący zachowanie guza
Wykorzystując te wzorce, badacze zastosowali kombinacje 101 metod uczenia maszynowego, aby sprowadzić zestaw do 11 genów tworzących „prognostyczną sygnaturę ukierunkowaną na leczenie” (TOPS). Ten wskaźnik dzieli pacjentów na grupy wysokiego i niskiego ryzyka. W kilku niezależnych zbiorach pacjentów osoby z wysokim wynikiem TOPS konsekwentnie cechowały się krótszym przeżyciem, bardziej zaawansowaną chorobą i typami guzów znanymi z inwazyjnego zachowania. Jednocześnie guzy o wysokim TOPS rzadziej reagowały zarówno na chemioterapię, jak i na inhibitory punktów kontrolnych układu odpornościowego, podczas gdy guzy o niskim TOPS wykazywały lepsze odpowiedzi i dłuższe przeżycie po immunoterapii. Wskaźnik przewyższał tradycyjne cechy kliniczne, takie jak wiek, płeć czy stadium choroby, w przewidywaniu wyników.
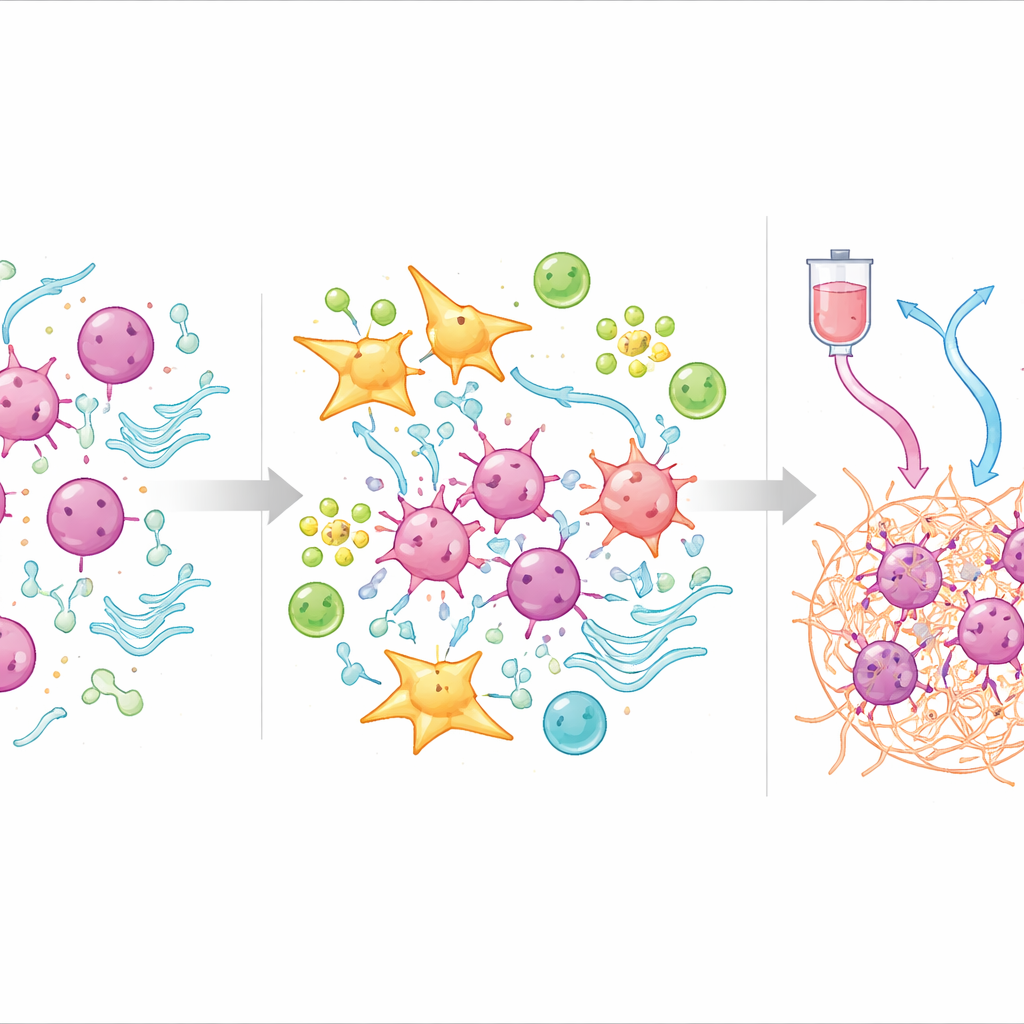
Co ekosystem guza ujawnia o oporności
Aby zrozumieć, dlaczego wskaźnik działa, zespół sięgnął po sekwencjonowanie pojedynczych komórek, które bada poszczególne komórki w obrębie guzów. Stwierdzili, że guzy o wysokim TOPS były wypełnione fibroblastami — komórkami budującymi rusztowanie tkanki — oraz określonymi komórkami naczyniowymi, tworząc gęstą, ochronną otoczkę wokół komórek nowotworowych. W obrębie tej otoczki fibroblasty podążały ścieżką rozwojową w kierunku podtypu, który silnie komunikuje się z komórkami guza i aktywuje szlaki związane z angiogenezą, zmienionym metabolizmem i supresją układu odpornościowego. Dla porównania, guzy o niskim TOPS zawierały więcej komórek T, komórek B i plazmatycznych, które mogą przeprowadzić skuteczny atak immunologiczny, i wykazywały wzorce aktywności genów sprzyjające normalnemu metabolizmowi i utrzymaniu tkanki zamiast inwazji.
Co to może oznaczać dla przyszłego leczenia
Dla pacjentów główne przesłanie badania jest takie, że nie wszystkie raki żołądka są takie same, nawet jeśli wyglądają podobnie pod mikroskopem. Odczytując 11-genową sygnaturę związaną z tym, jak komórki radzą sobie z odłączeniem i jak zachowuje się otaczająca tkanka, lekarze mogą w przyszłości lepiej przewidywać, kto skorzysta na standardowej chemioterapii lub immunoterapii, a kto będzie potrzebował alternatywnych lub skojarzonych strategii celujących również w komórki podporowe i sygnały w otoczeniu guza. Choć model wymaga jeszcze potwierdzenia w prospektywnych badaniach klinicznych, daje obiecującą mapę drogową prowadzącą do bardziej rzeczywiście spersonalizowanego leczenia raka żołądka i poprawy rokowań dla pacjentów z tą trudną chorobą.
Cytowanie: Liu, F., Zhou, Y., Xie, Y. et al. Comprehensive machine learning identifies anoikis signatures predicting therapeutic resistance and survival in gastric cancer. Sci Rep 16, 11571 (2026). https://doi.org/10.1038/s41598-026-38996-5
Słowa kluczowe: rak żołądka, oporność na leczenie, mikrośrodowisko guza, odpowiedź na immunoterapię, biomarkery uczenia maszynowego