Clear Sky Science · tr
Hassas CAR T hücre tedavisi için test platformu olarak akciğer tümoroidleri
Hastalar için Küçük Akciğer Modelleri Neden Önemli
Akciğer kanseri, her tümörün farklı olması ve sıklıkla tedaviden kaçmayı öğrenmesi nedeniyle dünyanın en ölümcül kanseri olmaya devam ediyor. Bu çalışma, laboratuvarda hasta‑özgü akciğer tümörlerinin küçük replikalarını yetiştirme ve bunları CAR T hücreleri olarak adlandırılan gelişmiş immün tedaviler için bir test alanı olarak kullanma yöntemini tanıtıyor. Araştırmacılar, aynı hastadan alınan eşleşen sağlıklı akciğer organoidleriyle bu tümör “mini‑organlarını” karşılaştırarak, doktorların bir gün hangi tedavilerin işe yarayacağını, hangilerinin başarısız olacağını ve hastayı tedavi etmeden önce tehlikeli yan etkilerden nasıl kaçınılacağını tahmin edebileceğini gösteriyor.
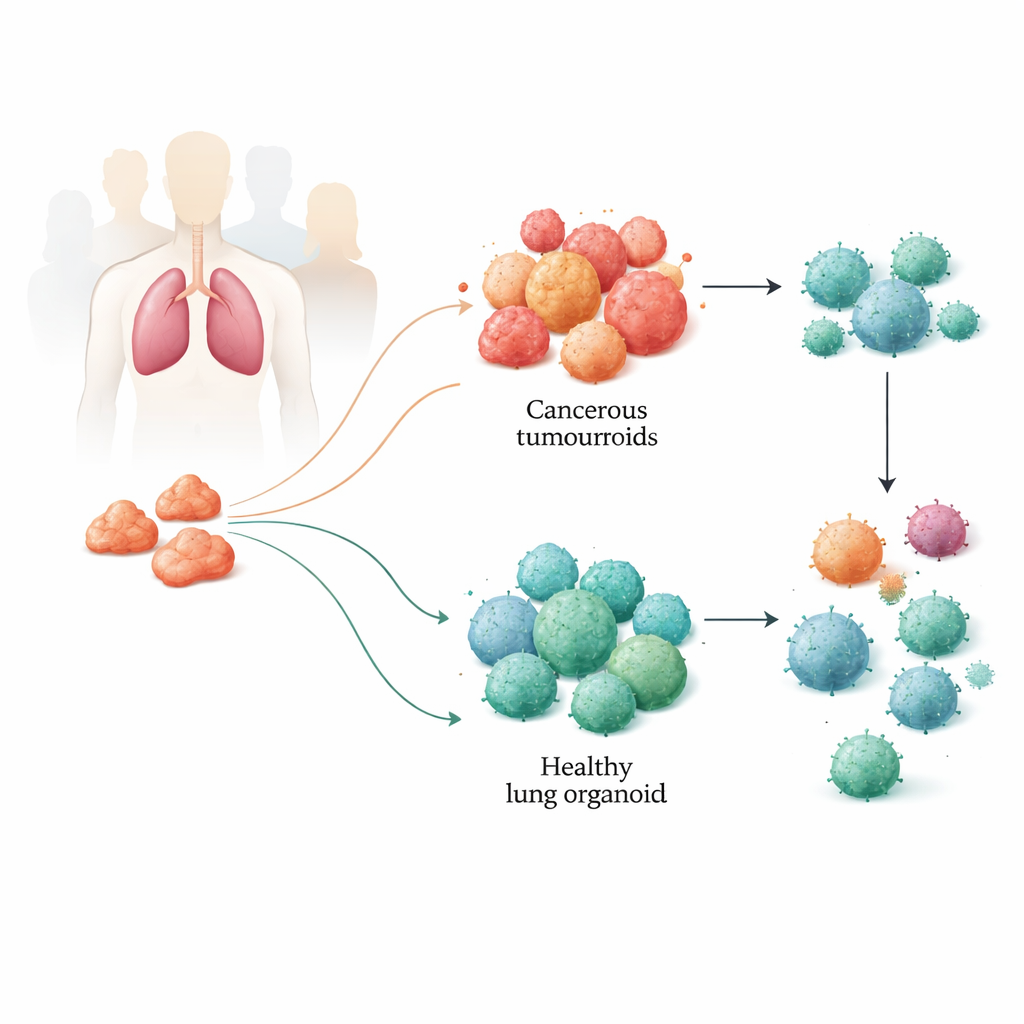
Hasta Dokusundan Küçük Akciğerler İnşa Etmek
Ekip, akciğer kanseri ameliyatı geçiren hastalardan tümör örnekleri ve yakınındaki sağlıklı akciğer dokusunu topladı. Bu örneklerden, üç boyutlu yapılar olan organoidler yetiştirdiler: kanser dokusundan tümoroidler ve normal akciğerden sağlıklı organoidler. Bu küçük küreler kendi kendine organizasyon gösteriyor ve aylarca canlı tutulabiliyor. Dikkatli genetik, epigenetik ve protein düzeyindeki analizler, tümoroidlerin özgün tümörlerin temel moleküler özelliklerini koruduğunu; yaygın akciğer kanseri mutasyonları ve karmaşık hücre tipi karışımını içerdiğini gösterdi. Sağlıklı organoidler ise kanser dışı akciğer dokusunun ayırt edici özelliklerini muhafaza ederek araştırmacılara her hastanın hastalığı ve normal akciğerinin güvenilir bir yan‑yana modelini sağladı.
Gerçek Dünya İlaç Yanıtlarını Yansıtmak
Bu mini‑organların hastalarda olanları gerçekten yansıtıp yansıtmadığını test etmek için araştırmacılar, tümoroidleri hastaların daha önce aldığı aynı kemoterapi ve hedefe yönelik ilaçlara maruz bıraktı. Canlı hücre görüntüleme ve canlılık testleri kullanarak, tümoroidlerin sıklıkla klinikteki özgün tümörler gibi davrandığını buldular: ilaca dirençli olan hastalardan alınan örnekler kapta da dirençli olma eğilimindeydi; kısmi yanıt verenlerden alınan tümoroidler daha duyarlıydı. Binlerce proteini aynı anda ölçen proteomik profilleme, platin bazlı kemoterapiye kötü yanıtlarla daha önce ilişkilendirilmiş moleküllerin yüksek düzeyleri gibi ilaç direnciyle bağlantılı desenleri ortaya çıkardı. Bu bulgular, tümoroidlerin belirli bir ilacın bir hasta için faydalı olup olmayacağını önceden tahmin etmekte kullanılabileceğini düşündürüyor.
Yeni Nesil İmmün Hücreleri Özel Olarak Test Etmek
Çalışmanın merkezinde, hastanın T hücrelerinin kanser hücrelerindeki belirli işaretleri tanıyacak şekilde mühendislik yapıldığı güçlü bir yaklaşım olan CAR T hücre tedavisini kişiselleştirmek için bir iş akışı bulunuyor. Bilim insanları önce hücre yüzeyindeki potansiyel hedef moleküller için tümör ve sağlıklı dokuları ve bunların eşleşen organoidlerini taradı. Ardından, HER2 veya PDL1 gibi bazı akciğer kanserlerinde bulunan umut verici hedefleri tanımak için viral olmayan bir gen düzenleme yöntemi kullanarak CAR T hücre panelleri ürettiler. Bu CAR T hücrelerini tümoroidlerle ve sağlıklı organoidlerle ortak kültüre alarak, bağışıklık hücrelerinin ne kadar güçlü aktifleştiğini, ne kadar tümör hasarı yaptığını ve sağlıklı benzeri akciğer dokusuna zarar verip vermediğini eş zamanlı olarak değerlendirebildiler.
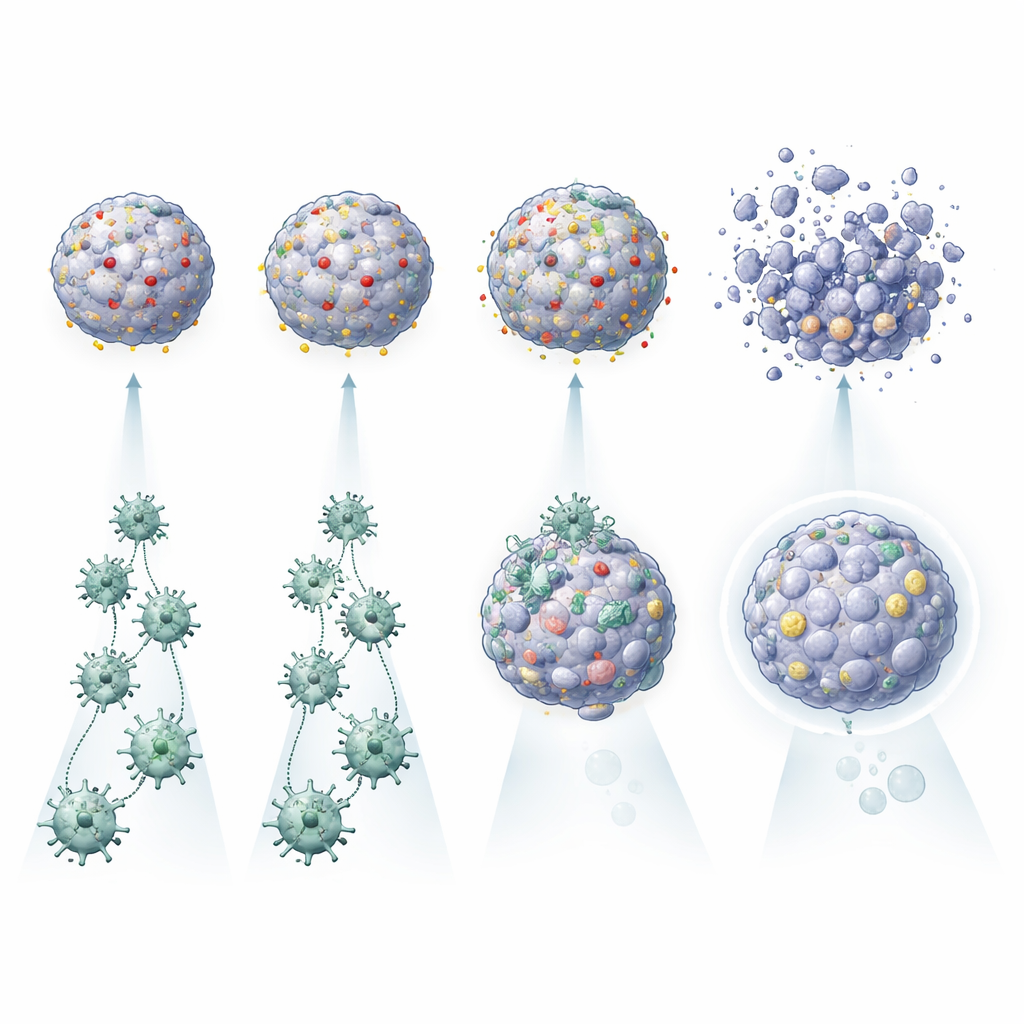
Bazı Tümörlerin Neden CAR T Hücrelerine Direndiğini Ortaya Çıkarmak
Dikkat çeken bir sonuç, yalnızca CAR T hücre aktivasyonunun etkili tümör öldürmeyi garanti etmediğiydi. Bazı hastaların tümoroidlerinde CAR T hücreleri etkinleşip inflamatuar moleküller saldı, ancak kanser mini‑organlarına sadece sınırlı zarar verdiler. Diğerlerinde, özellikle tümör yüzeyinde hedef molekülün çok sayıda kopyasına sahip olanlarda, aynı CAR T hücreleri tümoroidleri çok daha verimli yok etti. Platform ayrıca daha ince etkileri de yakaladı: IL‑6 gibi belirli sitokinleri salgılayan tümoroidler daha iyi CAR T aktivitesini destekliyormuş gibi görünürken; otofaji ve immün kaçış proteinleri bakımından zengin olanlar veya inflamatuar koşullar altında PDL1’i hızla artırabilenler yok edilmesi daha zor olanlardı. Her tümörü kendi sağlıklı organoidleriyle karşılaştırarak, ekip belirli bir CAR tasarımının normal akciğer dokusunu koruyabileceği—veya kabul edilemez riskler oluşturabileceği—hastaları da tanımlayabildi.
Geleceğin Kanser Bakımı İçin Anlamı Ne Olabilir
Daha yalın bir ifadeyle, bu çalışma hasta kaynaklı akciğer tümoroidlerinin hem standart ilaçlar hem de sofistike immün tedaviler için gerçekçi “çarpışma testi kurbanları” olarak hareket edebileceğini gösteriyor. Model, tedaviye gerçek hasta yanıtlarını yeniden üretiyor, neden bazı tümörlerin yenildiğini diğerlerinin neden direnç gösterdiğini ortaya koyuyor ve umut verici bir CAR T yaklaşımının sağlıklı akciğer hücrelerine zarar verip vermeyeceğini vurguluyor. Daha fazla geliştirme gerekse de, bu platform onkologların hastayı risklere maruz bırakmadan önce bir hastanın kendi mini‑tümörlerini kullanarak tedavileri seçmesine ve ince ayar yapmasına—özelleştirilmiş CAR T hücreleri dahil—doğru bir yolu işaret ediyor.
Atıf: Ehlen, L., Farrera-Sal, M., Szyska, M. et al. Lung tumouroids as a testing platform for precision CAR T cell therapy. Nat. Biomed. Eng 10, 815–831 (2026). https://doi.org/10.1038/s41551-025-01594-3
Anahtar kelimeler: akciğer kanseri, organoidler, CAR T hücre tedavisi, kişiselleştirilmiş tıp, immünoterapi direnci