Clear Sky Science · pl
Tumouroidy płuc jako platforma do testowania precyzyjnej terapii CAR T
Dlaczego małe modele płuc są ważne dla pacjentów
Rak płuca pozostaje najgroźniejszym nowotworem na świecie, w dużej mierze dlatego, że każdy guz jest inny i często uczy się unikać leczenia. W tym badaniu opisano metodę hodowli miniaturowych, specyficznych dla pacjenta replik guzów płuca w laboratorium oraz wykorzystania ich jako poligonu do testowania zaawansowanych terapii immunologicznych zwanych komórkami CAR T. Porównując te „mini‑organy” nowotworowe z dopasowanymi zdrowymi organoidami płuc z tego samego pacjenta, badacze pokazują, jak w przyszłości lekarze mogliby przewidywać, które terapie zadziałają, które zawiodą i jak uniknąć niebezpiecznych skutków ubocznych przed rozpoczęciem leczenia pacjenta.
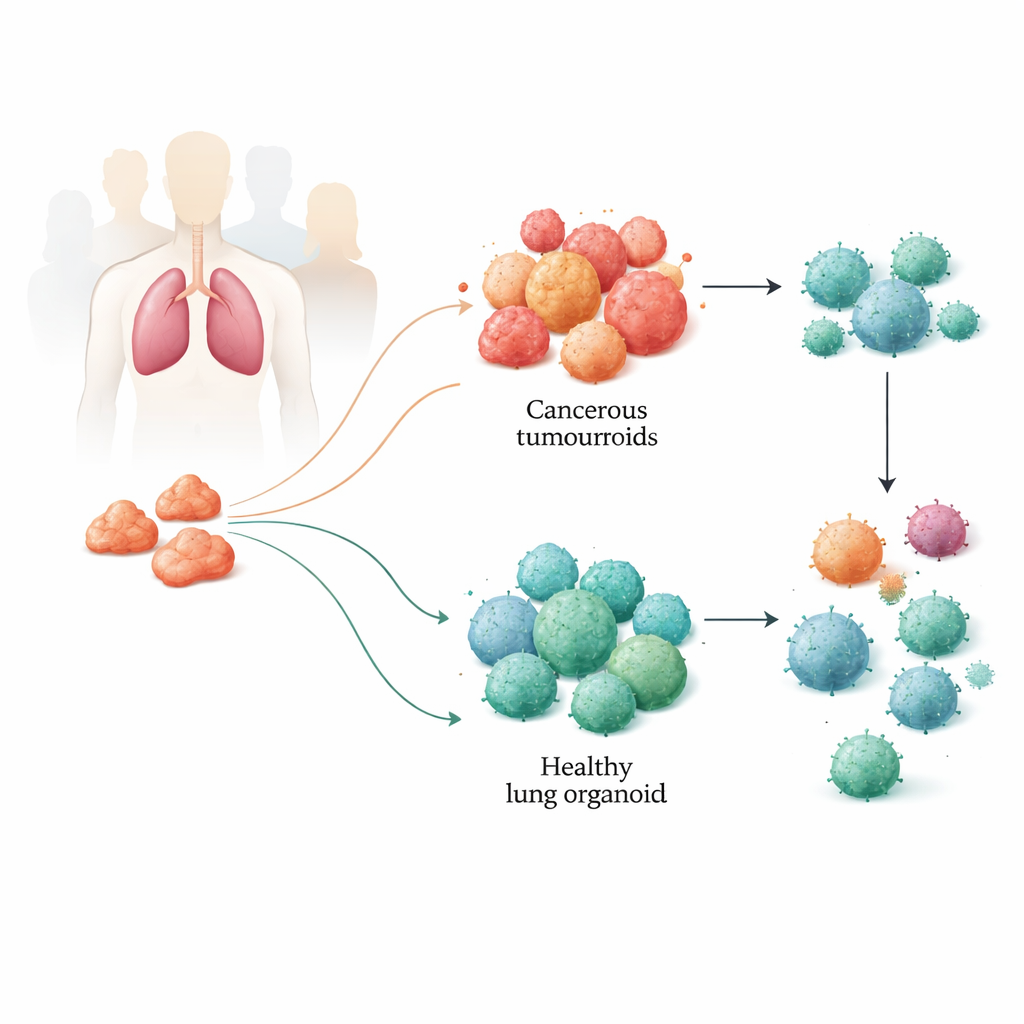
Budowanie miniaturowych płuc z tkanki pacjenta
Zespół pobierał próbki guza i pobliskiej zdrowej tkanki płucnej od pacjentów poddawanych operacji z powodu raka płuca. Z tych próbek hodowano trójwymiarowe struktury znane jako organoidy: tumouroidy z tkanki nowotworowej oraz zdrowe organoidy z normalnego płuca. Te maleńkie sfery samoorganizują się i mogą być utrzymywane przy życiu przez wiele miesięcy. Dokładne analizy genetyczne, epigenetyczne i na poziomie białek wykazały, że tumouroidy zachowały kluczowe cechy molekularne oryginalnych guzów, w tym typowe mutacje raka płuca oraz ich złożony skład komórkowy. Zdrowe organoidy z kolei zachowały cechy tkanek niebędących nowotworem, dając badaczom wiarygodny model „obok siebie” choroby i normalnego płuca konkretnego pacjenta.
Odwzorowanie reakcji na leki w rzeczywistości klinicznej
Aby sprawdzić, czy te mini‑organy rzeczywiście odzwierciedlają to, co dzieje się u pacjentów, badacze wystawili tumouroidy na te same chemioterapeutyki i leki celowane, które pacjenci wcześniej otrzymali. Korzystając z obrazowania żywych komórek i testów żywotności, stwierdzili, że tumouroidy często zachowywały się podobnie jak oryginalne guzy w klinice: próbki od pacjentów, których nowotwory były oporne na dany lek, wykazywały oporność także in vitro, podczas gdy tumouroidy od pacjentów z częściową odpowiedzią były bardziej wrażliwe. Profilowanie proteomiczne — mierzenie tysięcy białek jednocześnie — ujawniło wzorce związane z opornością na leki, takie jak wysokie poziomy molekuł wcześniej powiązanych ze słabymi odpowiedziami na chemioterapię platynową. Wyniki sugerują, że tumouroidy mogłyby służyć do przewidywania, czy dany lek prawdopodobnie pomoże konkretnego pacjenta.
Indywidualne testowanie nowej generacji komórek odpornościowych
Ośrodkiem badania jest procedura dostosowywania terapii komórkami CAR T — potężnego podejścia, w którym komórki T pacjenta są inżynierowane tak, by rozpoznawać konkretne markery na komórkach nowotworowych. Naukowcy najpierw przesiewowo badali tkanki guza i zdrowe tkanki, a także ich dopasowane organoidy, w poszukiwaniu potencjalnych celów na powierzchni komórek. Następnie stworzyli panele komórek CAR T — używając metody edycji genów bez wirusa — aby rozpoznawały obiecujące cele, takie jak HER2 czy PDL1, występujące w niektórych rakach płuca. Wspólna hodowla tych komórek CAR T z tumouroidami i zdrowymi organoidami pozwoliła jednocześnie ocenić, jak silnie komórki odpornościowe się aktywują, jaki powodują uszczerbek w guzie oraz czy uszkadzają tkankę przypominającą zdrowe płuca.
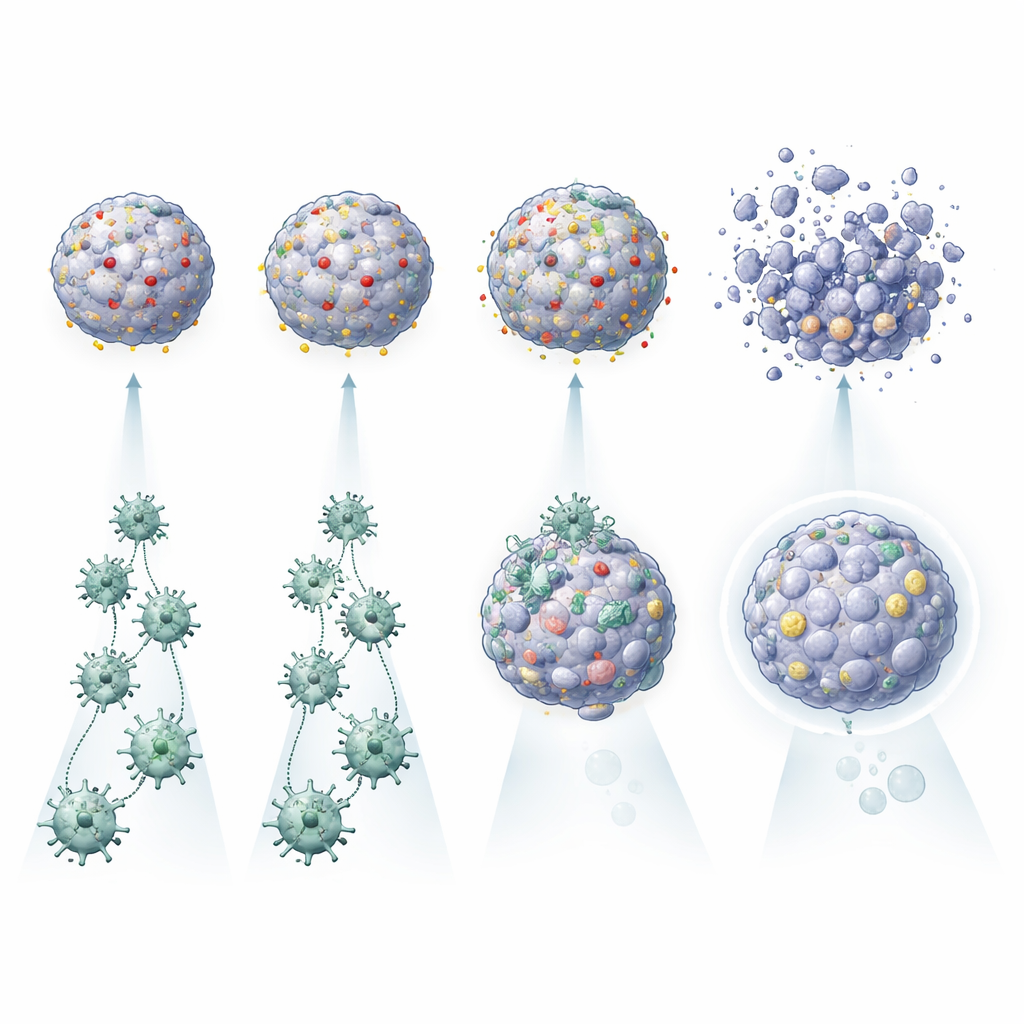
Odkrywanie, dlaczego niektóre guzy są oporne na komórki CAR T
Jednym z uderzających wyników było to, że sama aktywacja komórek CAR T nie gwarantowała skutecznego zabijania guza. W tumouroidach niektórych pacjentów komórki CAR T ulegały aktywacji i wydzielały molekuły zapalne, ale tylko umiarkowanie niszczyły mini‑organy nowotworowe. W innych przypadkach, szczególnie tam, gdzie na powierzchni guza występowało wiele kopii docelowej molekuły, te same komórki CAR T niszczyły tumouroidy znacznie efektywniej. Platforma uchwyciła także subtelniejsze wpływy: tumouroidy wydzielające określone cytokiny, takie jak IL‑6, wydawały się wspierać lepszą aktywność CAR T, podczas gdy te bogate w białka związane z autofagią i uchylaniem się przed układem odpornościowym, albo zdolne do gwałtownego zwiększania ekspresji PDL1 w warunkach zapalnych, były trudniejsze do wyeliminowania. Porównując każdy guz z jego własnymi zdrowymi organoidami, zespół mógł też zidentyfikować pacjentów, dla których dany projekt CAR mógłby oszczędzić normalną tkankę płucną — albo wiązać się z nieakceptowalnym ryzykiem.
Co to może znaczyć dla przyszłej opieki onkologicznej
Mówiąc prosto, praca ta pokazuje, że tumouroidy płuc pochodzące od pacjentów mogą działać jak realistyczne „manekiny zderzeniowe” zarówno dla standardowych leków, jak i zaawansowanych terapii immunologicznych. Model odtwarza rzeczywiste odpowiedzi pacjentów na leczenie, ujawnia, dlaczego niektóre guzy ustępują, a inne stają się oporne, oraz wskazuje, kiedy obiecujące podejście CAR T może także uszkodzić zdrowe komórki płuc. Chociaż potrzebne są dalsze udoskonalenia, platforma wskazuje kierunek ku przyszłości, w której onkolodzy używają mini‑guzów pacjenta do wyboru i dopracowania terapii — w tym szytych na miarę komórek CAR T — zanim narazi się pacjenta na ich ryzyko.
Cytowanie: Ehlen, L., Farrera-Sal, M., Szyska, M. et al. Lung tumouroids as a testing platform for precision CAR T cell therapy. Nat. Biomed. Eng 10, 815–831 (2026). https://doi.org/10.1038/s41551-025-01594-3
Słowa kluczowe: rak płuca, organoidy, terapia CAR T, medycyna precyzyjna, oporność na immunoterapię