Clear Sky Science · ru
Тумороиды лёгких как платформа тестирования для персонализированной CAR‑T терапии
Почему крошечные модели лёгких важны для пациентов
Рак лёгкого остаётся самой смертоносной формой рака в мире, отчасти потому, что каждая опухоль уникальна и часто обучается ускользать от лечения. В этом исследовании описан способ вырастить миниатюрные, специфичные для пациента копии лёгочных опухолей в лаборатории и использовать их в качестве полигона для испытаний современных иммунных терапий — клеток CAR‑T. Сравнивая эти «мини‑органы» опухоли с соответствующими здоровыми органоидами лёгкого от того же пациента, исследователи демонстрируют, как в будущем врачи смогут предсказывать, какие терапии сработают, какие — нет, и как избежать опасных побочных эффектов до начала лечения пациента.
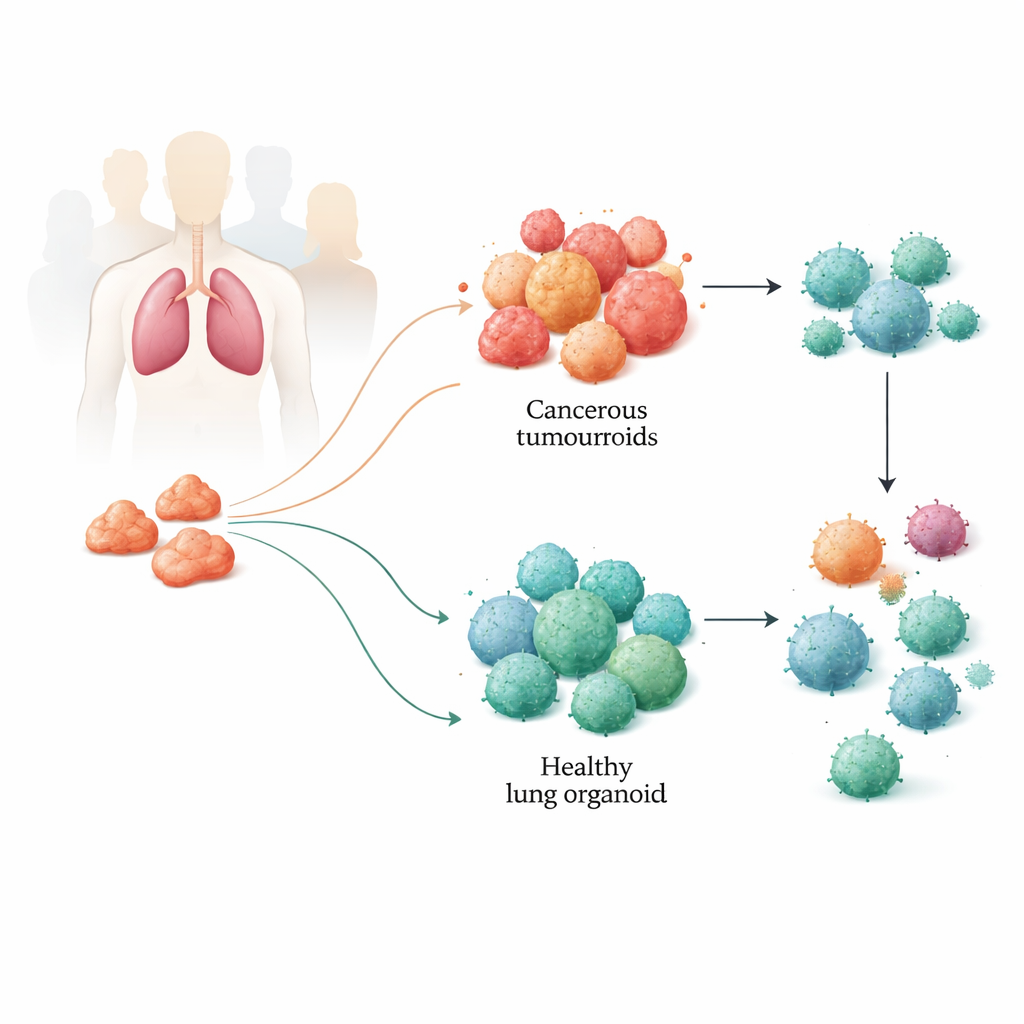
Создание миниатюрных лёгких из ткани пациентов
Команда собрала образцы опухоли и прилегающей здоровой ткани лёгкого у пациентов, перенесших операцию по удалению рака. Из этих образцов они вырастили трёхмерные структуры, известные как органоиды: тумороиды из раковой ткани и здоровые органоиды из нормальной лёгочной ткани. Эти крошечные сферы самоорганизуются и могут сохраняться жизнеспособными в течение многих месяцев. Тщательный генетический, эпигенетический и протеиновый анализ показал, что тумороиды сохраняют ключевые молекулярные особенности исходных опухолей, включая типичные мутации при раке лёгкого и их сложный состав клеточных типов. Здоровые органоиды, в свою очередь, сохраняли признаки незлокачественной лёгочной ткани, предоставляя исследователям надёжную модель «бок о бок» для каждой болезни и нормальной ткани пациента.
Отражение реакций на лекарства в реальном мире
Чтобы проверить, действительно ли эти мини‑органы отражают события у пациентов, исследователи подвергали тумороиды тем же химио‑ и таргетным препаратам, которые уже получили пациенты. С помощью живой микроскопии и тестов на жизнеспособность они обнаружили, что тумороиды часто вели себя как исходные опухоли в клинике: образцы от пациентов с резистентностью к препарату оказывались устойчивыми и в чашке Петри, тогда как тумороиды от частичных ответчиков были более чувствительны. Протеомное профилирование — измерение тысяч белков одновременно — выявило паттерны, связанные с лекарственной резистентностью, например высокие уровни молекул, ранее ассоциированных с плохим ответом на платиновую химиотерапию. Эти результаты позволяют предполагать, что тумороиды можно использовать для прогнозирования того, поможет ли конкретный препарат отдельному пациенту.
Индивидуальное тестирование клеток следующего поколения
Ключевым элементом исследования является конвейер для персонализации CAR‑T терапии — мощного подхода, при котором Т‑клетки пациента генетически модифицируют для распознавания специфических маркеров на раковых клетках. Сначала учёные скринировали опухолевые и здоровые ткани, а также соответствующие органоиды, на предмет потенциальных мишеней на поверхности клеток. Затем они создали панели CAR‑T клеток — используя бесвирусный метод редактирования генов — для распознавания перспективных мишеней, таких как HER2 или PDL1, которые присутствуют в некоторых раках лёгкого. Совместное культивирование этих CAR‑T клеток с тумороидами и здоровыми органоидами позволило одновременно оценить степень активации иммунных клеток, масштабы повреждения опухоли и возможный вред для ткани, похожей на здоровую лёгочную.
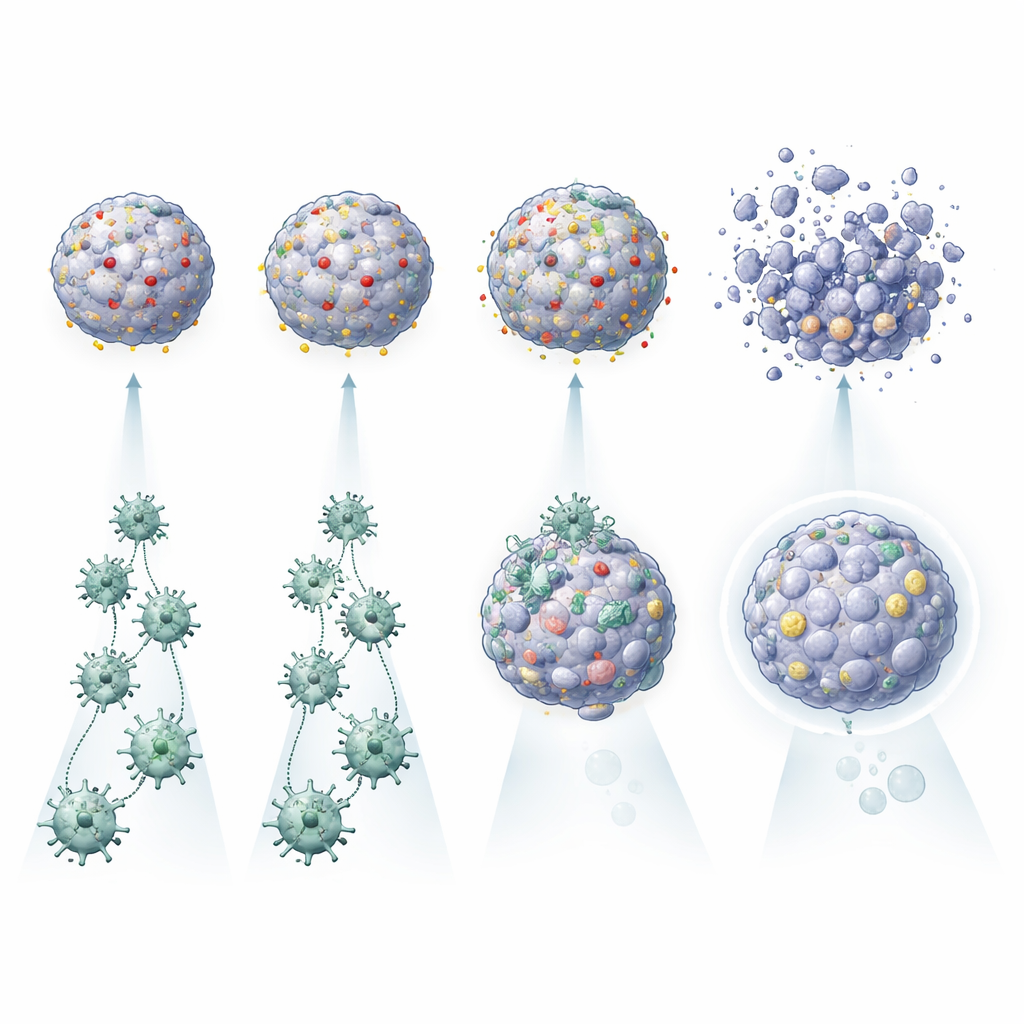
Почему некоторые опухоли сопротивляются CAR‑T клеткам
Одним из поразительных результатов оказалось то, что сама активация CAR‑T клеток не гарантировала эффективного уничтожения опухоли. В тумороидах некоторых пациентов CAR‑T клетки активировались и выделяли провоспалительные молекулы, но при этом лишь умеренно повреждали мини‑органоиды опухоли. В других случаях, особенно при большом числе копий мишени на поверхности опухоли, те же CAR‑T клетки гораздо эффективнее разрушали тумороиды. Платформа также фиксировала более тонкие влияния: тумороиды, секретировавшие определённые цитокины, такие как IL‑6, казались более поддерживающими активность CAR‑T, тогда как тумороиды с высоким содержанием белков, связанных с аутофагией и уклонением от иммунитета, или способные резко повышать экспрессию PDL1 в воспалительных условиях, были труднее ликвидировать. Сравнивая каждую опухоль с её собственными здоровыми органоидами, команда также могла выявлять пациентов, для которых та или иная конструкция CAR могла бы пощадить нормальную ткань лёгкого или, напротив, представлять неприемлемый риск.
Что это может значить для будущего лечения рака
Проще говоря, эта работа показывает, что тумороиды лёгких, полученные от пациентов, могут служить реалистичными «краш‑тестовыми макетами» как для стандартных препаратов, так и для сложных иммунных терапий. Модель воспроизводит ответы реальных пациентов на лечение, объясняет, почему одни опухоли поддаются терапии, а другие сопротивляются, и выявляет случаи, когда перспективный CAR‑T подход может повредить здоровые клетки лёгкого. Хотя необходима дополнительная доработка, эта платформа указывает на будущее, в котором онкологи используют мини‑опухоли пациента для выбора и тонкой настройки терапий — включая индивидуальные CAR‑T клетки — прежде чем подвергать пациента сопутствующим рискам.
Цитирование: Ehlen, L., Farrera-Sal, M., Szyska, M. et al. Lung tumouroids as a testing platform for precision CAR T cell therapy. Nat. Biomed. Eng 10, 815–831 (2026). https://doi.org/10.1038/s41551-025-01594-3
Ключевые слова: рак лёгкого, органоиды, CAR‑T терапия, персонализированная медицина, устойчивость к иммунотерапии