Clear Sky Science · de
Lungen-Tumouroide als Testplattform für präzise CAR‑T‑Zell‑Therapie
Warum winzige Lungenmodelle für Patientinnen und Patienten wichtig sind
Lungenkrebs bleibt weltweit die tödlichste Krebsart, zum großen Teil, weil jeder Tumor verschieden ist und häufig Wege findet, Behandlungen zu umgehen. Diese Studie stellt eine Methode vor, mit der sich miniature, patientenspezifische Nachbildungen von Lungentumoren im Labor züchten lassen, um sie als Prüfstand für fortgeschrittene Immuntherapien, sogenannte CAR‑T‑Zellen, zu nutzen. Indem die Forschenden diese Tumor‑„Mini‑Organe“ mit passenden gesunden Lungenorganoiden desselben Patienten verglichen, zeigen sie, wie Ärztinnen und Ärzte eines Tages vorhersehen könnten, welche Therapien wirken, welche versagen und wie gefährliche Nebenwirkungen vermieden werden können, bevor der Patient behandelt wird.
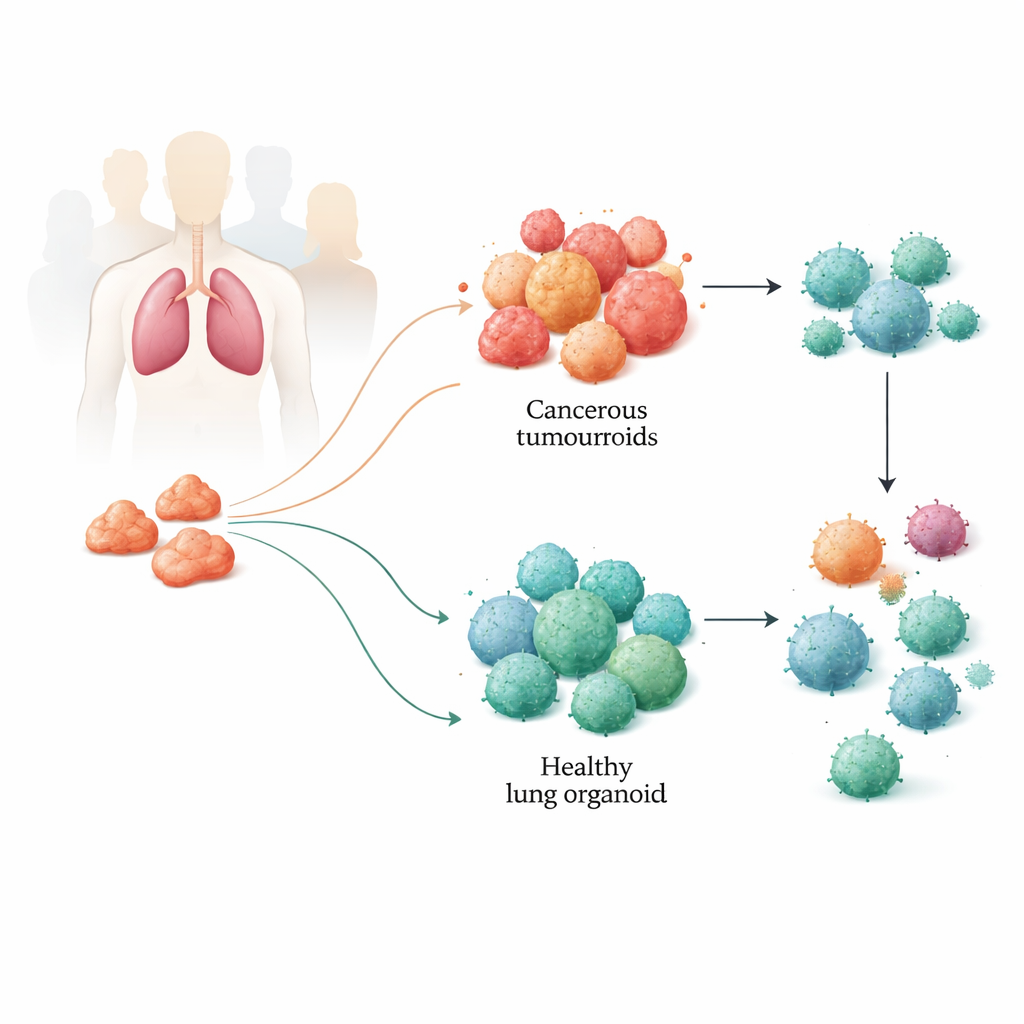
Miniatur‑Lungen aus Patientengewebe aufbauen
Das Team entnahm Tumorproben und angrenzendes gesundes Lungengewebe von Patientinnen und Patienten während Lungenkrebsoperationen. Aus diesen Proben züchteten sie dreidimensionale Strukturen, sogenannte Organoide: Tumouroide aus Krebsgewebe und gesunde Organoide aus normaler Lunge. Diese winzigen Kugeln organisieren sich selbst und lassen sich über viele Monate am Leben erhalten. Sorgfältige genetische, epigenetische und proteomische Analysen zeigten, dass die Tumouroide die wesentlichen molekularen Merkmale der ursprünglichen Tumoren bewahrten, einschließlich häufiger Lungenkrebs‑Mutationen und der komplexen Zellzusammensetzung. Die gesunden Organoide wiederum behielten die Kennzeichen nicht‑krebsartiger Lungenzellen, sodass die Forschenden ein zuverlässiges Neben‑einander‑Modell für die Erkrankung und das normale Lungengewebe jedes Patienten erhielten.
Realitätsnahe Reaktionen auf Medikamente abbilden
Um zu prüfen, ob diese Mini‑Organe wirklich widerspiegeln, was bei Patientinnen und Patienten geschieht, setzten die Forschenden die Tumouroide denselben Chemotherapien und zielgerichteten Medikamenten aus, die die Patienten bereits erhalten hatten. Mit Live‑Zell‑Bildgebung und Vitalitätsassays stellten sie fest, dass sich Tumouroide oft ähnlich verhielten wie die ursprünglichen Tumoren in der Klinik: Proben von Patientinnen und Patienten, deren Tumoren einem Medikament widerstanden, zeigten im Experiment ebenfalls Resistenz, während Tumouroide von Teilansprechern empfindlicher waren. Proteomische Profile — also die gleichzeitige Messung von Tausenden Proteinen — offenbarten Muster, die mit Medikamentenresistenz verknüpft sind, etwa hohe Mengen an Molekülen, die zuvor mit schlechter Ansprechrate auf Platin‑Chemotherapie assoziiert wurden. Diese Befunde deuten darauf hin, dass Tumouroide genutzt werden könnten, um vorherzusagen, ob ein bestimmtes Medikament einem individuellen Patienten wahrscheinlich helfen wird.
Maßgeschneidertes Testen von Immunzellen der nächsten Generation
Der Kern der Studie ist eine Pipeline zur Anpassung der CAR‑T‑Zelltherapie, einem kraftvollen Ansatz, bei dem die T‑Zellen eines Patienten so gentechnisch verändert werden, dass sie spezifische Marker auf Krebszellen erkennen. Die Wissenschaftlerinnen und Wissenschaftler untersuchten zunächst Tumor‑ und gesundes Gewebe sowie die dazugehörigen Organoide auf potenzielle Zielmoleküle an der Zelloberfläche. Anschließend generierten sie Panels von CAR‑T‑Zellen — mit einer virenfreien Geneditierungsmethode —, die vielversprechende Ziele wie HER2 oder PDL1 erkennen, die bei manchen Lungenkrebsformen vorkommen. Durch das Ko‑Kultivieren dieser CAR‑T‑Zellen mit Tumouroiden und gesunden Organoiden konnten sie gleichzeitig bewerten, wie stark die Immunzellen aktiviert wurden, wie viel Tumorschaden sie anrichteten und ob sie gesundem Lungengewebe schadeten.
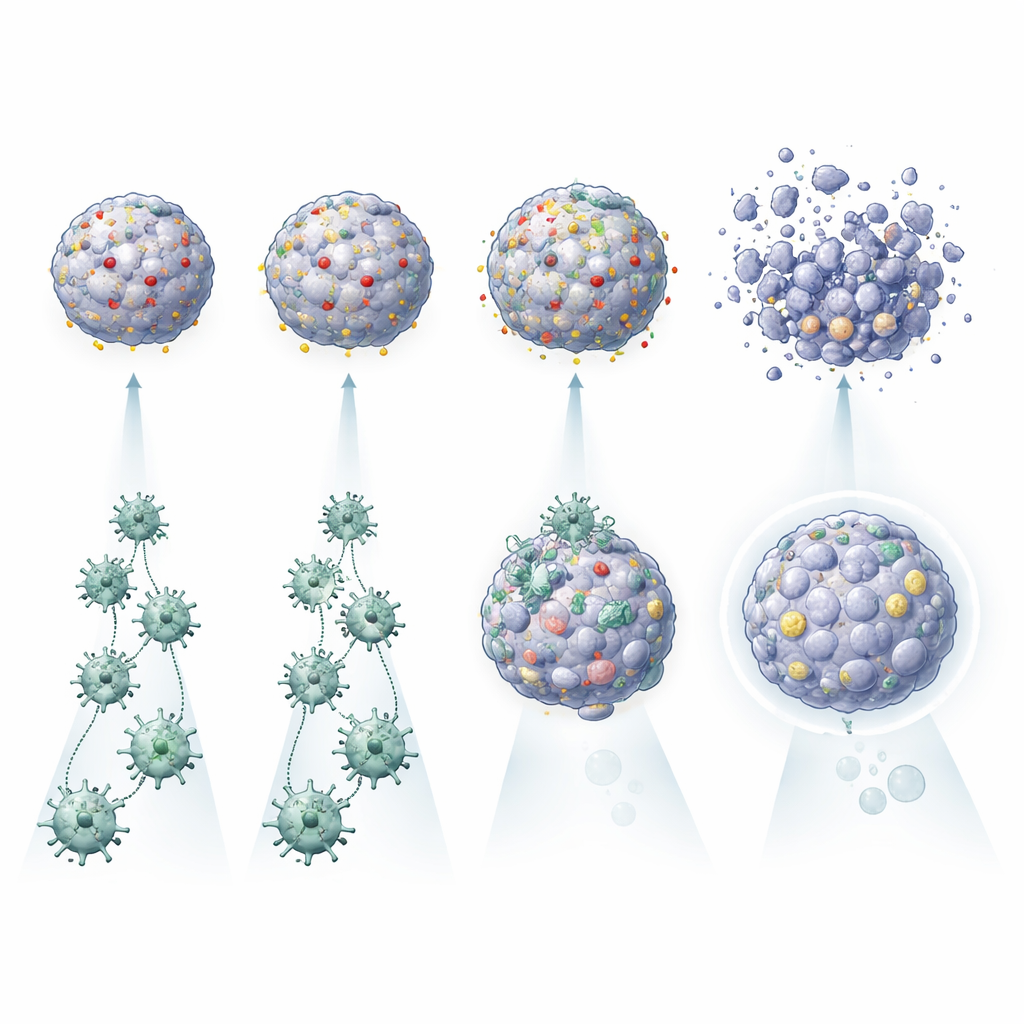
Warum manche Tumoren CAR‑T‑Zellen widerstehen
Ein auffälliges Ergebnis war, dass allein die Aktivierung von CAR‑T‑Zellen kein wirksames Tumorvernichten garantierte. In den Tumouroiden mancher Patientinnen und Patienten leuchteten CAR‑T‑Zellen auf und setzten entzündliche Moleküle frei, richteten aber nur mäßigen Schaden an den Krebs‑Mini‑Organen an. Bei anderen, insbesondere solchen mit vielen Kopien des Zielmoleküls an der Tumoroberfläche, zerstörten dieselben CAR‑T‑Zellen die Tumouroide deutlich effizienter. Die Plattform erfasste auch subtilere Einflüsse: Tumouroide, die bestimmte Zytokine wie IL‑6 sezernierten, schienen die CAR‑T‑Aktivität zu unterstützen, während Tumouroide, die reich an Autophagie‑ und Immun‑Evasions‑Proteinen waren oder unter Entzündungsbedingungen PDL1 stark hochfahren konnten, schwerer zu eliminieren waren. Durch den Vergleich jedes Tumors mit seinen eigenen gesunden Organoiden konnte das Team außerdem Patientinnen und Patienten identifizieren, bei denen ein bestimmtes CAR‑Design normales Lungengewebe verschonen könnte — oder unvertretbare Risiken darstellen würde.
Was das für die zukünftige Krebsbehandlung bedeuten könnte
Einfache gesagt zeigt diese Arbeit, dass patientenabgeleitete Lungen‑Tumouroide als realistische „Crash‑Test‑Dummies“ sowohl für Standardmedikamente als auch für ausgefeilte Immuntherapien dienen können. Das Modell reproduziert echte Patientenreaktionen auf Behandlungen, erklärt, warum manche Tumoren empfindlich sind, andere resistent bleiben, und macht deutlich, wann ein vielversprechender CAR‑T‑Ansatz auch gesunde Lungenzellen schädigen könnte. Zwar sind weitere Verfeinerungen nötig, doch weist diese Plattform in eine Zukunft, in der Onkologinnen und Onkologen die Mini‑Tumoren eines Patienten nutzen, um Therapien — einschließlich maßgeschneiderter CAR‑T‑Zellen — auszuwählen und zu optimieren, bevor sie die Patientinnen und Patienten den Risiken aussetzen.
Zitation: Ehlen, L., Farrera-Sal, M., Szyska, M. et al. Lung tumouroids as a testing platform for precision CAR T cell therapy. Nat. Biomed. Eng 10, 815–831 (2026). https://doi.org/10.1038/s41551-025-01594-3
Schlüsselwörter: Lungenkrebs, Organoide, CAR‑T‑Zelltherapie, präzisionsmedizin, Immuntherapie‑Resistenz